Los trastornos ácido-base son condiciones fisiológicas que reflejan alteraciones en el equilibrio entre ácidos y bases en el organismo, lo que puede afectar el pH sanguíneo. Para evaluar con precisión el estado ácido-base, se requiere tanto un análisis de gases en sangre como un panel químico, ya que proporcionan información sobre el pH, la concentración de bicarbonato (HCO3-) y el dióxido de carbono (Pco2), entre otros parámetros.
El pH sanguíneo venoso es típicamente entre 0.03 y 0.04 unidades más bajo que el pH sanguíneo arterial, aunque sigue siendo una aproximación bastante cercana al pH arterial. Si se requiere una evaluación más precisa del pH sanguíneo y los niveles de Pco2, es necesario realizar un análisis de gases arteriales. El bicarbonato (HCO3-) se calcula mediante la ecuación de Henderson-Hasselbalch, lo que significa que el valor de bicarbonato medido en un panel de electrolitos es el utilizado en este cálculo. La ecuación de Henderson-Hasselbalch es la siguiente:
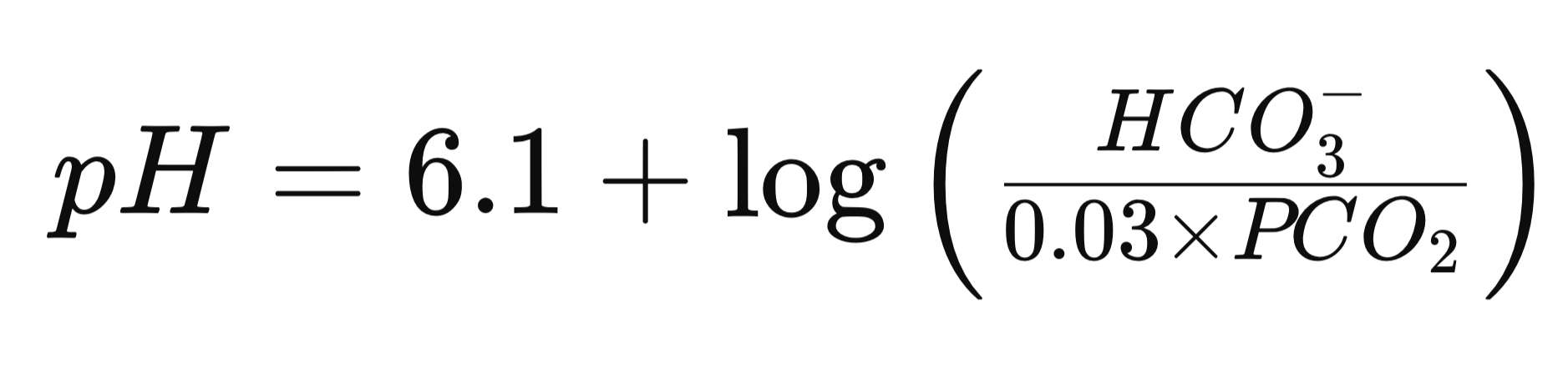
Los trastornos primarios ácido-base pueden ser causados por alteraciones en el bicarbonato sérico o en el Pco2. El primer paso para identificar la causa del trastorno es observar el pH en un análisis de gases sanguíneos, ya sea venoso o arterial. Si las variaciones en el pH son secundarias a cambios en los niveles de HCO3-, se trata de un trastorno metabólico. Por otro lado, si los cambios en el pH se deben a alteraciones en el Pco2, el trastorno será de origen respiratorio.
En cuanto al pH, si este es menor a 7.40, el proceso primario es la acidosis, que puede ser de origen respiratorio (con un Pco2 superior a 40 mmHg) o metabólico (con un HCO3- menor a 24 mEq/L). Si el pH es mayor a 7.40, el proceso primario es la alcalosis, que también puede ser respiratoria (con un Pco2 inferior a 40 mmHg) o metabólica (con un HCO3- superior a 24 mEq/L).
En condiciones fisiológicas normales, los riñones compensan los trastornos ácido-base respiratorios, mientras que los pulmones compensan los trastornos metabólicos para mantener el pH en un rango estrechamente regulado. Por ejemplo, en la acidosis metabólica (pH bajo, HCO3- bajo), la ventilación alveolar aumenta, lo que provoca una disminución de los niveles de Pco2, acercando el pH al rango normal. De manera similar, en la acidosis respiratoria (pH bajo, Pco2 alto), los riñones excretan iones de hidrógeno (H+) y aumentan los niveles de HCO3-, lo que también contribuye a normalizar el pH.
Sin embargo, es importante entender que esta compensación solo puede acercar el pH al valor normal, pero no puede corregir completamente el trastorno. Para normalizar el pH completamente, se debe tratar y corregir el trastorno primario subyacente. La intervención clínica depende, por lo tanto, de identificar y tratar la causa raíz del desequilibrio ácido-base, ya sea respiratoria o metabólica.
Un trastorno ácido-base simple ocurre cuando hay un único trastorno primario, ya sea respiratorio o metabólico, acompañado de una respuesta compensatoria apropiada. Este tipo de trastorno se caracteriza por la alteración de un solo sistema (respiratorio o metabólico) y una compensación del otro sistema, diseñada para restaurar el equilibrio ácido-base y mantener el pH dentro de un rango fisiológico estrecho. Por ejemplo, en una acidosis metabólica, los pulmones compensan mediante un aumento de la ventilación alveolar, lo que reduce el dióxido de carbono y ayuda a elevar el pH hacia niveles más normales. Similarmente, en una acidosis respiratoria, los riñones compensan mediante la excreción de iones de hidrógeno, aumentando el bicarbonato para contrarrestar el descenso del pH.
Por otro lado, un trastorno ácido-base mixto ocurre cuando coexisten dos o más trastornos primarios, ya sean respiratorios o metabólicos, lo que hace que el diagnóstico y la interpretación de los resultados sean más complejos. En un trastorno mixto, las respuestas compensatorias de un sistema pueden enmascarar o contrarrestar los efectos de otro trastorno, lo que dificulta la evaluación precisa del estado ácido-base y el pH sanguíneo. En estos casos, el diagnóstico requiere una cuidadosa consideración de todos los factores involucrados para poder identificar los trastornos primarios y sus interacciones.
Diagnosticar un trastorno ácido-base requiere un enfoque sistemático que combine la interpretación de los resultados de los análisis de gases sanguíneos y los valores de otros electrolitos en sangre, como el bicarbonato. Primero, es esencial identificar el trastorno primario, ya sea respiratorio o metabólico, a partir de la alteración en el pH y los niveles de dióxido de carbono o bicarbonato. Una vez que se ha determinado el trastorno primario, se debe evaluar si la respuesta compensatoria es adecuada.
Paso 1: Examinar el pH en un análisis de gases sanguíneos para determinar el trastorno primario, ya sea acidemia o alcalemia.
El primer paso en el análisis del estado ácido-base consiste en revisar el pH de la sangre, ya sea arterial o venosa, a través de un análisis de gases sanguíneos. El pH refleja el equilibrio entre los ácidos y las bases en el cuerpo. Si el pH está por debajo de 7.35, se considera que existe acidosis, mientras que un pH superior a 7.45 indica alcalosis. El valor del pH proporciona una visión inicial de si el trastorno es ácido (acidemia) o alcalino (alcalemia), lo que ayudará a guiar el diagnóstico hacia un trastorno respiratorio o metabólico, ya que ambos pueden causar estas alteraciones en el pH.
Paso 2: Revisar el valor del bicarbonato (HCO3–) sérico para determinar si el trastorno primario es metabólico.
Una vez determinado que el pH está alterado, el siguiente paso es examinar el nivel de bicarbonato en la sangre. El bicarbonato es un principal regulador del equilibrio ácido-base y juega un papel crucial en los trastornos metabólicos. Si el bicarbonato está fuera de los rangos normales (normalmente entre 22 y 26 mEq/L) y se encuentra disminuido, se sugiere un trastorno metabólico, como la acidosis metabólica o la alcalosis metabólica. Si el bicarbonato es normal o elevado en un contexto de acidosis o alcalosis, entonces el trastorno probablemente tiene un origen respiratorio, ya que el cuerpo intenta compensar el desequilibrio en el pH.
Paso 3: Calcular el intervalo aniónico.
El intervalo aniónico es una medida útil para identificar la causa de la acidosis metabólica. Este valor se calcula restando la concentración de los cationes (principalmente sodio) de la concentración de los aniones (como el cloro y el bicarbonato) en la sangre. La fórmula general para calcular el intervalo aniónico es:
Intervalo aniónico = [Sodio] – ([Cloro] + [Bicarbonato])
Un intervalo aniónico elevado puede indicar la presencia de ácidos no medidos en la sangre, como en el caso de la acidosis metabólica asociada con la acumulación de productos de desecho, como en la cetoacidosis diabética o la insuficiencia renal. Un intervalo aniónico normal o bajo, en cambio, sugiere que la acidosis es de origen gastrointestinal o renal.
Paso 4: Calcular el «delta gap» (diferencia del intervalo aniónico).
El «delta gap» es una herramienta que se utiliza para evaluar si hay un trastorno ácido-base mixto en presencia de una acidosis metabólica. Este cálculo compara el cambio en el intervalo aniónico con el cambio en el bicarbonato. Si el «delta gap» es mayor de lo esperado, puede indicar que un segundo trastorno ácido-base está presente, lo que complicaría el diagnóstico y tratamiento. El «delta gap» ayuda a identificar trastornos combinados, como una acidosis metabólica acompañada de una alcalosis respiratoria o viceversa.
Paso 5: Evaluar la magnitud de la compensación.
Una vez identificado el trastorno ácido-base primario, es crucial evaluar la respuesta compensatoria del cuerpo. Los sistemas respiratorio y renal trabajan para contrarrestar los efectos de la acidosis o alcalosis y devolver el pH hacia un rango normal. La compensación respiratoria ocurre rápidamente, mientras que la compensación renal puede llevar más tiempo. En la acidosis metabólica, por ejemplo, la compensación respiratoria implica un aumento de la ventilación para reducir el dióxido de carbono y aumentar el pH. Si la compensación es adecuada, el pH debería acercarse al valor normal, aunque no se espera una corrección completa del desequilibrio. La magnitud de la compensación también puede proporcionar pistas sobre la gravedad y la cronología del trastorno.
Paso 6: Examinar al paciente para determinar si los signos clínicos son compatibles con el análisis ácido-base.
El último paso es correlacionar los hallazgos del análisis ácido-base con la condición clínica del paciente. Es esencial que los resultados de laboratorio sean coherentes con los signos y síntomas clínicos observados en el paciente. Por ejemplo, un paciente con acidosis metabólica puede presentar respiración rápida y profunda (respiración de Kussmaul) debido a la compensación respiratoria. Un paciente con alcalosis metabólica puede mostrar signos de hipocalcemia, como espasmos musculares o tetania. La evaluación clínica completa permite confirmar el diagnóstico, determinar la gravedad del trastorno ácido-base y guiar el tratamiento adecuado.
Una respuesta compensatoria adecuada es aquella que corrige el pH de manera que se acerque a su valor normal, pero sin llegar a una normalización total, ya que los mecanismos compensatorios no son capaces de restaurar completamente el equilibrio ácido-base sin corregir la causa primaria del trastorno. Si la respuesta compensatoria es insuficiente o excesiva, esto sugiere que existe otro trastorno ácido-base primario que coexiste con el trastorno identificado inicialmente. Una respuesta insuficiente indicaría que el sistema compensatorio no está funcionando correctamente o que el trastorno primario es demasiado grave para ser compensado adecuadamente. Por otro lado, una respuesta exagerada podría indicar que se está produciendo una compensación de otro trastorno no identificado o que hay una interacción entre varios trastornos primarios, lo que resulta en un trastorno mixto.
El cálculo del intervalo aniónico sérico es una herramienta clave en la evaluación de los trastornos ácido-base, especialmente en el contexto de la acidosis metabólica. Existen dos razones principales por las cuales se debe calcular este intervalo: en primer lugar, ayuda a identificar la causa subyacente de la acidosis metabólica, y en segundo lugar, permite determinar la presencia de una acidosis metabólica con intervalo aniónico elevado, la cual puede estar presente incluso cuando la concentración de bicarbonato sérico no está disminuida.
El intervalo aniónico es la diferencia entre los principales cationes (sodio) y los principales aniones (cloro y bicarbonato) en la sangre. Este cálculo es útil porque, en muchos casos de acidosis metabólica, un aumento en el intervalo aniónico puede señalar la acumulación de ácidos no medidos en la sangre, como sucede en condiciones como la cetoacidosis diabética, la insuficiencia renal crónica o la intoxicación por metanol. Un intervalo aniónico elevado sugiere que la acidosis no es simplemente un resultado de la pérdida de bicarbonato, sino que también podría involucrar la acumulación de ácidos adicionales que no se miden de manera rutinaria.
En los pacientes con trastornos de acidosis metabólica, es importante calcular el «delta gap», que es la diferencia entre el cambio en el intervalo aniónico y el cambio en el bicarbonato sérico. Este cálculo ayuda a determinar si hay una acidosis metabólica mixta, que involucra tanto un aumento en el intervalo aniónico (debido a ácidos no medidos) como una disminución del bicarbonato. Si el delta gap no es congruente con el cambio en el bicarbonato, esto puede indicar la presencia de un trastorno ácido-base adicional, lo que complica el diagnóstico y tratamiento.
En los trastornos de acidosis con un intervalo aniónico elevado, es esperado que por cada aumento en el intervalo aniónico, se produzca una disminución proporcional en el bicarbonato (aproximadamente un milimol por milimol). Es decir, un aumento en el intervalo aniónico refleja la acumulación de ácidos que, a su vez, reduce la concentración de bicarbonato para mantener el equilibrio ácido-base.
Por lo tanto, es importante corregir el valor del bicarbonato sérico (HCO3–) para obtener una estimación más precisa del trastorno ácido-base en curso. Para ello, se debe calcular el bicarbonato corregido, sumando el cambio en el intervalo aniónico al valor del bicarbonato sérico. Este valor corregido proporciona una evaluación más precisa del estado ácido-base y permite detectar la presencia de trastornos concomitantes.
Si el bicarbonato corregido es mayor de lo normal (24 mEq/L), esto sugiere la presencia de alcalosis metabólica concomitante, ya que la acumulación de bases adicionales puede estar ocurriendo junto con la acidosis metabólica. Por el contrario, si el valor corregido de bicarbonato es inferior al normal, esto indica la presencia de una acidosis metabólica con intervalo aniónico normal, lo que se asocia comúnmente con trastornos como la acidosis láctica o la acidosis por diarrea.

Fuente y lecturas recomendadas:
- Goldman, L., & Schafer, A. I. (Eds.). (2020). Goldman-Cecil Medicine (26th ed.). Elsevier.
- Loscalzo, J., Fauci, A. S., Kasper, D. L., Hauser, S. L., Longo, D. L., & Jameson, J. L. (Eds.). (2022). Harrison. Principios de medicina interna (21.ª ed.). McGraw-Hill Education.
- Papadakis, M. A., McPhee, S. J., Rabow, M. W., & McQuaid, K. R. (Eds.). (2024). Diagnóstico clínico y tratamiento 2025. McGraw Hill.
- Rozman, C., & Cardellach López, F. (Eds.). (2024). Medicina interna (20.ª ed.). Elsevier España.
- Seifter JL et al. Disorders of acid-base balance: new perspectives. Kidney Dis (Basel). 2017;2:170. [PMID: 28232934]

Fuente y lecturas recomendadas:
- Goldman, L., & Schafer, A. I. (Eds.). (2020). Goldman-Cecil Medicine (26th ed.). Elsevier.
- Loscalzo, J., Fauci, A. S., Kasper, D. L., Hauser, S. L., Longo, D. L., & Jameson, J. L. (Eds.). (2022). Harrison. Principios de medicina interna (21.ª ed.). McGraw-Hill Education.
- Papadakis, M. A., McPhee, S. J., Rabow, M. W., & McQuaid, K. R. (Eds.). (2024). Diagnóstico clínico y tratamiento 2025. McGraw Hill.
- Rozman, C., & Cardellach López, F. (Eds.). (2024). Medicina interna (20.ª ed.). Elsevier España.
Originally posted on 21 de marzo de 2025 @ 10:24 PM