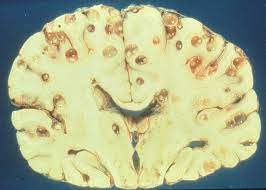
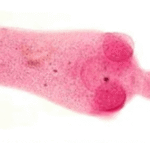
La cisticercosis es una enfermedad parasitaria causada por la infección de los tejidos humanos con quistes de Taenia solium, un parásito que se desarrolla cuando los seres humanos ingieren alimentos contaminados con huevos provenientes de heces humanas. En este contexto, los seres humanos actúan como hospedadores intermedios del parásito. Este ciclo de vida tiene lugar cuando los huevos de Taenia solium son excretados en las heces de personas infectadas y, al contaminar el entorno, se incorporan a la cadena alimentaria. Al consumir alimentos o agua contaminados, los seres humanos ingieren estos huevos, los cuales liberan larvas en su tracto digestivo que se diseminan a través de la circulación sanguínea hacia diferentes tejidos del cuerpo, especialmente el cerebro, donde forman los quistes característicos de la cisticercosis.
La prevalencia de la cisticercosis es elevada en las regiones donde el parásito es endémico, lo que incluye áreas de México, América Central y América del Sur, Filipinas y el sudeste asiático. Se estima que aproximadamente 20 millones de personas se infectan anualmente con cisticercos, lo que conlleva a la aparición de síntomas neurológicos en alrededor de 400,000 personas y alrededor de 50,000 muertes al año. En algunas de estas zonas endémicas, se han registrado tasas de prevalencia de anticuerpos que alcanzan hasta el 10% de la población, lo que indica una amplia exposición al parásito en la comunidad.
La cisticercosis se ha identificado como una de las principales causas de convulsiones en los países en desarrollo, así como entre los inmigrantes provenientes de países endémicos hacia Estados Unidos. En América Latina, se estima que entre 0.5 y 1.5 millones de personas padecen de epilepsia secundaria a esta infección. El impacto de la cisticercosis no solo es importante desde un punto de vista médico, sino que también plantea un desafío significativo en términos de salud pública, dado que las secuelas neurológicas de la infección pueden causar discapacidades a largo plazo y complicar la calidad de vida de los afectados.
Manifestaciones clínicas
La neurocisticercosis es una manifestación de la infección por Taenia solium que afecta al sistema nervioso central y puede dar lugar a una variedad de lesiones intracerebrales, subaracnoideas, en la médula espinal y quistes intraventriculares. Dependiendo de la gravedad y la extensión de la infección, pueden estar presentes tanto lesiones aisladas como múltiples, las cuales pueden persistir durante años sin que se presenten síntomas evidentes. Estas lesiones suelen desarrollarse de manera insidiosa debido a la inflamación local o a la obstrucción ventricular provocada por la acumulación de quistes en determinadas áreas del cerebro o la médula espinal.
Los síntomas más comunes de la neurocisticercosis incluyen convulsiones, déficits neurológicos focales, alteraciones en la cognición y enfermedades psiquiátricas. En muchos casos, los síntomas pueden tardar en aparecer, ya que los quistes pueden permanecer inactivos o sin causar efectos graves durante un largo periodo de tiempo. Sin embargo, cuando los quistes se localizan en los ventrículos cerebrales, los síntomas se desarrollan de forma más rápida y dramática. Los pacientes pueden presentar hidrocefalia (acumulación de líquido cefalorraquídeo en el cerebro) y signos de irritación meníngea, como dolor de cabeza intenso, vómitos, papiledema (hinchazón del nervio óptico) y pérdida visual. Estos hallazgos son característicos de la presencia de quistes intraventriculares, que afectan la dinámica del líquido cefalorraquídeo y la presión intracraneal.
Una forma particularmente agresiva de la neurocisticercosis es la cisticercosis racemosa, que se caracteriza por la proliferación masiva de los quistes en la base del cerebro. Esta forma de la enfermedad puede alterar de manera significativa el estado de conciencia y, si no se trata de manera adecuada, puede llevar a la muerte. Los pacientes con esta condición pueden experimentar un deterioro grave de sus funciones cerebrales debido a la compresión y la inflamación en áreas críticas del sistema nervioso central.
Las lesiones en la médula espinal también pueden ser observadas en algunos casos, y estas tienden a presentar hallazgos focales progresivos, lo que puede llevar a la pérdida de funciones motoras o sensoriales en una parte específica del cuerpo, dependiendo de la localización de los quistes. Sin embargo, en los casos en los que la cisticercosis afecta a órganos fuera del sistema nervioso central, la enfermedad suele ser clínicamente benigna.
La afectación de los músculos es poco frecuente, pero en algunos casos puede causar molestias, que se diagnostican mediante radiografías musculares, las cuales revelan múltiples lesiones calcificadas. Por otro lado, cuando la cisticercosis afecta la piel, suele presentarse como múltiples lesiones dérmicas palpables, generalmente indoloras. La implicación de los ojos puede dar lugar a ptosis (caída del párpado) debido a la invasión de los músculos extraoculares o a anormalidades intraoculares, que pueden comprometer la visión del paciente.
Exámenes diagnósticos
El diagnóstico de la neurocisticercosis generalmente requiere una evaluación integral que combine hallazgos clínicos, de laboratorio y de imágenes, ya que la presentación de la enfermedad puede ser diversa y sus síntomas no siempre son específicos. Para facilitar el diagnóstico, se utilizan los criterios diagnósticos revisados de Del Brutto de 2017, que han demostrado una alta sensibilidad y especificidad en la identificación de esta enfermedad. Estos criterios se basan en la integración de pruebas clínicas, serológicas y de imagen, lo que permite un diagnóstico más preciso y confiable.
La exploración del líquido cefalorraquídeo (LCR) es una herramienta valiosa en la evaluación de la neurocisticercosis. Los análisis del LCR pueden revelar pleocitosis linfocitaria o eosinofílica, lo que indica una respuesta inflamatoria en el sistema nervioso central. Además, puede haber una disminución de los niveles de glucosa y un aumento de la proteína, lo cual es característico de la inflamación meníngea que acompaña a la infección. Sin embargo, los resultados del LCR no siempre son definitivos, ya que pueden ser inespecíficos y deben interpretarse junto con otros hallazgos.
La serología desempeña un papel crucial en el diagnóstico, ya que permite detectar la presencia de anticuerpos y antígenos específicos contra Taenia solium. Existen ensayos altamente sensibles y específicos, como las pruebas de inmunoabsorción enzimática (ELISA) y los inmunoblotting relacionados, que son esenciales para confirmar la infección. No obstante, la sensibilidad de estas pruebas puede ser menor en los casos de lesiones únicas o calcificadas, lo que hace que en estos casos el diagnóstico se base en una combinación de métodos.
La neuroimagen mediante tomografía computarizada (TC) o resonancia magnética (RM) es indispensable para la evaluación de las lesiones cerebrales asociadas con la cisticercosis. En la mayoría de los casos, se observan múltiples quistes parenquimatosos en las imágenes, lo que es característico de la enfermedad. La calcificación parenquimatosa también es común, y su presencia puede ser un indicativo clave de la infección crónica o avanzada. Es recomendable realizar tanto TC como RM para obtener una visión completa del cuadro clínico. La TC es especialmente útil para identificar calcificaciones, mientras que la RM tiene una ventaja significativa al detectar lesiones más pequeñas y aquellas localizadas en los ventrículos cerebrales.
Los hallazgos típicos en las imágenes pueden ser altamente sugestivos del diagnóstico de neurocisticercosis, permitiendo a los médicos realizar una evaluación más precisa y tomar decisiones terapéuticas adecuadas. En resumen, la combinación de pruebas serológicas, análisis del líquido cefalorraquídeo y neuroimágenes (TC y RM) proporciona un enfoque diagnóstico robusto y confiable, que es crucial para el manejo efectivo de la enfermedad.
Tratamiento
El manejo médico de la neurocisticercosis ha sido objeto de controversia debido a que los beneficios de la eliminación de los quistes deben sopesarse con el riesgo potencial de una respuesta inflamatoria inducida por la muerte de los gusanos. El tratamiento con medicamentos antihelmínticos acelera la mejora radiológica en los casos de cisticercosis parenquimatosa, sin embargo, algunos ensayos clínicos aleatorizados han mostrado que el uso exclusivo de corticosteroides es igualmente efectivo que la terapia específica junto con corticosteroides para el control de las convulsiones. Esta información ha generado debate sobre el enfoque terapéutico más adecuado y ha resaltado la importancia de un tratamiento personalizado basado en las características individuales del paciente.
En términos generales, la mayoría de los expertos coinciden en que el tratamiento es recomendable para las lesiones activas, especialmente aquellas con una alta probabilidad de progresar, como los quistes intraventriculares. Este tipo de lesiones pueden ocasionar complicaciones graves debido a la obstrucción del flujo del líquido cefalorraquídeo o a la inflamación de estructuras cerebrales cruciales. Por otro lado, las lesiones inactivas y calcificadas probablemente no se benefician de una terapia antihelmíntica, ya que el parásito ha muerto y la presencia de calcificación indica una fase avanzada de la enfermedad, en la cual el daño ya ha sido realizado.
Además, el tratamiento cisticida debe evitarse en situaciones en las cuales exista un alto riesgo de hidrocefalia, como en los casos de implicación subaracnoidea. La eliminación de los quistes en este contexto puede desencadenar una reacción inflamatoria significativa, que podría agravar el riesgo de acumulación de líquido en los ventrículos cerebrales, provocando un aumento de la presión intracraneal que podría ser potencialmente mortal.
Cuando se considera que el tratamiento es adecuado, las terapias estándar incluyen el albendazol o el praziquantel. El albendazol se administra en dosis de 10 a 15 mg/kg/día por vía oral durante 8 días, mientras que el praziquantel se administra en dosis de 50 mg/kg/día por vía oral durante 15 a 30 días. En términos generales, el albendazol es probablemente la opción preferida debido a que ha demostrado una mayor eficacia en algunas comparaciones, y porque los corticosteroides parecen reducir los niveles circulantes de praziquantel, mientras que aumentan los niveles de albendazol. En algunos casos, aumentar la dosis de albendazol a 30 mg/kg/día por vía oral podría mejorar los resultados terapéuticos.
La combinación de albendazol con praziquantel también ha mostrado mejoras en los resultados comparado con el uso exclusivo de albendazol, especialmente en pacientes con múltiples quistes intraparenquimatosos viables. Los corticosteroides generalmente se administran junto con los antihelmínticos para controlar la inflamación y las respuestas inmunológicas del cuerpo ante la muerte de los quistes, aunque la dosificación de estos medicamentos no está completamente estandarizada y puede depender de la gravedad de los síntomas y la extensión de la enfermedad.
Es fundamental que los pacientes sean observados cuidadosamente para detectar cualquier signo de respuesta inflamatoria localizada, ya que esto puede afectar su evolución clínica. En muchos casos, la terapia anticonvulsiva será necesaria para controlar las convulsiones, y en aquellos con un aumento significativo de la presión intracraneal, puede ser necesario realizar una derivación para aliviar dicha presión. En los casos más complejos de neurocisticercosis o cuando la enfermedad presenta complicaciones no neurológicas sintomáticas, la extirpación quirúrgica de los quistes puede ser útil, ya sea como una medida para reducir los efectos locales de la inflamación o para mejorar el pronóstico global del paciente.

Fuente y lecturas recomendadas:
- Del Brutto OH. Human neurocysticercosis: an overview. Pathogens. 2022;1:1212. [PMID: 36297269]
- Garcia HH et al. Taenia solium cysticercosis and its impact in neurological disease. Clin Microbiol Rev. 2020;33:e00085–19. [PMID: 32461308]
- Pineda-Reyes R et al. Neurocysticercosis: an update on diagnosis, treatment, and prevention. Curr Opin Infect Dis. 2022;35:246. [PMID: 35665719]