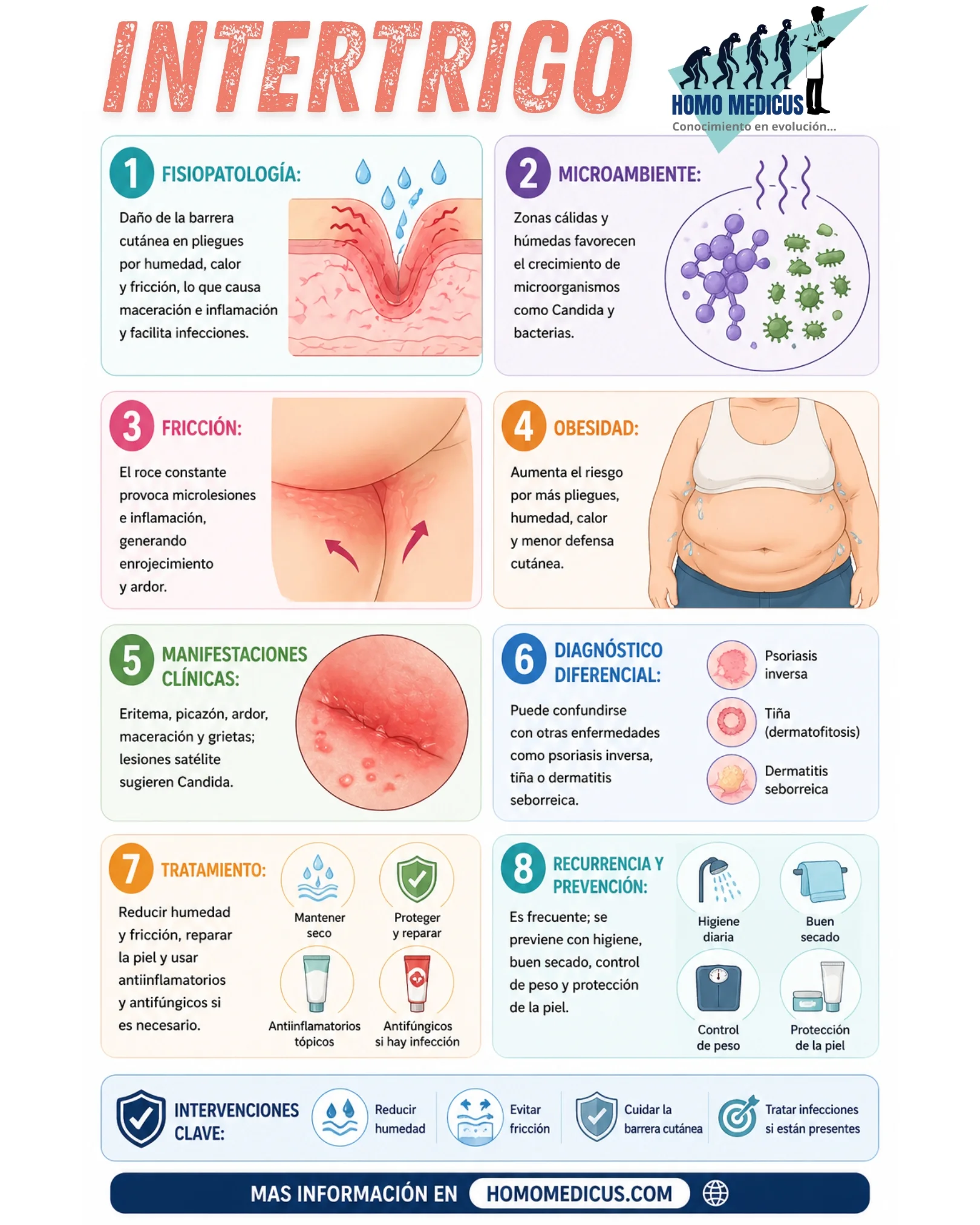
El intertrigo constituye una entidad dermatológica inflamatoria que emerge como consecuencia de la interacción sostenida entre factores físicos, microambientales y microbiológicos en superficies cutáneas en aposición. Su fisiopatología se comprende mejor al analizar la integridad de la barrera epidérmica, particularmente del estrato córneo, el cual actúa como primera línea de defensa frente a agresiones externas. En condiciones normales, este estrato mantiene un equilibrio homeostático entre hidratación, cohesión celular y función antimicrobiana mediada por lípidos intercelulares y péptidos antimicrobianos. Sin embargo, la exposición prolongada a calor, humedad y fricción altera profundamente estos mecanismos.
El aumento de la temperatura local incrementa la actividad de las glándulas sudoríparas ecrinas, generando una acumulación de sudor en espacios intertriginosos. Este sudor contiene electrolitos, urea y compuestos nitrogenados que, en condiciones de evaporación limitada, promueven la maceración del estrato córneo. La maceración implica una sobrehidratación que altera la organización de los corneocitos y debilita las uniones intercelulares, particularmente los corneodesmosomas, lo que reduce la resistencia mecánica de la piel. Se ha demostrado que la hidratación excesiva del estrato córneo incrementa su permeabilidad y disminuye su cohesión estructural, facilitando la penetración de irritantes y microorganismos.
Simultáneamente, la fricción mecánica repetitiva entre superficies cutáneas genera microtraumatismos. Estos microtraumatismos inducen la liberación de citocinas proinflamatorias como interleucina 1α y factor de necrosis tumoral alfa por parte de queratinocitos dañados. Este proceso activa cascadas inflamatorias locales que conducen a vasodilatación, aumento de la permeabilidad vascular y reclutamiento de células inmunitarias, manifestándose clínicamente como eritema y sensación de ardor.
La humedad persistente no solo favorece la maceración, sino que también altera el pH cutáneo, haciéndolo menos ácido. Este cambio en el microambiente facilita la proliferación de microorganismos oportunistas. Entre ellos destacan levaduras del género Candida, bacterias como Corynebacterium minutissimum y dermatofitos. Candida albicans, en particular, posee la capacidad de adherirse a queratinocitos mediante adhesinas específicas y formar hifas invasivas en condiciones de humedad elevada, lo que exacerba la inflamación y contribuye a la formación de lesiones eritematosas con bordes activos y pústulas satélite.
En el contexto de la obesidad, los mecanismos fisiopatológicos del intertrigo se intensifican de manera significativa. El incremento del tejido adiposo subcutáneo produce pliegues cutáneos más profundos y extensos, lo que incrementa el área de contacto piel con piel. Este aumento en la superficie de fricción eleva la carga mecánica sobre la epidermis. Además, el tejido adiposo actúa como un aislante térmico, dificultando la disipación del calor corporal y favoreciendo un microclima cálido en los pliegues. La obesidad también se asocia con hiperhidrosis relativa, lo que incrementa la humedad local.
A nivel sistémico, el tejido adiposo en exceso secreta adipocinas proinflamatorias como leptina y resistina, así como citocinas que inducen un estado inflamatorio crónico de bajo grado. Este estado puede alterar la respuesta inmunitaria cutánea, reduciendo la capacidad del huésped para controlar la proliferación microbiana. Asimismo, se ha documentado que individuos con obesidad presentan alteraciones en la microbiota cutánea, con un aumento en microorganismos potencialmente patógenos en áreas húmedas.
Clínicamente, el intertrigo se caracteriza por eritema bien delimitado en áreas intertriginosas, acompañado de prurito y sensación de ardor. La maceración conduce a un aspecto blanquecino y reblandecido de la piel, mientras que la fricción puede provocar fisuras dolorosas. En etapas más avanzadas, la denudación superficial expone capas epidérmicas más profundas, incrementando el riesgo de infección secundaria. La presencia de lesiones satélite sugiere candidiasis, mientras que una coloración marronácea con fluorescencia coral bajo luz de Wood es característica de eritrasma.
El diagnóstico diferencial es esencial debido a la superposición clínica con otras dermatosis. La psoriasis inversa, por ejemplo, presenta placas eritematosas bien definidas pero sin descamación evidente debido a la humedad. La dermatitis seborreica muestra eritema con escamas grasosas en áreas ricas en glándulas sebáceas. La tiña inguinal presenta bordes activos con descamación periférica, mientras que el eritrasma se asocia a infección bacteriana específica. Estas diferencias reflejan mecanismos patogénicos distintos, lo que justifica la necesidad de un diagnóstico preciso.
El manejo terapéutico del intertrigo se fundamenta en la restauración de la integridad de la barrera cutánea y la modificación del microambiente local. La reducción de la humedad mediante secado cuidadoso y el uso de materiales absorbentes disminuye la maceración. La aplicación de corticosteroides tópicos de baja potencia, como hidrocortisona al 1%, reduce la inflamación al inhibir la síntesis de mediadores proinflamatorios mediante la supresión de la fosfolipasa A2. Paralelamente, los antifúngicos azólicos como clotrimazol o imidazol interfieren con la síntesis de ergosterol en la membrana celular de los hongos, comprometiendo su viabilidad.
La recurrencia frecuente del intertrigo se explica por la persistencia de factores predisponentes. Mientras el microambiente cálido y húmedo no sea modificado, la piel permanece en un estado vulnerable. Por ello, las estrategias preventivas a largo plazo incluyen la reducción del peso corporal, el uso de ropa transpirable y la aplicación de barreras protectoras como óxido de zinc o petrolato, que disminuyen la fricción y la exposición a la humedad.
Fuente y lectura recomendada
- Bolognia, J. L., Schaffer, J. V., & Cerroni, L. (2018). Dermatology (4th ed.). Elsevier.
- Gabriel, S. E., & Otley, C. C. (2001). Pathophysiology of intertriginous skin disorders. Journal of the American Academy of Dermatology, 44(1), 1–12.
- James, W. D., Elston, D. M., Treat, J. R., Rosenbach, M. A., & Neuhaus, I. M. (2020). Andrews’ Diseases of the Skin: Clinical Dermatology (13th ed.). Elsevier.
- Korting, H. C., & Braun-Falco, O. (1996). The effect of detergents on skin pH and its consequences. Clinical Dermatology, 14(1), 23–29.
- Leyden, J. J., McGinley, K. J., & Foglia, A. N. (1987). The role of microorganisms in intertrigo. Journal of Investigative Dermatology, 88(3), 65–72.
- Naldi, L., & Rebora, A. (2009). Clinical practice: seborrheic dermatitis. New England Journal of Medicine, 360(4), 387–396.
- Scheinfeld, N. (2004). Obesity and dermatology. Clinics in Dermatology, 22(4), 303–309.
- Sobera, J. O., & Elewski, B. E. (2008). Fungal diseases. In Fitzpatrick’s Dermatology in General Medicine (7th ed.). McGraw-Hill.
- Wolf, R., & Wolf, D. (2012). Tinea cruris and intertrigo: diagnostic and therapeutic considerations. Clinics in Dermatology, 30(2), 137–141.