Durante milenios, la humanidad enfrentó el dolor quirúrgico mediante recursos empíricos derivados de plantas con propiedades psicoactivas y mediante intervenciones físicas destinadas a alterar de manera transitoria la percepción o la conducción nerviosa. Las preparaciones de Cannabis sativa, Hyoscyamus niger (henbane), Mandragora officinarum y Papaver somniferum fueron descritas en textos médicos antiguos por su capacidad para inducir somnolencia, analgesia parcial y estados de alteración de la conciencia. Los alcaloides presentes en estas especies, tales como los cannabinoides, la hiosciamina, la escopolamina y la morfina, actúan sobre receptores específicos del sistema nervioso central y periférico, modulando la neurotransmisión sináptica. La morfina, por ejemplo, ejerce su efecto analgésico a través de la activación de receptores opioides tipo μ, lo que inhibe la liberación de neurotransmisores excitatorios en las vías nociceptivas ascendentes, fenómeno demostrado en estudios neurofarmacológicos detallados sobre la transmisión del dolor. La escopolamina y la hiosciamina, por su parte, bloquean receptores muscarínicos colinérgicos, generando sedación y amnesia, aunque con efectos secundarios significativos como delirio y toxicidad cardiovascular.
Los métodos físicos, aunque rudimentarios, reflejan una comprensión incipiente de la fisiología. La aplicación de frío reduce la conducción nerviosa mediante la disminución de la velocidad de despolarización axonal, lo que atenúa la transmisión del impulso nociceptivo. La compresión de nervios periféricos interrumpe mecánicamente la conducción eléctrica, produciendo una analgesia localizada transitoria. La oclusión de la arteria carótida provoca hipoxia cerebral, lo que puede inducir pérdida de la conciencia, aunque con un alto riesgo de daño neurológico irreversible. La inducción de conmoción cerebral, utilizada de forma extrema, produce alteración difusa de la actividad neuronal, suprimiendo temporalmente la percepción consciente, pero con consecuencias impredecibles y potencialmente letales. Estos métodos carecían de control y reproducibilidad, lo que limitaba su utilidad clínica.
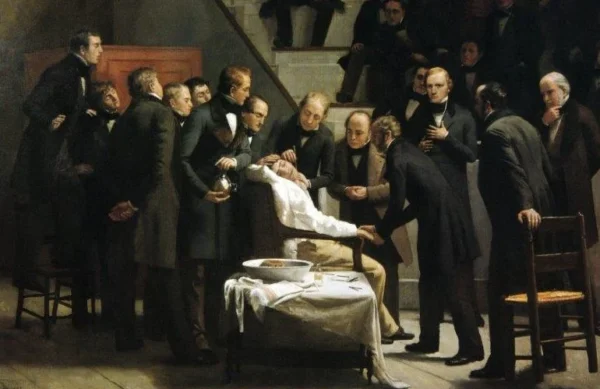
El advenimiento del éter dietílico como anestésico inhalado marcó un punto de inflexión en la historia de la medicina. Aunque su uso clínico se documenta desde 1842, la demostración pública de anestesia general en 1846 estableció un paradigma reproducible y relativamente seguro. El éter actúa principalmente mediante la potenciación de la neurotransmisión inhibitoria mediada por el ácido gamma-aminobutírico en receptores tipo A y la inhibición de receptores excitatorios como los del N-metil-D-aspartato, lo que resulta en depresión global del sistema nervioso central. Este avance permitió por primera vez la supresión controlada del dolor y la conciencia durante procedimientos quirúrgicos, lo que facilitó el desarrollo de la cirugía moderna.
Desde el punto de vista neurofisiológico, la anestesia general constituye un estado complejo que involucra múltiples sistemas neuronales. La inconsciencia se asocia con la interrupción de la conectividad funcional entre el tálamo y la corteza cerebral, particularmente en redes frontoparietales responsables de la integración consciente. La amnesia implica la inhibición de estructuras del lóbulo temporal medial, como el hipocampo, interfiriendo con la consolidación de la memoria episódica. La analgesia resulta de la supresión de las vías nociceptivas ascendentes y la activación de sistemas inhibitorios descendentes. La inhibición de reflejos autonómicos se logra mediante la depresión de centros bulbares y del sistema nervioso autónomo, reduciendo respuestas cardiovasculares y respiratorias al estímulo quirúrgico. La relajación del músculo esquelético se obtiene mediante la acción sobre la unión neuromuscular, ya sea de forma directa o mediante bloqueadores neuromusculares que antagonizan los receptores nicotínicos de acetilcolina.
Ningún agente anestésico único es capaz de producir de manera óptima todos estos efectos sin generar efectos adversos significativos. Por ejemplo, los agentes hipnóticos como el propofol inducen inconsciencia y amnesia de manera rápida, pero carecen de propiedades analgésicas robustas. Los opioides proporcionan analgesia potente, pero no inducen inconsciencia suficiente. Los agentes inhalados contribuyen a la amnesia y la inmovilidad, pero pueden deprimir la función cardiovascular. Esta limitación ha llevado al desarrollo del concepto de anestesia balanceada, en el cual se combinan múltiples fármacos con mecanismos de acción complementarios para lograr un perfil anestésico óptimo.
El anestésico ideal, desde una perspectiva farmacológica, debería poseer una cinética de inicio rápida, permitiendo una inducción suave de la inconsciencia, y una eliminación eficiente que facilite una recuperación pronta. Además, debería tener un amplio índice terapéutico, minimizando el riesgo de toxicidad incluso en presencia de variabilidad interindividual. Sin embargo, las propiedades fisicoquímicas que permiten una rápida penetración al sistema nervioso central, como la alta liposolubilidad, también pueden asociarse con acumulación tisular y efectos residuales prolongados, lo que representa un desafío en el diseño de nuevos agentes.
En la práctica contemporánea, la anestesia balanceada combina agentes intravenosos e inhalados para optimizar la seguridad y la eficacia. El propofol, un agente hipnótico intravenoso, actúa potenciando la actividad del receptor GABA tipo A, induciendo rápidamente la pérdida de la conciencia. El tiopental, un barbitúrico, comparte un mecanismo similar, aunque con mayor riesgo de acumulación. Los anestésicos inhalados, como los halogenados volátiles, modulan múltiples canales iónicos, incluyendo receptores GABA y canales de potasio, contribuyendo a la estabilidad del plano anestésico. El óxido nitroso proporciona analgesia y reduce la concentración requerida de otros agentes inhalados. Los opioides, como la morfina o el fentanilo, se emplean para suprimir la respuesta al dolor quirúrgico.
La selección de la técnica anestésica depende de múltiples variables clínicas, incluyendo la naturaleza del procedimiento, el estado fisiológico del paciente y los objetivos terapéuticos. En intervenciones menores o procedimientos diagnósticos invasivos, el cuidado anestésico monitoreado combina sedantes con anestesia local, permitiendo mantener la ventilación espontánea y la capacidad de respuesta del paciente. Este enfoque se basa en la administración titulada de fármacos que modulan la ansiedad y el dolor sin inducir una depresión profunda del sistema nervioso central. En procedimientos más invasivos, se emplea una secuencia que incluye premedicación con benzodiacepinas para reducir la ansiedad y facilitar la amnesia, inducción con agentes intravenosos de acción rápida, y mantenimiento mediante una combinación de anestésicos inhalados y analgésicos opioides. Esta estrategia permite un control preciso de los distintos componentes del estado anestésico, mejorando los resultados clínicos y reduciendo la incidencia de complicaciones.


Fuente y lecturas recomendadas:
- Brown, E. N., Lydic, R., & Schiff, N. D. (2010). General anesthesia, sleep, and coma. New England Journal of Medicine, 363(27), 2638–2650.
- Franks, N. P. (2008). General anaesthesia: From molecular targets to neuronal pathways of sleep and arousal. Nature Reviews Neuroscience, 9(5), 370–386.
- Hemmings, H. C., & Egan, T. D. (2019). Pharmacology and physiology for anesthesia: Foundations and clinical application. Elsevier.
- Kandel, E. R., Koester, J. D., Mack, S. H., & Siegelbaum, S. A. (2021). Principles of neural science. McGraw-Hill.
- Miller, R. D., Cohen, N. H., Eriksson, L. I., Fleisher, L. A., & Wiener-Kronish, J. P. (2020). Miller’s anesthesia. Elsevier.
- Rang, H. P., Ritter, J. M., Flower, R. J., & Henderson, G. (2019). Rang and Dale’s pharmacology. Elsevier.
- Sneyd, J. R., & Rigby-Jones, A. E. (2010). New drugs and technologies, intravenous anaesthesia is on the move. British Journal of Anaesthesia, 105(3), 246–254.
- Yaksh, T. L., Wallace, M. S. (2018). Opioids, analgesia, and pain management. En Goodman & Gilman’s The Pharmacological Basis of Therapeutics. McGraw-Hill.