El desarrollo embrionario del diafragma constituye un proceso morfogenético altamente coordinado que integra migración celular, partición de cavidades corporales, señalización molecular y reorganización tridimensional del embrión en crecimiento. Esta complejidad explica por qué pequeñas alteraciones en cualquiera de sus etapas pueden generar anomalías estructurales graves con repercusiones funcionales significativas en la vida posnatal.
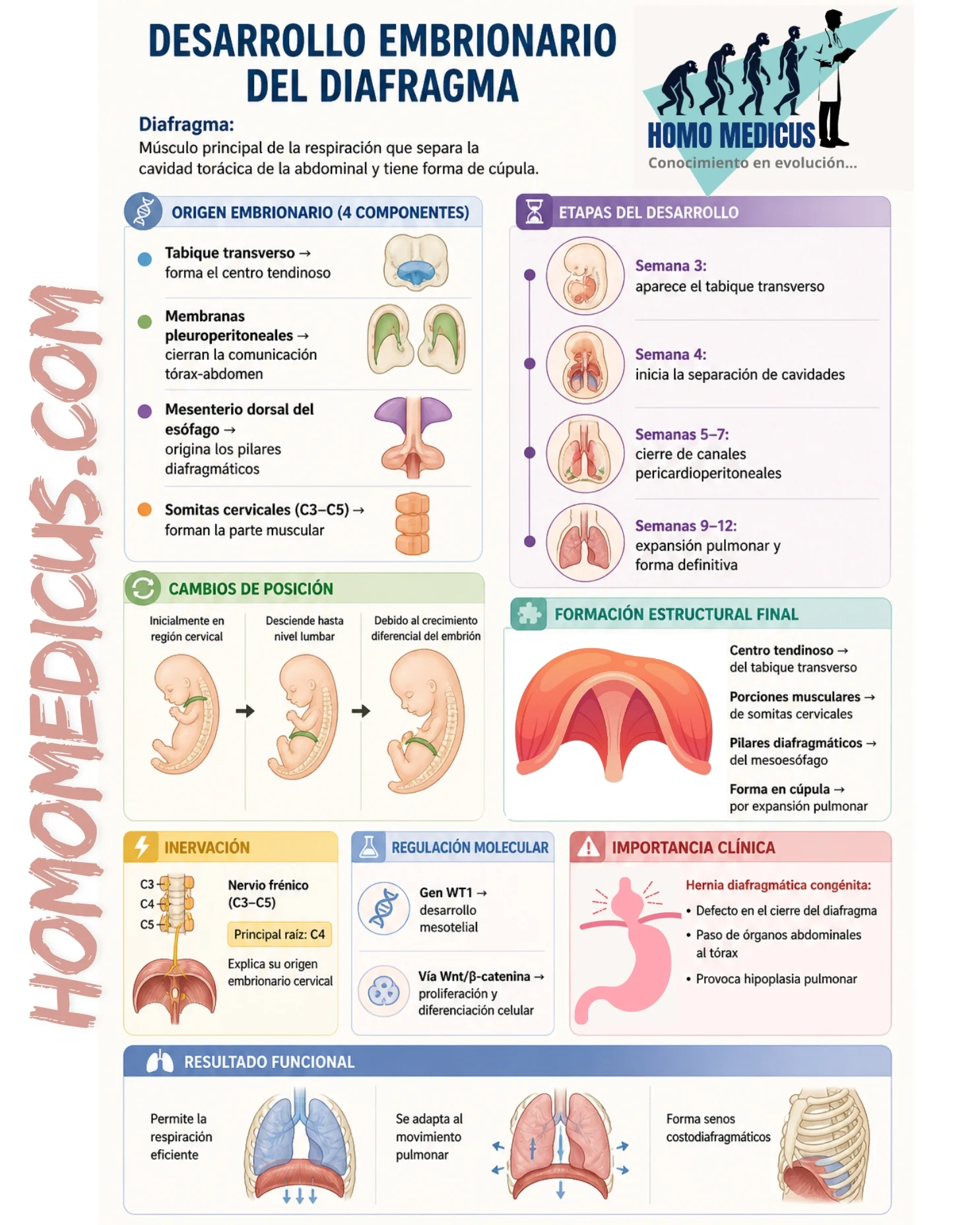
Eel diafragma se origina a partir de cuatro primordios mesodérmicos distintos que se integran progresivamente: el tabique transverso, las membranas pleuroperitoneales, el mesenterio dorsal del esófago y el componente muscular derivado de la pared corporal lateral. Cada uno de estos elementos no solo aporta una contribución estructural específica, sino que además participa en la regulación espacial y temporal del cierre de las cavidades corporales primitivas.
El tabique transverso aparece hacia finales de la tercera semana como una masa de mesodermo esplácnico localizada entre la cavidad pericárdica en desarrollo y el pedículo del saco vitelino. Su posición inicial cervical obedece al patrón cefalocaudal primitivo del embrión, en el cual las estructuras toracoabdominales aún no han experimentado el plegamiento longitudinal completo. Este tabique constituye el primordio del centro tendinoso del diafragma debido a su composición predominantemente fibrosa y a su limitada contribución miogénica. Su desplazamiento caudal progresivo durante las semanas subsecuentes es consecuencia directa del crecimiento diferencial del eje dorsoventral del embrión, particularmente del alargamiento de la columna vertebral, lo cual induce una aparente migración hacia niveles torácicos y posteriormente lumbares. Este fenómeno explica la trayectoria elongada del nervio frénico en el adulto y su origen cervical, evidenciando la estrecha relación entre morfogénesis estructural e inervación funcional.
Durante la cuarta semana, el plegamiento cefálico y lateral del embrión posiciona al tabique transverso entre la cavidad torácica primitiva y la cavidad abdominal en formación, pero sin lograr una separación completa. En este estadio persisten amplias comunicaciones bilaterales denominadas canales pericardioperitoneales, que conectan la cavidad pericárdica con la cavidad peritoneal. La persistencia transitoria de estas comunicaciones es fundamental para permitir el crecimiento y la expansión de estructuras como el esófago y los pulmones en desarrollo.
El cierre de estos canales depende de la aparición y expansión de las membranas pleuroperitoneales, estructuras mesodérmicas que emergen desde la pared dorsolateral del embrión y crecen ventromedialmente. Estas membranas desempeñan un papel crucial en la separación definitiva de las cavidades torácica y abdominal. Su fusión con el tabique transverso y con el mesenterio dorsal del esófago establece una barrera continua que constituye la base anatómica del diafragma. La importancia de este proceso radica en que cualquier retraso o defecto en la formación o fusión de estas membranas puede resultar en la persistencia de aberturas posterolaterales, las cuales son el sitio más frecuente de hernias diafragmáticas congénitas. La evidencia experimental ha demostrado que la alteración en la proliferación y migración de células mesoteliales en estas membranas compromete la integridad estructural del diafragma, favoreciendo defectos de cierre.
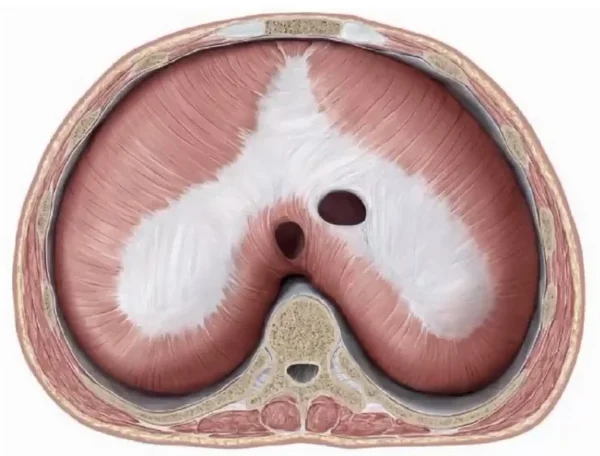
El mesenterio dorsal del esófago contribuye principalmente a la formación de los pilares diafragmáticos, estructuras musculares que anclan el diafragma a la columna vertebral. Este componente no solo proporciona soporte mecánico, sino que también establece una relación funcional con el hiato esofágico, permitiendo el paso del esófago y participando en mecanismos antirreflujo. Durante su desarrollo, células miogénicas migran hacia esta región y se organizan en fascículos musculares que cruzan la línea media, lo cual refleja una compleja coordinación entre señales de orientación celular y gradientes moleculares.
El componente muscular del diafragma deriva de mioblastos originados en las somitas cervicales C3 a C5. Estas células migran hacia las estructuras previamente formadas, especialmente hacia las membranas pleuroperitoneales, donde se diferencian en fibras musculares esqueléticas. Este proceso de migración está regulado por señales moleculares específicas, incluyendo factores de crecimiento y rutas de señalización que controlan la diferenciación miogénica. La conservación de la inervación cervical se debe a que los mioblastos arrastran consigo sus nervios segmentarios durante la migración, lo que explica la distribución del nervio frénico y su papel en la función respiratoria.
Entre las semanas 9 y 12, el crecimiento de los pulmones induce una expansión de las cavidades pleurales hacia la pared corporal lateral. Este proceso segmenta la pared en dos capas, contribuyendo a la configuración definitiva del diafragma. La interacción mecánica entre el crecimiento pulmonar y la resistencia del tejido diafragmático en formación es determinante para la adopción de su forma en cúpula. Esta morfología no es arbitraria, sino que responde a principios biomecánicos que optimizan la eficiencia ventilatoria, permitiendo una distribución homogénea de las presiones durante la inspiración.
A nivel molecular, el desarrollo diafragmático está regulado por redes genéticas complejas. El gen WT1 desempeña un papel esencial en la diferenciación del mesotelio y en la regulación de la proliferación celular en el tabique transverso y las membranas pleuroperitoneales. La alteración de su expresión se ha asociado con defectos estructurales del diafragma. Asimismo, la vía de señalización Wnt/β-catenina interviene en la regulación de la migración celular, la diferenciación miogénica y la apoptosis programada, procesos indispensables para la correcta formación del diafragma. La disrupción de esta vía puede generar defectos en la integración de los distintos componentes embrionarios, favoreciendo la aparición de hernias congénitas.
La hernia diafragmática congénita representa una consecuencia directa de la alteración en estos procesos. La presencia de un defecto diafragmático permite la herniación de vísceras abdominales hacia la cavidad torácica, lo cual interfiere con el desarrollo pulmonar normal al limitar el espacio disponible para la expansión pulmonar. Este fenómeno conduce a hipoplasia pulmonar y a alteraciones en la vasculatura pulmonar, incrementando la resistencia vascular y comprometiendo la oxigenación en el periodo neonatal. La gravedad de esta condición refleja la importancia crítica del diafragma no solo como estructura anatómica, sino como regulador del desarrollo torácico.
El desarrollo del diafragma ilustra un ejemplo paradigmático de integración embriológica, donde múltiples tejidos, señales moleculares y fuerzas mecánicas convergen para formar una estructura funcional esencial. La comprensión detallada de estos procesos no solo tiene valor académico, sino que también proporciona bases fundamentales para el diagnóstico y manejo de anomalías congénitas.

Fuente y lecturas recomendadas:
- Sadler, T. W. (2023). Langman’s Medical Embryology (15th ed.). Wolters Kluwer.
- Moore, K. L., Persaud, T. V. N., & Torchia, M. G. (2020). The Developing Human: Clinically Oriented Embryology(11th ed.). Elsevier.
- Gilbert, S. F., & Barresi, M. J. F. (2020). Developmental Biology (12th ed.). Sinauer Associates.
- Greer, J. J. (2013). Current concepts on the pathogenesis and etiology of congenital diaphragmatic hernia. Respiratory Physiology & Neurobiology, 189(2), 232–240.
- Clugston, R. D., & Greer, J. J. (2007). Diaphragm development and congenital diaphragmatic hernia. Seminars in Pediatric Surgery, 16(2), 94–100.
- Paris, N. D., et al. (2015). Wt1 and β-catenin cooperatively regulate diaphragm development. Developmental Biology, 403(1), 56–68.
- Ackerman, K. G., et al. (2005). Fog2 is required for normal diaphragm and lung development in mice and humans. PLoS Genetics, 1(1), e10.
Síguenos en X: @el_homomedicus y @enarm_intensivo Síguenos en instagram: homomedicus y en Treads.net como: Homomedicus