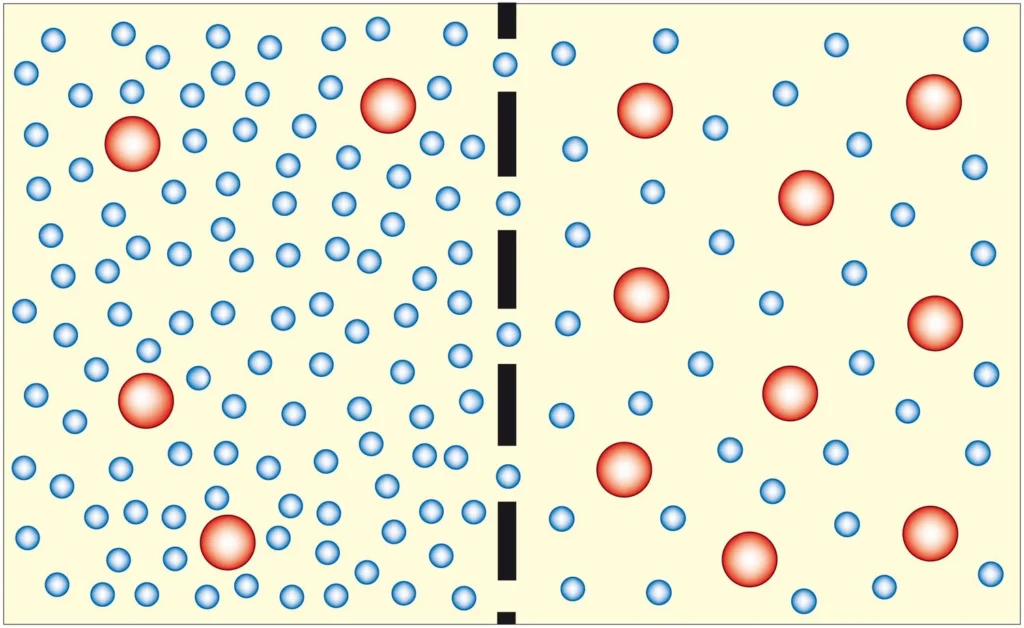
Los líquidos isoosmóticos, hiperosmóticos e hipoosmóticos constituyen categorías fisicoquímicas definidas por la cantidad total de partículas osmóticamente activas disueltas por unidad de volumen de solución, habitualmente expresadas como osmolaridad u osmolalidad, y su efecto biológico depende no solamente de dicha cantidad total, sino también de la capacidad de cada soluto para atravesar o no la membrana celular y, por lo tanto, modificar el volumen celular mediante flujo neto de agua a través de la bicapa lipídica y de canales especializados de agua como las acuaporinas. Este principio ha sido establecido de manera consistente en la fisiología celular moderna, donde se distingue estrictamente entre osmolaridad y tonicidad como conceptos no equivalentes en sistemas biológicos reales debido a la permeabilidad selectiva de las membranas celulares.
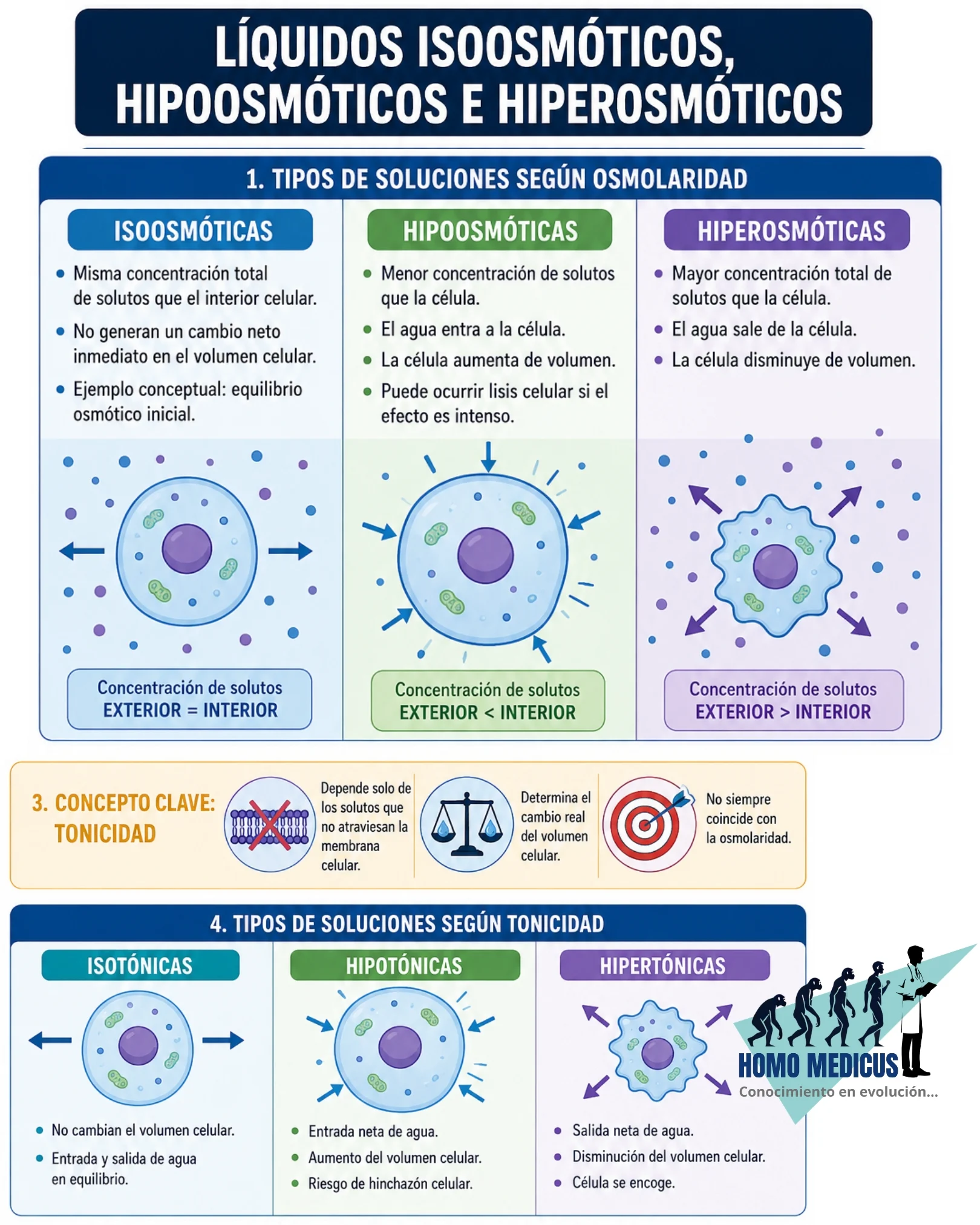
Un líquido isoosmótico es aquel cuya concentración total de partículas osmóticamente activas es aproximadamente equivalente a la del citosol celular, típicamente cercana a trescientos miliosmoles por litro en mamíferos. Sin embargo, la condición isoosmótica no implica necesariamente ausencia de flujo de agua, ya que el efecto sobre el volumen celular depende de si los solutos presentes son efectivos o no efectivos desde el punto de vista osmótico. La evidencia fisiológica muestra que soluciones isoosmóticas pueden no alterar el volumen celular de manera inmediata cuando están compuestas por solutos que no atraviesan fácilmente la membrana plasmática, lo que establece una situación de equilibrio inicial entre compartimientos intra y extracelulares.
En contraste, una solución hipoosmótica presenta una concentración total de solutos menor que la del interior celular, lo que genera un gradiente osmótico neto que favorece la entrada de agua hacia el interior de la célula, produciendo aumento del volumen celular y, en casos extremos, lisis celular. Este comportamiento ha sido descrito experimentalmente en eritrocitos expuestos a medios con baja osmolaridad, donde el incremento de volumen ocurre de manera rápida debido a la alta permeabilidad de la membrana al agua, fenómeno que se explica por la elevada conductividad hidráulica de la membrana celular mediada por proteínas canal acuaporinas.
Por otro lado, una solución hiperosmótica contiene una concentración total de solutos mayor que la del interior celular, lo que induce un flujo neto de agua desde el interior hacia el espacio extracelular, provocando disminución del volumen celular y, en muchos casos, crenación o encogimiento celular. Este fenómeno ha sido ampliamente documentado en estudios de regulación del volumen celular, donde se observa que las células activan mecanismos compensatorios como el ajuste regulador de volumen para recuperar parcialmente su tamaño mediante entrada de iones y osmolitos orgánicos compatibles.
No obstante, la categoría fisiológicamente más relevante no es únicamente la osmolaridad, sino la tonicidad, la cual describe el efecto efectivo de una solución sobre el volumen celular en función de los solutos que no atraviesan libremente la membrana plasmática. Una solución isotónica es aquella que mantiene el volumen celular estable porque los solutos presentes no generan gradientes osmóticos efectivos sostenidos a través de la membrana. Este concepto ha sido fundamental para comprender por qué soluciones con la misma osmolaridad pueden producir efectos celulares completamente distintos dependiendo de la permeabilidad de sus componentes.
Las soluciones hipertónicas son aquellas que contienen solutos no permeables en concentración mayor que el compartimiento intracelular, lo que produce salida de agua desde la célula hacia el exterior. Este principio es la base fisiológica del uso clínico de soluciones salinas hipertónicas para reducir edema celular en situaciones patológicas, ya que incrementan la osmolaridad extracelular efectiva y movilizan agua desde el compartimiento intracelular hacia el extracelular.
En contraste, las soluciones hipotónicas contienen menor concentración de solutos no permeables que el interior celular, generando entrada neta de agua y aumento del volumen celular. La importancia de esta distinción ha sido demostrada en estudios de homeostasis del volumen celular, donde se evidencia que la tonicidad depende exclusivamente de solutos efectivamente impermeables en el corto plazo, mientras que solutos permeables pueden igualar concentraciones sin generar fuerzas osmóticas sostenidas.
Un ejemplo fundamental que ilustra la diferencia entre osmolaridad y tonicidad es el comportamiento de la urea. La urea puede atravesar con relativa facilidad la membrana celular, por lo que una solución de urea puede ser isoosmótica con el plasma pero comportarse funcionalmente como hipotónica en el corto plazo, debido a su difusión hacia el interior celular y el consiguiente arrastre de agua. Este fenómeno ha sido descrito en estudios clásicos de fisiología celular, donde se demuestra que la permeabilidad diferencial de solutos convierte a la urea en un osmole inefectivo en términos de tonicidad, a pesar de contribuir a la osmolaridad total de la solución.
El comportamiento del agua en estos sistemas se explica por el principio termodinámico del potencial químico del agua, que determina su movimiento desde regiones de menor concentración efectiva de solutos hacia regiones de mayor concentración efectiva de solutos no permeables. La membrana celular actúa como barrera semipermeable que permite el paso de agua con gran facilidad, mientras restringe de forma selectiva el paso de múltiples solutos, lo que genera cambios volumétricos celulares dependientes del gradiente osmótico efectivo.
En condiciones fisiológicas, el volumen celular se mantiene estable mediante mecanismos de regulación del volumen que incluyen el transporte activo de iones como sodio y potasio, así como la acumulación o liberación de osmólitos orgánicos compatibles. Estos mecanismos permiten a la célula contrarrestar cambios osmóticos persistentes, manteniendo la homeostasis volumétrica incluso en entornos extracelulares variables.
Desde una perspectiva sistémica, el compartimiento extracelular está dominado por sodio como principal osmole efectivo, lo que hace que la regulación del sodio plasmático sea determinante en la osmolalidad efectiva del organismo. Alteraciones en la concentración de sodio se correlacionan directamente con cambios en la osmolaridad plasmática y, por ende, con desplazamientos de agua entre compartimientos intra y extracelulares, lo cual ha sido ampliamente demostrado en estudios clínicos de trastornos del equilibrio hídrico.

Fuente y lecturas recomendadas:
- Boron, W. F., & Boulpaep, E. L. (2017). Medical Physiology (3rd ed.). Elsevier.
- Alberts, B., Johnson, A., Lewis, J., Morgan, D., Raff, M., Roberts, K., & Walter, P. (2015). Molecular Biology of the Cell(6th ed.). Garland Science.
- Adrogué, H. J., & Madias, N. E. (2000). Hyponatremia. The New England Journal of Medicine, 342(21), 1581–1589.
- Verbalis, J. G., Goldsmith, S. R., Greenberg, A., Schrier, R. W., & Sterns, R. H. (2013). Diagnosis, evaluation, and treatment of hyponatremia: Expert panel recommendations. The American Journal of Medicine, 126(10 Suppl 1), S1–S42.
- Strange, K. (2004). Cellular volume homeostasis. Physiological Reviews, 84(3), 1067–1106.