Durante la vida embrionaria, fetal y adulta se producen diferentes hemoglobinas
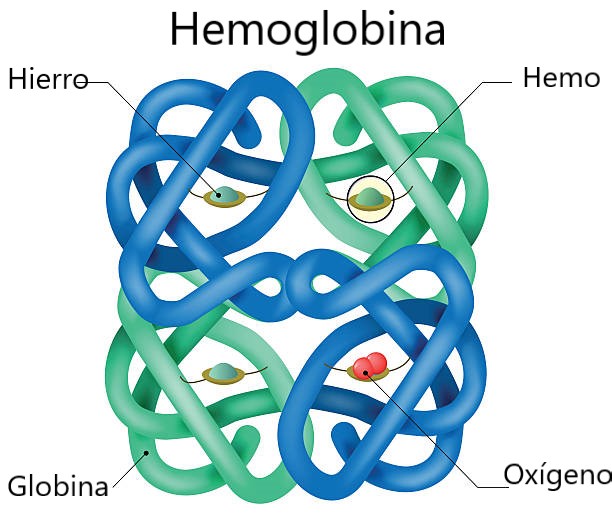
Cada una de las diferentes hemoglobinas del humano consta de un tetrámero de cadenas polipeptídicas de globina: un par de cadenas similares a α de 141 aminoácidos de longitud y un par de cadenas similares a ß de 146 aminoácidos.
La principal hemoglobina del adulto, HbA, tiene la estructura α2ß2.
La principal hemoglobina del adulto, HbA, tiene la estructura a2ß2. La hemoglobina fetal HbF (a2γ2) predomina durante la mayor parte del embarazo, y la HbA2 (a2δ2) es una hemoglobina menor del adulto.
Cada cadena de globina envuelve entre sus pliegues un solo anillo hemo, que consiste en un anillo de protoporfirina IX que forma un complejo con un único átomo de hierro en estado ferroso (Fe+).
Cada fracción hemo puede unir una única molécula de oxígeno, de modo que cada molécula de hemoglobina puede transportar hasta cuatro moléculas de oxígeno.
Las secuencias de aminoácidos de las diferentes globinas son muy semejantes entre sí. Cada una tiene una estructura secundaria muy helicoidal.
Sus estructuras terciarias globulares motivan que las superficies externas tengan abundantes aminoácidos polares (hidrófilos) que facilitan la solubilidad y que el interior esté revestido de grupos no polares, que forman una “bolsa” hidrófoba en la que se inserta el hemo.
La estructura tetramérica cuaternaria de la hemoglobina contiene dos dímeros αß. Múltiples interacciones estrechas mantienen juntas las cadenas α y ß. El tetrámero completo se conserva unido por interfases entre la cadena similar a α de un dímero y la cadena distinta de
α, del otro dímero.
El tetrámero de hemoglobina es muy soluble, pero las cadenas individuales de globina son insolubles.
Las propiedades principales de solubilidad y la unión reversible del oxígeno dependen sobre todo de los aminoácidos hidrófilos de la superficie, de los aminoácidos hidrófobos que revisten la bolsa de hemo, de una histidina clave en la hélice F y de los aminoácidos que forman las superficies de contacto α1ß1 y α1ß2.

Fuente: Harrison: Principios de Medicina Interna, 20ª Edición. McGraw-Hill Interamericana. 2020
Síguenos en X: @el_homomedicus y @enarm_intensivo Síguenos en instagram: homomedicus y en Treads.net como: Homomedicus