Las bacterias, tanto Gram positivas como Gram negativas, no son entidades simples delimitadas únicamente por una pared celular y una membrana. Muchas especies poseen estructuras externas adicionales que rodean o se proyectan desde la superficie celular y que desempeñan funciones cruciales para la supervivencia, la adaptación al ambiente, la colonización de nichos específicos y la patogenicidad. Estas estructuras externas no suelen ser indispensables para el crecimiento bacteriano en condiciones ideales de laboratorio, pero adquieren una importancia decisiva en ambientes naturales y, especialmente, durante la interacción con un hospedador. Entre las más relevantes se encuentran las cápsulas y capas mucosas, los biofilms, los flagelos y las fimbrias o pili.
Cápsula y glicocálix
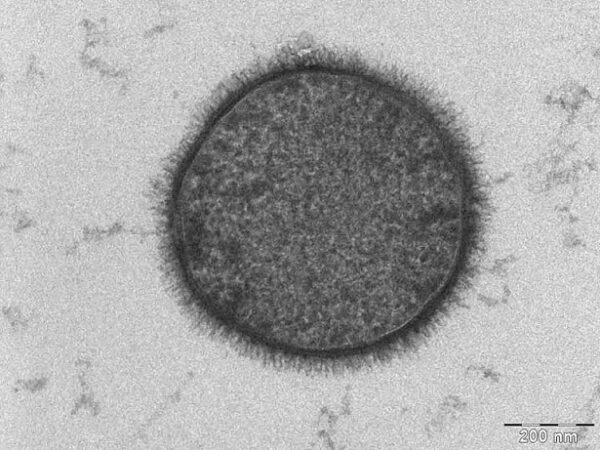
Muchas bacterias están rodeadas por una capa externa laxa y organizada, compuesta principalmente por polisacáridos, conocida como cápsula. En algunos casos, cuando esta capa es menos definida y más difusa, se la denomina capa mucosa o glicocálix. La cápsula se encuentra firmemente asociada a la superficie bacteriana, aunque su estructura es hidratada y poco densa, lo que dificulta su visualización directa mediante microscopía óptica convencional. Sin embargo, su presencia puede inferirse utilizando técnicas de tinción negativa, como la exclusión de partículas de tinta china, que dejan un halo claro alrededor de la célula.
Aunque la mayoría de las cápsulas bacterianas están formadas por polisacáridos, existen excepciones notables, como Bacillus anthracis, cuya cápsula está compuesta por un polímero de naturaleza polipeptídica. Esta diversidad química refleja adaptaciones evolutivas específicas y tiene implicaciones directas en la antigenicidad y en el reconocimiento inmunitario.
La cápsula no es esencial para el crecimiento bacteriano en medios ricos, pero constituye un factor crítico para la supervivencia dentro del hospedador. Su baja antigenicidad dificulta el reconocimiento por el sistema inmunitario adaptativo, mientras que su efecto antífagocítico impide la ingestión eficiente de la bacteria por macrófagos y neutrófilos. Como consecuencia, las bacterias encapsuladas presentan una mayor capacidad para persistir y diseminarse en los tejidos del hospedador.
En numerosos patógenos, la cápsula representa un determinante mayor de virulencia. Un ejemplo clásico es Streptococcus pneumoniae, cuya capacidad para causar enfermedad invasiva depende en gran medida de la presencia de una cápsula intacta. Cepas que pierden la cápsula durante el crecimiento en condiciones de laboratorio, donde la presión selectiva del sistema inmunitario está ausente, muestran una marcada reducción de su virulencia.
Además de su función inmunológica, la cápsula actúa como una barrera física frente a sustancias tóxicas, en particular moléculas hidrofóbicas como detergentes y ciertos agentes antimicrobianos. También favorece la adhesión de la bacteria a superficies bióticas y abióticas, facilitando la colonización de tejidos del hospedador o la asociación con otras bacterias.
Biofilms
En determinadas condiciones ambientales y cuando la densidad bacteriana alcanza un umbral crítico, algunas especies producen grandes cantidades de polisacáridos extracelulares que dan lugar a estructuras complejas denominadas biofilms. Este proceso, regulado por sistemas de comunicación celular dependientes de la densidad poblacional, permite a las bacterias organizarse en comunidades multicelulares adheridas a superficies.
El biofilm consiste en una matriz tridimensional rica en polisacáridos, proteínas y ácidos nucleicos extracelulares, dentro de la cual las bacterias quedan embebidas y protegidas. Esta matriz crea un microambiente que difiere significativamente del medio externo, tanto en disponibilidad de nutrientes como en condiciones físico-químicas.
Los biofilms confieren a las bacterias una protección notable frente a antibióticos y frente a los mecanismos de defensa del hospedador. La matriz extracelular dificulta la penetración de agentes antimicrobianos y limita el acceso de células inmunitarias, lo que favorece infecciones persistentes y crónicas. Ejemplos bien conocidos incluyen la producción de biofilms por Pseudomonas aeruginosa y Staphylococcus aureus en dispositivos médicos o tejidos dañados.
En Streptococcus mutans, la producción de biofilms ricos en dextrano y levano permite la adhesión firme al esmalte dental y conduce a la formación de la placa dentaria, un proceso clave en el desarrollo de la caries. Este ejemplo ilustra cómo los biofilms no solo protegen a la bacteria, sino que también modifican de manera significativa el entorno del hospedador.
Flagelos
Los flagelos son apéndices largos y filamentosos con apariencia de cuerdas helicoidales, compuestos por subunidades proteicas repetitivas de flagelina. Estas estructuras se anclan a la envoltura bacteriana mediante un complejo sistema formado por un cuerpo basal y un gancho, que conecta el filamento externo con un motor proteico integrado en las membranas celulares. El movimiento del flagelo es impulsado por el potencial de membrana, que suministra la energía necesaria para la rotación del motor.
La disposición de los flagelos varía entre especies bacterianas. Algunas poseen un único flagelo, mientras que otras presentan múltiples flagelos distribuidos en diferentes regiones de la superficie celular. Esta variabilidad estructural se asocia con diferentes patrones de motilidad.
La función principal de los flagelos es conferir motilidad, permitiendo a las bacterias desplazarse activamente en medios líquidos. Este movimiento no es aleatorio, sino que está finamente regulado por sistemas de quimiotaxis que permiten a la célula orientarse hacia fuentes de nutrientes y alejarse de sustancias tóxicas. El desplazamiento bacteriano se caracteriza por fases de nado rectilíneo alternadas con cambios bruscos de dirección, conocidos como tumbos. A medida que aumenta la concentración de un quimioatrayente, la duración de los periodos de nado rectilíneo se prolonga, optimizando la aproximación al estímulo favorable.
Además de su función mecánica, los flagelos poseen relevancia inmunológica. La flagelina actúa como un antígeno específico de cepa y como un ligando reconocido por receptores de reconocimiento de patrones del sistema inmunitario innato, lo que desencadena respuestas defensivas del hospedador.
Fimbrias y pilli
Las fimbrias, también denominadas pili, son estructuras filamentosas cortas y delgadas que emergen de la superficie bacteriana. Están compuestas por subunidades proteicas llamadas pilinas y se distinguen de los flagelos por su menor diámetro y por carecer de la estructura helicoidal característica. Generalmente, una bacteria puede presentar cientos de fimbrias distribuidas de manera uniforme sobre toda su superficie, y algunas de ellas pueden alcanzar longitudes muy superiores al tamaño de la célula.
La función principal de las fimbrias es la adhesión. Actúan como factores de adherencia que permiten a las bacterias fijarse a otras bacterias o a superficies del hospedador. En muchos casos, los extremos de las fimbrias contienen proteínas con afinidad específica por determinados azúcares presentes en las células humanas, lo que confiere un alto grado de especificidad tisular. Esta capacidad adhesiva es un paso esencial en la colonización y el establecimiento de infecciones.
Las fimbrias constituyen factores de virulencia clave en numerosas infecciones, como las infecciones del tracto urinario causadas por Escherichia coli o las infecciones de transmisión sexual producidas por Neisseria gonorrhoeae. Al facilitar la adherencia inicial, estas estructuras permiten a la bacteria resistir la eliminación mecánica y establecerse en el hospedador.
Un tipo especializado de pili, conocidos como pili sexuales, desempeña una función distinta. Estos pili median el contacto entre bacterias y forman un conducto a través del cual se transfieren grandes fragmentos de material genético durante el proceso de conjugación. Los pili sexuales están codificados por plásmidos específicos y representan un mecanismo fundamental de transferencia horizontal de genes, contribuyendo a la diseminación de factores de virulencia y de resistencia a antibióticos entre poblaciones bacterianas.

Fuente y lecturas recomendadas:
- Madigan, M. T., Martinko, J. M., Bender, K. S., Buckley, D. H., & Stahl, D. A. (2018). Brock biology of microorganisms (15th ed.). Pearson.
- Murray, P. R., Rosenthal, K. S., & Pfaller, M. A. (2025). Medical microbiology (10th ed.). Elsevier.
- Carroll, K. C., & Pfaller, M. A. (2023). Manual of clinical microbiology (13th ed.). American Society for Microbiology Press.
- Riedel, S., Hobden, J. A., Miller, S., Morse, S. A., Mietzner, T. A., Detrick, B., Mitchell, T. G., Sakanari, J. A., Hotez, P., & Mejía, R. (2020). Microbiología médica (28ª ed.). McGraw-Hill Interamericana Editores.