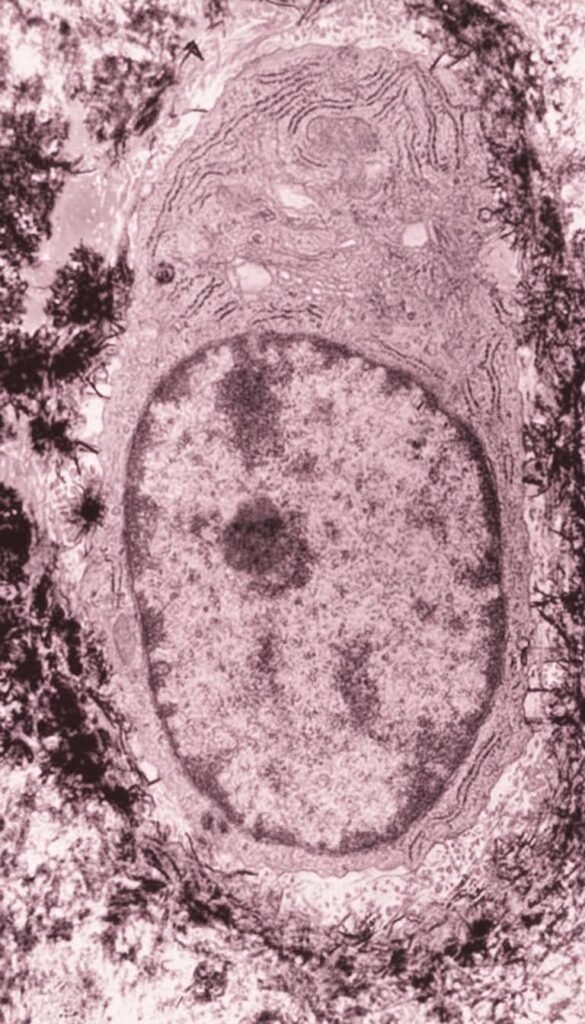
El osteocito representa la etapa terminal de diferenciación de la línea osteoblástica, un proceso altamente regulado dentro del tejido óseo. Desde el punto de vista de la biología celular, esta transformación no consiste únicamente en un cambio de nombre, sino en una profunda reprogramación estructural y funcional. Cuando un osteoblasto sintetiza activamente matriz extracelular —principalmente colágeno tipo uno y proteínas no colágenas—, llega un punto en el que queda completamente rodeado por el material que él mismo ha secretado. Este fenómeno genera un aislamiento físico progresivo que impide la continuación de su actividad secretora típica.
La transición hacia osteocito ocurre porque el microambiente tridimensional en el que queda atrapado impone nuevas condiciones de difusión de nutrientes, oxígeno y señales moleculares. En respuesta a ello, la célula reduce su volumen, reorganiza sus orgánulos y modifica su expresión génica. La disminución del retículo endoplásmico rugoso y del aparato de Golgi refleja una menor actividad secretora masiva, mientras que el desarrollo de prolongaciones citoplasmáticas permite compensar el aislamiento físico mediante la creación de una red de comunicación intercelular.
Adaptaciones morfofuncionales durante la transformación
Durante aproximadamente tres días, el osteoblasto experimenta cambios cuantitativos y cualitativos que responden a exigencias biofísicas y metabólicas. La producción de una cantidad de matriz que supera varias veces su propio volumen responde a la necesidad de consolidar una estructura extracelular rígida capaz de soportar cargas mecánicas. Sin embargo, una vez rodeado por esta matriz, mantener un gran tamaño celular sería ineficiente debido a las limitaciones en el intercambio de sustancias.
Por esta razón, la reducción de hasta un 70% del volumen celular representa una estrategia adaptativa para disminuir las demandas metabólicas en un entorno relativamente confinado. Paralelamente, la extensión de múltiples prolongaciones citoplasmáticas —alrededor de cincuenta por célula— permite maximizar la superficie de contacto y establecer conexiones con otras células. Estas prolongaciones no son estructuras arbitrarias, sino elementos esenciales para la supervivencia celular y la integración funcional del tejido óseo.
Organización en lagunas y canalículos
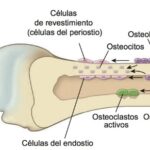
Una vez mineralizada la matriz ósea, el osteocito queda alojado en una cavidad denominada laguna. Aunque esta disposición podría sugerir aislamiento, en realidad el tejido óseo desarrolla un sistema altamente organizado de canalículos que albergan las prolongaciones citoplasmáticas. Este sistema constituye una red interconectada que permite la comunicación directa entre osteocitos mediante uniones tipo nexo.
Desde una perspectiva fisiológica, esta red canalicular es indispensable porque el tejido óseo es relativamente poco vascularizado en comparación con otros tejidos. Por tanto, la difusión de nutrientes y señales depende en gran medida de esta arquitectura microscópica. Además, las prolongaciones permiten la transmisión de estímulos mecánicos en forma de cambios en el flujo de líquido intersticial, lo que convierte al osteocito en un sensor mecánico altamente especializado.
El osteocito no solo mantiene comunicación local con células vecinas, sino que también participa en redes de señalización más amplias. A través de la secreción de moléculas señalizadoras, puede influir indirectamente en osteoblastos, células del endotelio vascular y otros componentes del microambiente medular. Esta capacidad responde a la necesidad de coordinar la actividad de formación y resorción ósea, procesos que deben mantenerse en equilibrio dinámico.
Desde el punto de vista molecular, el osteocito expresa proteínas que regulan la actividad de otras células óseas, como factores que inhiben o estimulan la formación de hueso. Esto explica por qué, a pesar de estar físicamente atrapado en la matriz mineralizada, posee un papel central en la regulación del metabolismo óseo a nivel local y sistémico.
Actividad metabólica y mecanotransducción
Contrario a concepciones antiguas que lo consideraban una célula pasiva, el osteocito es altamente activo desde el punto de vista metabólico. Su papel en la mecanotransducción se basa en su capacidad para detectar deformaciones mecánicas del hueso y traducirlas en señales bioquímicas. Este proceso ocurre principalmente mediante cambios en el flujo del líquido dentro de los canalículos, lo que genera fuerzas de cizallamiento sobre la membrana celular.
Cuando los estímulos mecánicos son adecuados, el osteocito promueve la formación ósea al estimular a los osteoblastos. En cambio, la ausencia de carga mecánica —como sucede en la inmovilidad prolongada o en condiciones de microgravedad— reduce la señalización anabólica y favorece la resorción ósea. Esta relación explica por qué el hueso es un tejido altamente dinámico que se adapta continuamente a las demandas funcionales del organismo.
Los osteocitos poseen la capacidad de modificar activamente su entorno inmediato, lo que implica cambios en el tamaño de la laguna y en el diámetro de los canalículos. Este fenómeno refleja una forma de remodelado microscópico que permite ajustar la composición mineral y la disponibilidad de iones en función de las necesidades del organismo.
Desde un enfoque fisiológico, esta capacidad contribuye a la homeostasis del calcio y del fosfato, elementos esenciales para múltiples procesos biológicos. La existencia de diferentes estados funcionales —latente, formativo y resortivo— evidencia que el osteocito no es una entidad estática, sino una célula capaz de alternar entre distintos perfiles metabólicos según las condiciones del entorno.
Estados funcionales y especialización
Los distintos estados del osteocito responden a variaciones en su actividad biosintética y degradativa. En su forma latente, la célula presenta una actividad mínima, lo que se refleja en la escasez de orgánulos asociados con la síntesis proteica. Este estado es compatible con un entorno estable donde no se requiere remodelación activa.
En contraste, el osteocito formativo reactiva parcialmente la maquinaria biosintética, adoptando características similares a las del osteoblasto. Esto ocurre cuando es necesario depositar nueva matriz en su entorno inmediato. Por otro lado, el osteocito resortivo presenta abundantes lisosomas y estructuras asociadas con la degradación, lo que le permite participar en la liberación de minerales desde la matriz ósea.
Longevidad celular y muerte
Una de las características más notables del osteocito es su longevidad, que puede extenderse durante décadas. Esta larga vida útil se explica por su bajo nivel de proliferación y por su adaptación a un entorno relativamente estable. Sin embargo, con el tiempo, factores como el estrés oxidativo, la acumulación de daño molecular y la disminución de la capacidad de reparación conducen a su muerte.
La muerte del osteocito puede ocurrir mediante apoptosis, necrosis o senescencia, y tiene consecuencias importantes para la integridad del tejido óseo. Cuando las lagunas quedan vacías, pueden rellenarse con material mineral, lo que altera la estructura de la red canalicular y reduce la capacidad de comunicación celular.
El aumento progresivo de osteocitos muertos con la edad refleja un deterioro en la capacidad del tejido óseo para mantener su homeostasis. Desde una perspectiva biológica, esto implica una disminución en la detección de estímulos mecánicos y en la regulación del remodelado óseo. Como resultado, el hueso se vuelve más frágil y susceptible a fracturas.
Este fenómeno no es simplemente una consecuencia del paso del tiempo, sino el resultado de una interacción compleja entre factores mecánicos, metabólicos y moleculares. La pérdida de osteocitos funcionales compromete la integridad de la red de comunicación, lo que reduce la eficiencia de la respuesta adaptativa del hueso frente a las demandas del organismo.

Fuente y lecturas recomendadas:
- Ross, M. H. & Pawlina, W. (2020). Histología: texto y atlas: correlación con biología molecular y celular (8.ª ed.). Wolters Kluwer.
- Gartner, L. P. (2020). Textbook of Histology (5th ed.). Elsevier.
- Karp, G., Iwasa, J., & Marshall, W. (2019). Biología celular y molecular: conceptos y experimentos (8.ª ed.). McGraw-Hill Interamericana.