La oncocercosis, también conocida como ceguera de los ríos, es una enfermedad parasitaria causada por el nematodo Onchocerca volvulus. Este parásito infecta a millones de personas en todo el mundo, y se estima que aproximadamente treinta y siete millones de individuos están afectados, de los cuales entre tres y cuatro millones presentan manifestaciones cutáneas, alrededor de quinientas mil personas sufren un deterioro visual severo, y trescientas mil han quedado completamente ciegas como resultado de la infección. Más del noventa y nueve por ciento de los casos se concentran en el África subsahariana, especialmente en la sabana del África occidental, siendo Nigeria y la República Democrática del Congo los países con la mayor carga de la enfermedad, donde se registra casi la mitad de los casos a nivel mundial. En ciertas comunidades africanas consideradas hiperendémicas, la prevalencia de infección puede acercarse al cien por ciento, y más del diez por ciento de la población puede sufrir ceguera. Además, la oncocercosis también se encuentra en regiones del suroeste de la Península Arábiga y en países de América Latina, incluyendo zonas del sur de México, Guatemala, Venezuela, Colombia, Ecuador y el noroeste de Brasil.
La transmisión de la oncocercosis ocurre a través de la picadura de moscas negras del género Simulium. Estas moscas se reproducen en aguas rápidas y limpias, como arroyos y ríos de corriente rápida, y tienen hábitos diurnos de alimentación. Cuando una mosca negra infectada pica a una persona, deposita larvas de Onchocerca volvulus en la piel. Estas larvas se desarrollan y maduran durante un período de seis a doce meses hasta convertirse en adultos. Los gusanos adultos se alojan en tejidos subcutáneos, formando nódulos en el tejido conectivo o muscular, donde pueden vivir durante una década o más. Desde estos nódulos, las hembras liberan microfilarias, que son larvas microscópicas que migran a través de la piel y también alcanzan los tejidos oculares.
La patología de la enfermedad no se debe únicamente a la presencia de los parásitos adultos o sus larvas, sino también a la respuesta inflamatoria del huésped frente a los mismos, la cual se ve intensificada por la presencia de bacterias intracelulares del género Wolbachia que habitan simbióticamente dentro de los gusanos. Estas bacterias desencadenan una reacción inmunitaria que contribuye al daño tisular, especialmente en la piel y en los ojos, lo que puede derivar en lesiones cutáneas crónicas y en la pérdida progresiva de la visión que caracteriza la ceguera de los ríos. En conjunto, la interacción compleja entre el parásito, las bacterias simbióticas y la respuesta inmunológica del paciente determina la gravedad y la progresión de esta enfermedad debilitante.
Manifestaciones clínicas
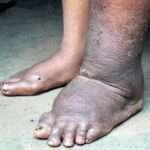
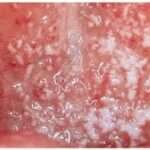
Después de un período de incubación que puede extenderse entre uno y tres años, la oncocercosis suele manifestarse inicialmente con una erupción cutánea caracterizada por enrojecimiento, presencia de pequeñas elevaciones o pápulas y un intenso prurito. Esta reacción inflamatoria de la piel tiende a ser persistente y puede evolucionar hacia cambios crónicos, como el engrosamiento de la piel y la pérdida de pigmentación, lo que genera áreas blanquecinas que alteran la apariencia cutánea. El prurito asociado con la infección suele ser intenso, llegando en muchos casos a ser refractario a los tratamientos convencionales, causando un malestar significativo y contribuyendo a una considerable pérdida en la calidad de vida. De hecho, la carga de años vividos con discapacidad a causa de las alteraciones cutáneas producidas por la oncocercosis es mayor que la asociada a la ceguera provocada por la enfermedad.
En muchos pacientes se observan nódulos subcutáneos firmes, indoloros y móviles, con un tamaño que varía entre medio centímetro y tres centímetros, donde residen los gusanos adultos. La localización de estos nódulos varía geográficamente debido a las diferencias en el comportamiento del vector transmisor: en África, son más frecuentes en la parte inferior del cuerpo, mientras que en América Latina tienden a encontrarse en la cabeza y la parte superior del cuerpo. Además, es común la presencia de linfadenopatía en las regiones inguinal y femoral, que en algunos casos puede evolucionar hacia una condición conocida como “ingle colgante,” en la que los ganglios linfáticos se encuentran suspendidos en una piel atrófica, debilitada y flácida, lo que representa una deformidad significativa.
Los pacientes afectados por oncocercosis también pueden experimentar síntomas sistémicos, tales como pérdida de peso y dolor en las articulaciones y músculos, reflejo de una respuesta inflamatoria más generalizada. No obstante, las manifestaciones más graves se relacionan con la migración de las microfilarias a través de los tejidos oculares. En estos casos, se pueden identificar lesiones características, como la queratitis punteada y la opacificación corneal, que progresan hacia una queratitis esclerosante y, en última instancia, la ceguera irreversible. Otros daños oculares incluyen inflamación del iris y del cuerpo ciliar (iridociclitis), glaucoma, inflamación de la coroides (coroiditis) y atrofia del nervio óptico, todos los cuales contribuyen al deterioro visual. La probabilidad de desarrollar ceguera tras la infección no es uniforme y depende en gran medida de la región geográfica, siendo mucho mayor en las áreas de sabana del África occidental, donde la carga y agresividad de la enfermedad son particularmente elevadas.
Exámenes diagnósticos
El diagnóstico de la oncocercosis se fundamenta en la identificación directa del parásito, en cualquiera de sus formas, mediante diversos métodos clínicos y de laboratorio. La técnica más común y específica consiste en la obtención de pequeñas biopsias superficiales de piel, conocidas como escarificaciones cutáneas. Estas muestras, habitualmente tomadas de la cresta ilíaca en regiones africanas o de la escápula en poblaciones americanas, se sumergen en solución salina fisiológica durante un período de entre dos y cuatro horas, o incluso más tiempo si es necesario. Durante este intervalo, las microfilarias, si están presentes en el tejido, emergen activamente de la muestra hacia el líquido. Posteriormente, se examina la solución al microscopio para detectar la presencia de estas larvas. Este procedimiento, mínimamente invasivo, no requiere biopsias profundas mediante sacabocados, ya que las microfilarias suelen encontrarse en las capas más superficiales de la dermis.
En casos en que los resultados de la escarificación cutánea sean negativos, pero la sospecha clínica de oncocercosis persista, se recomienda repetir el procedimiento en lugar de recurrir a métodos más invasivos. La visualización directa de las microfilarias también puede lograrse mediante examen oftalmológico con lámpara de hendidura, lo que permite observarlas en la córnea o en la cámara anterior del ojo, especialmente en casos con compromiso ocular evidente.
Otra vía diagnóstica, aunque menos frecuente, consiste en la obtención de material de nódulos subcutáneos, ya sea por biopsia o aspirado con aguja fina, con el fin de identificar gusanos adultos. En raras ocasiones, se han descrito microfilarias en muestras de orina, aunque este hallazgo no constituye un método diagnóstico de rutina.
El ultrasonido también puede ser útil como herramienta complementaria. En manos expertas, permite detectar hallazgos característicos de la presencia de gusanos adultos dentro de los nódulos, especialmente cuando estos se encuentran en localizaciones profundas o difíciles de explorar clínicamente.
Cuando el diagnóstico sigue siendo incierto a pesar de los métodos convencionales, puede recurrirse al denominado test de Mazzotti. Este consiste en la administración tópica o por vía oral de una dosis de cincuenta miligramos del antiparasitario dietilcarbamacina. En individuos infectados, este medicamento provoca una exacerbación inmediata del prurito y de la erupción cutánea debido a la muerte masiva de microfilarias, lo que constituye una reacción altamente sugestiva de oncocercosis. Sin embargo, este procedimiento conlleva riesgos considerables, ya que puede inducir reacciones inflamatorias severas, especialmente oculares, en pacientes con infecciones de alta carga parasitaria.
Desde el punto de vista hematológico, es frecuente observar eosinofilia, aunque este hallazgo no es constante y no tiene valor diagnóstico definitivo. Actualmente, se encuentran en desarrollo técnicas serológicas para la detección de antígenos y anticuerpos específicos contra Onchocerca volvulus, que podrían en el futuro ofrecer alternativas menos invasivas y más sensibles para el diagnóstico de esta enfermedad. No obstante, por el momento, el diagnóstico sigue dependiendo principalmente de la observación directa del parásito en tejidos oculares, dérmicos o nódulos subcutáneos.
Tratamiento
El tratamiento de elección para la oncocercosis es la ivermectina, un antiparasitario eficaz que actúa eliminando las microfilarias, es decir, las formas larvales del parásito Onchocerca volvulus. Sin embargo, este fármaco no posee actividad directa contra los gusanos adultos, los cuales pueden sobrevivir en el organismo humano durante más de una década. Por esta razón, el control efectivo de la enfermedad no puede lograrse con una única administración, sino que requiere un régimen de tratamiento repetido a lo largo del tiempo.
La ivermectina se administra generalmente en una única dosis oral de ciento cincuenta microgramos por kilogramo de peso corporal. Aunque no existe aún un esquema universalmente estandarizado para las dosis subsecuentes, uno de los regímenes comúnmente utilizados consiste en administrar el medicamento cada tres meses durante un año, seguido de aplicaciones adicionales cada seis a doce meses, durante un período aproximado de quince años, que corresponde a la vida media estimada del parásito adulto. Este enfoque permite mantener reducida la carga de microfilarias en la piel y en los tejidos oculares, disminuyendo así la transmisión y el riesgo de nuevas lesiones. No obstante, aún no se ha determinado con certeza si la ivermectina puede frenar de manera significativa la progresión del daño ocular irreversible.
En general, los efectos adversos asociados con la ivermectina son leves y transitorios, e incluyen fiebre, prurito, urticaria, dolor muscular, edema, hipotensión y dolor ganglionar. Estas reacciones no son atribuibles a toxicidad directa del fármaco, sino a la respuesta inmunológica provocada por la muerte masiva de las microfilarias. En pacientes coinfectados con Loa loa, un parásito filarial distinto, el uso de ivermectina puede desencadenar reacciones graves, incluida la encefalopatía, por lo cual su administración debe realizarse con precaución en regiones endémicas de loiasis.
En busca de un tratamiento más efectivo y duradero, se han explorado terapias combinadas, como la administración conjunta de ivermectina con dietilcarbamacina y albendazol. Este enfoque ha mostrado mayor eficacia en la eliminación prolongada del parásito, similar a lo observado en el tratamiento de la filariasis linfática. Además, la moxidectina, un agente antiparasitario más reciente, ha sido aprobada para el tratamiento de la oncocercosis. Este fármaco se tolera bien y ha demostrado ser superior a la ivermectina en la supresión de microfilarias en la piel, lo que lo convierte en una opción terapéutica valiosa para el control y tratamiento de la enfermedad.
Por otro lado, se ha identificado que la doxiciclina, un antibiótico de amplio espectro, actúa de forma indirecta sobre Onchocerca volvulus al eliminar a las bacterias intracelulares del género Wolbachia, que viven simbióticamente dentro del parásito. Estas bacterias son esenciales para la reproducción y la supervivencia de los gusanos adultos. Un ciclo terapéutico de doxiciclina, consistente en la administración oral de cien miligramos diarios durante cuatro a seis semanas, elimina estas bacterias, lo que interrumpe la embriogénesis del parásito y puede esterilizar a los gusanos adultos por al menos dieciocho meses. Dado su efecto sostenido y su perfil de seguridad, la doxiciclina se postula como una prometedora terapia de primera línea, particularmente por su actividad sobre los adultos y su bajo riesgo de provocar reacciones inflamatorias agudas, debido a su acción lenta y progresiva.
En cuanto a la prevención, una medida clave es evitar la exposición a las moscas negras del género Simulium, responsables de la transmisión. Estas se reproducen en ríos de corriente rápida y pican durante el día, por lo que el uso de ropa protectora y repelentes constituye una medida básica de protección individual. A nivel colectivo, se han desplegado amplios programas para el control de vectores en África, mediante intervenciones ambientales y campañas de salud pública. Además, la distribución masiva de ivermectina a intervalos programados en comunidades endémicas ha reducido de forma significativa la prevalencia de manifestaciones cutáneas y oculares graves. Estas estrategias integradas, centradas tanto en el tratamiento como en la prevención, han demostrado ser efectivas y ofrecen esperanza en el control a largo plazo de esta enfermedad devastadora.

Fuente y lecturas recomendadas:
- Goldman, L., & Schafer, A. I. (Eds.). (2020). Goldman-Cecil Medicine (26th ed.). Elsevier.
- Loscalzo, J., Fauci, A. S., Kasper, D. L., Hauser, S. L., Longo, D. L., & Jameson, J. L. (Eds.). (2022). Harrison. Principios de medicina interna (21.ª ed.). McGraw-Hill Education.
- Papadakis, M. A., McPhee, S. J., Rabow, M. W., & McQuaid, K. R. (Eds.). (2024). Diagnóstico clínico y tratamiento 2025. McGraw Hill.
- Rozman, C., & Cardellach López, F. (Eds.). (2024). Medicina interna (20.ª ed.). Elsevier España.
- Opoku NO et al. A randomized, open-label study of the tolerability and efficacy of one or three daily doses of ivermectin plus diethylcarbamazine and albendazole (IDA) versus one dose of ivermectin plus albendazole (IA) for treatment of onchocerciasis. PLoS Negl Trop Dis. 2023;17:e0011365. [PMID: 37205721]