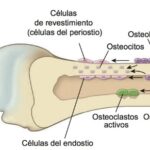
Los osteoclastos constituyen un linaje celular singular dentro del tejido óseo debido a su origen, morfología y función. A diferencia de otras células óseas como los osteoblastos u osteocitos, los osteoclastos no derivan de células mesenquimáticas, sino de precursores hematopoyéticos. En términos biológicos, esto implica que su estirpe está estrechamente vinculada a la del sistema mononuclear fagocítico. Específicamente, surgen a partir de células progenitoras de granulocitos y monocitos, las cuales poseen la capacidad de diferenciarse en macrófagos o células relacionadas con funciones de defensa y remodelación tisular.
Este origen explica por qué los osteoclastos comparten múltiples características con los macrófagos, como la capacidad fagocítica, la abundancia de lisosomas y su competencia en la degradación de matrices complejas. Sin embargo, lo que los distingue es su especialización extrema hacia la resorción de tejido mineralizado. La formación de un osteoclasto implica la fusión de múltiples precursores mononucleares, dando lugar a una célula multinucleada de gran tamaño, lo que incrementa su capacidad metabólica y funcional. Esta multinucleación no es un rasgo meramente estructural, sino una adaptación que permite coordinar de manera eficiente los procesos intensivos de secreción, transporte vesicular y digestión extracelular.
La diferenciación de los osteoclastos no ocurre de manera autónoma, sino que depende críticamente del microambiente de la médula ósea. Las células del estroma medular desempeñan un papel central al secretar moléculas señalizadoras que regulan tanto la proliferación como la diferenciación de los precursores hematopoyéticos hacia el linaje osteoclástico. Este proceso es un ejemplo claro de regulación paracrina, donde la proximidad celular permite una comunicación molecular altamente específica.
Las citocinas liberadas en este contexto actúan como moduladores del destino celular, induciendo la expresión de genes necesarios para la fusión celular, la adquisición de polaridad funcional y la activación de mecanismos de resorción. Este control asegura que la formación de osteoclastos esté finamente ajustada a las necesidades del tejido óseo, evitando tanto la resorción excesiva como la insuficiente. Desde una perspectiva fisiológica, este equilibrio es esencial para mantener la homeostasis del esqueleto, ya que el hueso es un tejido dinámico en constante remodelación.
Activación funcional y establecimiento de la resorción ósea
Una vez formado, el osteoclasto no es inmediatamente activo. Requiere un proceso de activación que implica cambios estructurales y bioquímicos que le permiten adherirse firmemente a la superficie ósea y comenzar la resorción. Esta activación conlleva la reorganización del citoesqueleto, la polarización de la célula y la especialización de dominios de membrana.
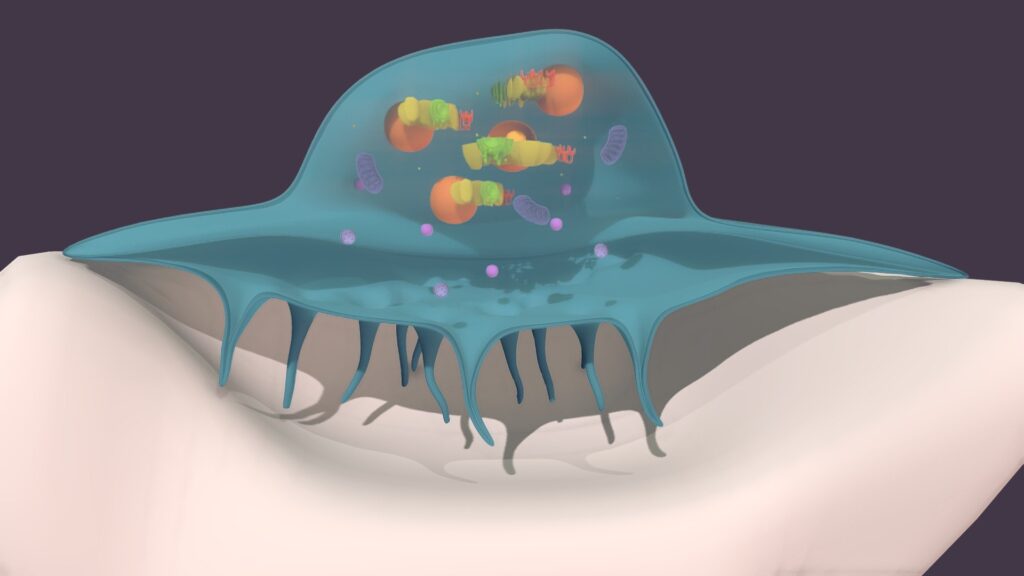
El osteoclasto activo se posiciona directamente sobre la superficie ósea, estableciendo una interacción íntima que resulta en la formación de una depresión característica denominada laguna de resorción o laguna de Howship. Esta estructura no es simplemente un efecto pasivo de desgaste, sino el resultado de un proceso altamente controlado en el que la célula crea un microambiente cerrado entre su membrana y el hueso. En este espacio confinado se liberan protones y enzimas hidrolíticas que disuelven tanto la fracción mineral como la matriz orgánica del hueso.
La capacidad del osteoclasto para degradar tejido óseo depende de su compleja organización en dominios funcionales especializados. Esta compartimentalización permite que distintos procesos ocurran simultáneamente sin interferencias, optimizando la eficiencia celular.
El borde festoneado representa la región más activa en términos de resorción. Se trata de una zona altamente plegada de la membrana plasmática que incrementa enormemente la superficie de contacto con el hueso. Estos pliegues facilitan la secreción dirigida de enzimas lisosomales y protones hacia el compartimento de resorción. La abundancia de mitocondrias en esta región refleja la elevada demanda energética asociada al transporte activo de protones, necesario para acidificar el microambiente y permitir la disolución de los cristales minerales.
Adyacente a esta región se encuentra la zona clara o zona de sellado, que cumple una función esencial en la delimitación del espacio de resorción. Su composición rica en microfilamentos de actina le confiere propiedades contráctiles y estructurales que permiten mantener un contacto hermético con la superficie ósea. Este sello evita la dispersión de enzimas y protones hacia el entorno extracelular, asegurando que la degradación ocurra de manera localizada y eficiente. La presencia de moléculas de adhesión especializadas refuerza esta unión, estableciendo un anclaje firme entre la célula y la matriz mineralizada.
Por otro lado, la región basolateral participa en la fase final del proceso de resorción. Una vez que los componentes del hueso han sido degradados y endocitados en el borde festoneado, son transportados a través de vesículas hacia esta región. Allí, el material procesado es liberado al medio extracelular mediante exocitosis. Este flujo vectorial de material, desde la superficie ósea hacia el exterior celular, ilustra la sofisticación del sistema de transporte intracelular del osteoclasto.
Integración funcional en la dinámica del tejido óseo
El papel de los osteoclastos no puede entenderse de manera aislada, sino como parte de un sistema integrado de remodelación ósea. Su actividad está coordinada con la de los osteoblastos, que son responsables de la formación de nuevo tejido óseo. Aunque ambos tipos celulares tienen orígenes distintos, su interacción funcional es fundamental para mantener la integridad estructural del esqueleto.
La resorción ósea llevada a cabo por los osteoclastos permite la eliminación de tejido envejecido o dañado, así como la liberación de minerales almacenados, como el calcio. Este proceso es esencial no solo para la renovación estructural, sino también para la regulación del equilibrio mineral del organismo. La precisión con la que los osteoclastos ejecutan esta función refleja un alto grado de especialización evolutiva, en la que convergen mecanismos de adhesión, secreción, digestión extracelular y transporte intracelular.

Fuente y lecturas recomendadas:
- Ross, M. H. & Pawlina, W. (2020). Histología: texto y atlas: correlación con biología molecular y celular (8.ª ed.). Wolters Kluwer.
- Gartner, L. P. (2020). Textbook of Histology (5th ed.). Elsevier.
- Karp, G., Iwasa, J., & Marshall, W. (2019). Biología celular y molecular: conceptos y experimentos (8.ª ed.). McGraw-Hill Interamericana.