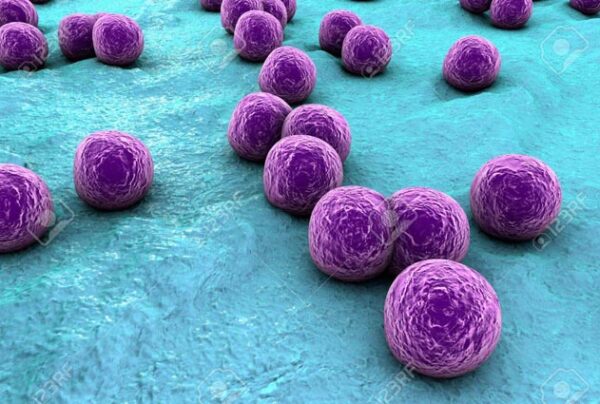
Los estafilococos constituyen un género de bacterias Gram-positivas esféricas (cocos) que se disponen típicamente en racimos semejantes a racimos de uvas. Su estructura celular y sus componentes fisiológicos les confieren capacidades únicas de supervivencia en distintos ambientes, así como mecanismos específicos de evasión inmunológica y resistencia antibiótica. La comprensión de estos elementos es esencial para explicar tanto su patogenicidad como su persistencia clínica en infecciones humanas.
Cápsula y Capa de Limo
La superficie externa de la pared celular de muchos estafilococos está recubierta por una cápsula polisacárida. Esta cápsula es un componente estructural altamente variable, cuya composición determina diferentes serotipos. Por ejemplo, en Staphylococcus aureus, los serotipos 1 y 2 presentan cápsulas particularmente gruesas, generando colonias de aspecto mucoide, aunque estas formas raramente están asociadas con enfermedad humana. En contraste, los serotipos 5 y 8 son los predominantes en aproximadamente el setenta y cinco por ciento de las infecciones humanas, lo que sugiere una relación directa entre ciertas cápsulas y la capacidad de causar enfermedad.
La cápsula actúa como un escudo protector contra el sistema inmunológico. Específicamente, inhibe la fagocitosis por parte de los leucocitos polimorfonucleares, lo que permite a la bacteria persistir en tejidos y fluidos corporales sin ser eliminada eficientemente. Además, muchos estafilococos producen una película extracelular suelta y soluble en agua, conocida como capa de limo o biofilm, compuesta por monosacáridos, proteínas y pequeños péptidos. Esta sustancia extracelular facilita la adhesión de las bacterias a superficies tisulares y a cuerpos extraños implantados, como catéteres, prótesis valvulares, articulaciones artificiales y derivaciones quirúrgicas. La capa de limo es especialmente crítica para la supervivencia de estafilococos coagulasa-negativos, que son relativamente poco virulentos pero pueden colonizar dispositivos médicos y resistir la eliminación por el huésped.
Peptidoglicano y Enzimas Asociadas
La pared celular de los estafilococos está compuesta en gran parte por peptidoglicano, un polímero de azúcares y aminoácidos que proporciona rigidez estructural y resistencia osmótica. En términos cuantitativos, aproximadamente la mitad del peso de la pared celular corresponde a peptidoglicano. Este polímero está formado por cadenas de glicanos compuestas por subunidades alternadas de ácido N-acetilmurámico y N-acetilglucosamina, típicamente entre diez y doce subunidades por cadena. Cada subunidad de ácido N-acetilmurámico tiene unida una cadena oligopeptídica, la cual se enlaza mediante puentes peptídicos con cadenas adyacentes, generando un entramado tridimensional altamente entrecruzado. A diferencia de las bacterias Gram-negativas, en las Gram-positivas estas múltiples capas cruzadas confieren una rigidez considerable, esencial para mantener la integridad celular frente a estrés mecánico y osmótico.
La síntesis de peptidoglicano es mediada por enzimas denominadas proteínas fijadoras de penicilina, que catalizan los pasos de transpeptidación y elongación de las cadenas de glicano. Estas enzimas son el blanco molecular de los antibióticos β-lactámicos, incluyendo penicilinas y cefalosporinas. Sin embargo, ciertas cepas de S. aureus han adquirido genes, como mecA o mecC, que codifican proteínas modificadas de unión a penicilina (PBP2a), con afinidad reducida por estos antibióticos, permitiendo la supervivencia bacteriana aun en presencia de tratamiento antimicrobiano. El gen mecA se encuentra integrado en un elemento genético móvil denominado cassette cromosómico estafilocócico mec (SCCmec), cuya diversidad genética explica la aparición de cepas de Staphylococcus aureus resistentes a meticilina (MRSA) tanto en hospitales como en la comunidad.
Más allá de su función estructural, el peptidoglicano de los estafilococos presenta actividad biológica significativa. Puede estimular la liberación de pirógenos endógenos, activar el sistema del complemento, inducir la producción de interleucina 1 por monocitos y promover la agregación de leucocitos polimorfonucleares, lo que contribuye a la formación de abscesos y a la inflamación local durante la infección. De esta manera, el peptidoglicano no solo es un elemento estructural, sino también un modulador directo de la respuesta inmune del huésped.
Ácidos Teicoicos y Lipoteicoicos
Los ácidos teicoicos constituyen un componente fundamental adicional de la pared celular de los estafilococos, complementando la función estructural del peptidoglicano. Estos polímeros, ricos en fosfato, son específicos de cada especie y se presentan en dos formas principales según su localización y enlace químico. La primera forma está covalentemente unida a los residuos de ácido N-acetilmurámico del peptidoglicano, mientras que la segunda, conocida como ácido lipoteicoico, se ancla a los lípidos de la membrana citoplasmática.
Aunque los ácidos teicoicos son pobres en generar respuestas inmunes por sí mismos, pueden inducir una reacción inmunitaria específica cuando están asociados con peptidoglicano, estimulando la producción de anticuerpos. Su presencia no solo contribuye a la integridad estructural de la pared celular, sino que también desempeña un papel en la fijación de iones y en la regulación de la autólisis bacteriana, siendo un factor indirecto en la resistencia a ciertos antibióticos y a condiciones de estrés osmótico.
Proteínas de Adhesión de Superficie
Los estafilococos, y particularmente Staphylococcus aureus, expresan una gran variedad de proteínas superficiales que funcionan como factores de virulencia esenciales. Estas proteínas median la adhesión a proteínas de la matriz extracelular del huésped, como fibronectina, fibrinógeno, elastina y colágeno, facilitando la colonización de tejidos y la formación de biofilms.
La mayoría de estas proteínas están covalentemente unidas al peptidoglicano y se agrupan bajo el término MSCRAMM (microbial surface components recognizing adhesive matrix molecules), que resalta su capacidad de reconocer y unirse a moléculas adhesivas de la matriz. Entre las proteínas más estudiadas se encuentran:
1. Proteína A estafilocócica (spa): se une a la región Fc de los anticuerpos IgG1, IgG2 e IgG4, interfiriendo con la opsonización y la fagocitosis.
2. Proteínas de unión a fibronectina (FnBPA y FnBPB): facilitan la adhesión a la fibronectina presente en la matriz extracelular.
3. Factores de aglutinación (ClfA y ClfB, también llamados coagulasa): se unen al fibrinógeno y lo convierten en fibrina insoluble, provocando la agregación o “clumping” de las bacterias.
Estas proteínas permiten que la bacteria establezca infecciones al adherirse firmemente a las células y tejidos del huésped. Es importante destacar dos aspectos clave: primero, S. aureus posee múltiples proteínas superficiales especializadas para la adhesión; segundo, algunas de estas proteínas son exclusivas de S. aureus, sirviendo como marcadores diagnósticos para identificar la especie.
Membrana Citoplasmática
La membrana citoplasmática de los estafilococos está compuesta por una matriz compleja de proteínas, lípidos y pequeñas cantidades de carbohidratos. Esta membrana actúa como barrera osmótica, protegiendo a la célula de cambios bruscos en la concentración de solutos en el entorno. Además, la membrana proporciona un anclaje funcional para numerosas enzimas implicadas en la biosíntesis celular y la respiración, como aquellas que participan en la síntesis de lípidos, proteínas y componentes de la pared celular. La integridad y la funcionalidad de esta membrana son esenciales para la supervivencia bacteriana, la resistencia a estrés ambiental y la capacidad de la bacteria de generar energía y materiales necesarios para su proliferación.

Fuente y lecturas recomendadas:
- Madigan, M. T., Martinko, J. M., Bender, K. S., Buckley, D. H., & Stahl, D. A. (2018). Brock biology of microorganisms (15th ed.). Pearson.
- Murray, P. R., Rosenthal, K. S., & Pfaller, M. A. (2025). Medical microbiology (10th ed.). Elsevier.
- Carroll, K. C., & Pfaller, M. A. (2023). Manual of clinical microbiology (13th ed.). American Society for Microbiology Press.
- Riedel, S., Hobden, J. A., Miller, S., Morse, S. A., Mietzner, T. A., Detrick, B., Mitchell, T. G., Sakanari, J. A., Hotez, P., & Mejía, R. (2020). Microbiología médica (28ª ed.). McGraw-Hill Interamericana Editores.