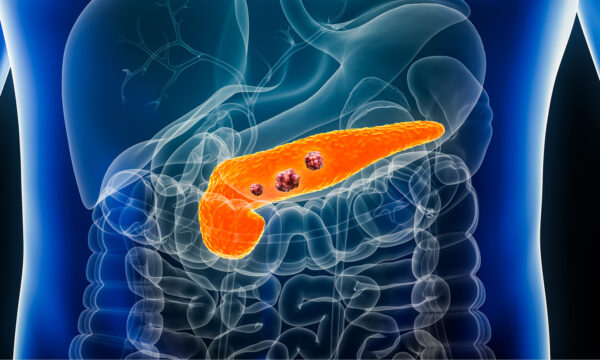
El carcinoma es la neoplasia más frecuente del páncreas debido a una combinación de factores genéticos, ambientales y biológicos que afectan a este órgano altamente especializado. La mayor parte de los carcinomas pancreáticos (aproximadamente el 75%) se localizan en la cabeza del páncreas, mientras que el 25% restante se sitúa en el cuerpo y la cola. Esta distribución anatómica se relaciona con la estructura del drenaje ductal pancreático y la cercanía de la cabeza del páncreas a la ampolla de Vater, zona en la que convergen el conducto pancreático principal y el colédoco antes de desembocar en el duodeno.
Los carcinomas pancreáticos representan aproximadamente el 3% de todos los cánceres, pero son responsables del 7% de las muertes por cáncer, lo que refleja su elevada letalidad y la tendencia al diagnóstico en fases avanzadas. De hecho, la incidencia de este tipo de cáncer ha ido en aumento, especialmente en mujeres menores de 55 años, un fenómeno que aún está siendo estudiado, pero que podría relacionarse con cambios en los estilos de vida, exposiciones ambientales y factores hormonales.
En contraste, los carcinomas de la ampolla de Vater son mucho menos frecuentes. Esta neoplasia ampular, aunque más accesible al diagnóstico por su tendencia a obstruir precozmente la vía biliar (lo que puede generar ictericia), no alcanza la prevalencia del adenocarcinoma pancreático.
Entre los factores de riesgo identificados para el desarrollo del cáncer de páncreas se incluyen la edad avanzada, el consumo de tabaco (implicado en un 20 a 25% de los casos), el consumo excesivo de alcohol, la obesidad, la pancreatitis crónica, la diabetes mellitus, la exposición previa a radiación abdominal, los antecedentes familiares y posiblemente la presencia de litiasis biliar, úlcera gástrica o exposición a sustancias tóxicas como el arsénico y el cadmio.
Un signo clínico temprano, aunque inespecífico, es la aparición de diabetes mellitus de reciente inicio en personas mayores de 45 años, la cual puede ser un indicador inicial de un carcinoma pancreático subyacente. De igual manera, la pérdida de peso inexplicada puede preceder al diagnóstico clínico. En pacientes diabéticos, el uso de metformina y, posiblemente, de ácido acetilsalicílico se ha asociado con una ligera reducción del riesgo, mientras que el tratamiento con insulina y agonistas del receptor del péptido similar al glucagón tipo 1 (como la sitagliptina) podría aumentarlo.
Aproximadamente el 7% de los pacientes con cáncer pancreático tienen antecedentes familiares en un familiar de primer grado, en comparación con apenas el 0.6% en la población general. Esto sugiere una fuerte componente genética, en especial cuando el carcinoma forma parte de síndromes hereditarios como el cáncer de mama familiar (particularmente en portadores de mutaciones en el gen BRCA2, quienes tienen un riesgo vitalicio del 7% de desarrollar cáncer pancreático), la pancreatitis hereditaria, el síndrome de Peutz-Jeghers, el síndrome de melanoma múltiple familiar atípico, la ataxia-telangiectasia y el síndrome de Lynch.
La mayoría de los cánceres de páncreas tienen su origen en lesiones precursoras microscópicas denominadas neoplasias pancreáticas intraepiteliales, que miden menos de 5 milímetros de diámetro. Estas lesiones suelen ser imperceptibles mediante técnicas de imagen convencionales, lo que dificulta su detección precoz.
A pesar del predominio del adenocarcinoma ductal pancreático, existen otros tipos de neoplasias pancreáticas, menos frecuentes pero clínicamente relevantes. Los tumores neuroendocrinos, por ejemplo, representan entre el 1% y el 2% de las neoplasias pancreáticas. Pueden ser funcionales (secretando hormonas como gastrina, insulina, glucagón, somatostatina, ACTH, entre otras) o no funcionales. Aunque en general tienen un pronóstico más favorable, pueden comportarse de forma agresiva si no se detectan a tiempo.
Las neoplasias quísticas del páncreas constituyen menos del 10% de las neoplasias pancreáticas, pero su importancia clínica es considerable, ya que los quistes pancreáticos son comunes y pueden confundirse con pseudocistos. La sospecha de una neoplasia quística debe surgir ante la presencia de una lesión quística pancreática sin antecedentes de pancreatitis o trauma abdominal. Se estima que al menos el 15% de los quistes pancreáticos son de naturaleza neoplásica.
Dentro de este grupo, los cistoadenomas serosos (responsables del 32–39% de las neoplasias quísticas) son benignos. Sin embargo, otros tipos como las neoplasias quísticas mucinosas (definidas por la presencia de estroma ovárico y responsables del 10–45% de las neoplasias quísticas), las neoplasias mucinosas papilares intraductales (21–33%), los tumores sólidos pseudopapilares (menos del 5%, que suelen afectar a mujeres jóvenes) y los tumores quísticos de células de los islotes (3–5%) presentan potencial maligno. Aunque su pronóstico es en general más favorable que el del adenocarcinoma pancreático, este depende del grado de avance local o sistémico al momento del diagnóstico.
Manifestaciones clínicas
El dolor se presenta en más del setenta por ciento de los casos de cáncer pancreático y suele caracterizarse por ser inespecífico, difuso y localizado principalmente en el epigastrio, es decir, en la parte superior central del abdomen. Cuando la lesión tumoral afecta la cola del páncreas, el dolor se puede sentir en el cuadrante superior izquierdo del abdomen. Es común que este dolor se irradie hacia la región dorsal, incluso llegando a predominar en la espalda, lo cual refleja la íntima relación anatómica del páncreas con estructuras nerviosas profundas.
Una característica clínica relevante es que el dolor puede aliviarse parcialmente al sentarse y flexionarse hacia adelante, maniobra que cambia la posición del páncreas y reduce la presión sobre estructuras adyacentes. Este hallazgo suele indicar que el tumor ha invadido tejidos circundantes fuera del órgano, lo que generalmente significa que la enfermedad ha alcanzado un estado avanzado e inoperable.
Entre los síntomas menos frecuentes, pero importantes de reconocer, está la diarrea, que puede deberse a una digestión inadecuada provocada por la insuficiencia exocrina pancreática. Un signo raro pero significativo es la tromboflebitis migratoria, que refleja un estado procoagulante asociado con la neoplasia.
La pérdida de peso es una manifestación común en estos pacientes y puede estar acompañada por síntomas neuropsiquiátricos como la depresión, los cuales a menudo agravan el cuadro clínico general. Alteraciones metabólicas precedentes al diagnóstico incluyen hiperglucemia, reducción de la grasa subcutánea abdominal y disminuciones en los niveles séricos de lípidos, reflejando cambios metabólicos sistémicos que anticipan la presencia tumoral.
En algunos pacientes, generalmente mayores de cuarenta años, la presentación inicial puede simular una pancreatitis aguda, sin que se identifique otra causa evidente para esta inflamación, lo que debe alertar al clínico sobre la posibilidad de una neoplasia oculta.
La ictericia es un signo característico y habitualmente se debe a la obstrucción del conducto biliar común por un tumor ubicado en la cabeza del páncreas. En este contexto, la palpación de una vesícula biliar aumentada de tamaño y no dolorosa (signo de Courvoisier) sugiere la presencia de dicha obstrucción neoplásica, aunque existen excepciones frecuentes que limitan su valor diagnóstico absoluto.
Al examen físico, puede identificarse una masa abdominal dura, fija y en ocasiones dolorosa, señal de que el tumor ha alcanzado un tamaño significativo y ha afectado tejidos vecinos. En fases avanzadas de la enfermedad, la presencia de un nódulo duro en la región periumbilical, conocido como nódulo de Sister Mary Joseph, puede palparse, representando una metástasis cutánea de mal pronóstico.
Exámenes diagnósticos
En pacientes con cáncer pancreático, puede observarse anemia leve, resultado de la cronicidad y el impacto sistémico de la enfermedad. Alteraciones metabólicas relacionadas con la regulación de la glucosa son frecuentes; entre el diez y el veinte por ciento de los casos presentan glucosuria, hiperglucemia, intolerancia a la glucosa o incluso diabetes mellitus franca. Estas manifestaciones reflejan tanto el daño funcional del tejido endocrino pancreático como la respuesta metabólica del organismo ante la neoplasia.
Los niveles séricos de enzimas pancreáticas, como la lipasa y la amilasa, pueden estar elevados de manera ocasional, aunque no son marcadores consistentes para el diagnóstico. En contraste, las pruebas bioquímicas hepáticas suelen revelar alteraciones sugestivas de colestasis obstructiva, particularmente cuando el tumor se localiza en la cabeza pancreática y obstruye la vía biliar.
La presencia de esteatorrea en ausencia de ictericia es poco común, ya que la insuficiencia exocrina pancreática generalmente se manifiesta en etapas más avanzadas o cuando la obstrucción biliar no es el factor predominante. Por otro lado, la detección de sangre oculta en las heces puede indicar la presencia de un carcinoma en la ampolla de Vater; este tipo de neoplasia puede producir una combinación característica de obstrucción biliar y sangrado, que tiñe las deposiciones de un tono plateado distintivo.
Desde el punto de vista de marcadores tumorales, el antígeno carbohidrato 19-9 presenta una sensibilidad cercana al setenta por ciento y una especificidad del ochenta y siete por ciento para el cáncer pancreático; sin embargo, su utilidad en la detección temprana es limitada, dado que valores elevados también se observan en enfermedades inflamatorias del páncreas, como la pancreatitis aguda y crónica, así como en procesos infecciosos del sistema biliar, como la colangitis.
En contraste, los niveles plasmáticos de cromogranina A se encuentran elevados en un rango que va del ochenta y ocho al cien por ciento en pacientes con tumores neuroendocrinos pancreáticos, lo que convierte a este marcador en un indicador útil para el diagnóstico y seguimiento de esta subcategoría neoplásica.
La evaluación imagenológica juega un papel fundamental en el diagnóstico y estadificación del cáncer pancreático, orientando tanto el tratamiento como la planificación quirúrgica. La tomografía computarizada helicoidal con cortes finos y en múltiples fases, conocida como protocolo pancreático, suele ser el método inicial de elección debido a su alta sensibilidad, detectando masas tumorales en entre el setenta y seis y el noventa y seis por ciento de los casos. Esta técnica permite además identificar metástasis, definir con precisión la extensión local del tumor y guiar procedimientos diagnósticos como la aspiración con aguja fina percutánea, facilitando la obtención de material para estudios citológicos y marcadores tumorales.
Como alternativa a la tomografía computarizada, la resonancia magnética proporciona imágenes de alta resolución que pueden ser útiles en casos donde la tomografía no sea concluyente o esté contraindicada. La ecografía abdominal, por su parte, presenta limitaciones importantes debido a la interferencia del gas intestinal, lo que disminuye su confiabilidad en la visualización del páncreas y en la detección de lesiones.
La tomografía por emisión de positrones es una técnica sensible para la detección tanto del tumor primario como de metástasis a distancia, aunque su uso combinado con la tomografía computarizada para el estadiaje no se ha establecido como un procedimiento rutinario en la práctica clínica habitual.
Las técnicas invasivas como la arteriografía selectiva de las arterias celíaca y mesentérica superior pueden revelar la invasión vascular por el cáncer, dato crucial que contraindica la resección quirúrgica. Sin embargo, este procedimiento ha perdido protagonismo desde la introducción de la tomografía helicoidal multipropósito, que ofrece información anatómica y funcional de forma menos invasiva.
La ultrasonografía endoscópica se destaca por su mayor sensibilidad en la detección del cáncer pancreático en comparación con la tomografía computarizada y muestra una capacidad similar para evaluar el compromiso ganglionar y la posibilidad de resección quirúrgica. La ausencia de hallazgos patológicos en la ultrasonografía endoscópica prácticamente descarta la presencia de carcinoma pancreático. Además, esta técnica facilita la realización de aspiraciones o biopsias guiadas para confirmar el diagnóstico mediante análisis histopatológicos, marcadores tumorales y estudios genéticos.
La colangiopancreatografía retrógrada endoscópica es útil para clarificar resultados dudosos en tomografía o resonancia magnética, permitiendo delinear el sistema ductal pancreático y confirmar la presencia de neoplasias ampulares o biliares. La colangiopancreatografía por resonancia magnética ofrece una sensibilidad comparable a la de la técnica endoscópica para la detección de cáncer pancreático, siendo menos invasiva.
En algunos centros especializados, procedimientos avanzados como la pancreatoscopia o la ultrasonografía intraductal se emplean para evaluar defectos de llenado en el conducto pancreático y determinar la resecabilidad de neoplasias mucinosas papilares intraductales.
Cuando se produce la obstrucción de la vena esplénica, pueden aparecer esplenomegalia o varices gástricas, detectables mediante endoscopia, ultrasonografía endoscópica o angiografía, reflejando complicaciones hemodinámicas secundarias.
Las neoplasias quísticas pancreáticas se distinguen por características específicas en las imágenes obtenidas por tomografía, ultrasonografía endoscópica y colangiopancreatografía retrógrada endoscópica, así como por el análisis macroscópico, citológico y genético del líquido contenido en los quistes. Por ejemplo, los cistoadenomas serosos suelen presentar una cicatriz central o un patrón en panal de abeja. Los cistoadenomas mucinosos se caracterizan por ser uni o multiloculares, con líquido rico en mucina, niveles bajos de glucosa (menores de veinticinco miligramos por decilitro o uno coma cuatro milimoles por litro), elevación del antígeno carcinoembrionario (superior a ciento noventa y dos nanogramos por mililitro o ciento noventa y dos microgramos por litro) y variantes patogénicas en los genes KRAS y GNAS. Por último, las neoplasias mucinosas papilares intraductales se asocian con la dilatación del conducto pancreático y la extrusión de material gelatinoso a través de la ampolla de Vater.
Estadificación
La estadificación del cáncer pancreático se realiza habitualmente mediante el sistema TNM, una clasificación universalmente aceptada que permite categorizar la enfermedad según el tamaño y extensión del tumor primario (T), el compromiso de los ganglios linfáticos regionales (N) y la presencia o ausencia de metástasis a distancia (M). Esta categorización resulta esencial no solo para estimar el pronóstico a largo plazo del paciente, sino también para guiar las decisiones terapéuticas, incluyendo la selección de candidatos para tratamientos adyuvantes o neoadyuvantes.
Dentro del espectro del cáncer pancreático localizado, se reconocen diferentes subgrupos que varían en su posibilidad de tratamiento quirúrgico. El tumor puede ser resecable, lo que implica que puede ser extirpado completamente con márgenes libres de tumor mediante cirugía. También existe la categoría de tumores borderline resecables, en los que la neoplasia compromete estructuras vasculares mayores, como la arteria mesentérica superior o la vena porta, pero en una extensión que podría permitir una resección tras un tratamiento previo. Finalmente, se encuentra la enfermedad localmente avanzada, en la cual la invasión tumoral a estructuras vitales impide la resección quirúrgica curativa, limitando las opciones terapéuticas a tratamientos paliativos o a terapias sistémicas.
Es importante destacar que más del treinta por ciento de los pacientes son diagnosticados cuando la enfermedad ya se encuentra en esta etapa localmente avanzada, lo que dificulta considerablemente las opciones curativas. Aún más, más de la mitad de los casos presentan enfermedad metastásica al momento del diagnóstico, situación que generalmente contraindica la cirugía y se asocia con un pronóstico reservado.
Tratamiento
La exploración abdominal quirúrgica suele ser necesaria en aquellos casos en los que no se ha logrado obtener un diagnóstico citológico definitivo o cuando se plantea la posibilidad de resección del tumor, lo que ocurre en hasta un treinta por ciento de los pacientes con carcinoma pancreático. En pacientes que presentan una masa localizada en la cabeza del páncreas sin ictericia clínica, la laparoscopía diagnóstica puede revelar la presencia de pequeñas metástasis peritoneales o hepáticas no detectables con otros métodos de imagen, lo que evita la realización de una cirugía mayor innecesaria en aproximadamente entre el cuatro y el trece por ciento de estos pacientes.
La resección radical mediante una pancreaticoduodenectomía, conocida también como procedimiento de Whipple, está indicada para neoplasias confinadas estrictamente a la cabeza pancreática, la región periampular o el duodeno, sin evidencia de afectación ganglionar o metastásica (etapa T1, N0, M0). En este grupo, la tasa de supervivencia a cinco años oscila entre el veinte y el veinticinco por ciento, aumentando hasta un cuarenta por ciento en aquellos casos en que los márgenes quirúrgicos son negativos y no existe compromiso de los ganglios linfáticos.
Previa a la cirugía, se puede realizar una descompresión endoscópica del conducto biliar obstruido mediante la colocación de un stent plástico o metálico de corta longitud, aunque este procedimiento no ha demostrado reducir la mortalidad operatoria y puede estar asociado a complicaciones como infecciones o migración del stent.
Los mejores resultados quirúrgicos se obtienen en centros especializados que cuentan con un enfoque multidisciplinario para el tratamiento del cáncer pancreático, integrando cirugía, oncología, radioterapia y cuidados paliativos.
El tratamiento adyuvante con quimioterapia ha demostrado mejorar la supervivencia en comparación con la ausencia de terapia complementaria. Los regímenes más comunes incluyen gemcitabina, 5-fluorouracilo o la combinación de gemcitabina con capecitabina. Recientemente, combinaciones como gemcitabina con capecitabina o esquemas modificados de FOLFIRINOX (que incluye 5-fluorouracilo, leucovorina, irinotecán y oxaliplatino) han mostrado superioridad frente a la gemcitabina sola. La utilidad de la quimioterapia concomitante con radioterapia en el contexto adyuvante es un tema controversial, aunque es ampliamente empleada en Estados Unidos.
En cuanto al tratamiento neoadyuvante, que se administra antes de la cirugía, ha ganado terreno con el objetivo de reducir el tamaño tumoral y mejorar la posibilidad de resección en pacientes con tumores inicialmente resecables o borderline. Los esquemas más usados en este contexto incluyen FOLFIRINOX y gemcitabina combinada con nanopartículas de albúmina unidas a paclitaxel (nab-paclitaxel). La quimiorradioterapia neoadyuvante puede lograr la reducción tumoral necesaria para convertir aproximadamente al treinta por ciento de pacientes con enfermedad localmente avanzada en candidatos a cirugía.
Cuando la resección quirúrgica no es factible, la colocación endoscópica de stents biliares es el método preferido para aliviar la ictericia obstructiva. En pacientes con una expectativa de vida inferior a seis meses o cuando está prevista una cirugía posterior, se prefiere generalmente un stent plástico debido a su menor costo y facilidad de reemplazo. Por otro lado, en pacientes con supervivencia esperada igual o mayor a seis meses, se recomienda el uso de stents metálicos debido a su mayor durabilidad. La utilización de stents metálicos cubiertos, diseñados para evitar el crecimiento tumoral hacia el interior del conducto, aún es objeto de debate, ya que estos dispositivos presentan mayor incidencia de migración y pueden provocar colecistitis aguda por obstrucción del conducto cístico.
En pacientes con expectativa de vida superior a seis meses, puede considerarse la realización de una derivación quirúrgica biliar para evitar la obstrucción. Asimismo, la derivación duodenal quirúrgica se valora en aquellos pacientes con riesgo inminente de obstrucción gástrica o duodenal; como alternativa menos invasiva, la colocación endoscópica de un stent duodenal autoexpandible puede ser viable.
Finalmente, en casos de cáncer pancreático irresecable confinado al órgano, la quimiorradioterapia puede emplearse con fines paliativos, buscando aliviar síntomas y mejorar la calidad de vida.
En el cáncer pancreático metastásico, se han observado mejores tasas de respuesta con regímenes quimioterapéuticos intensivos como FOLFIRINOX, que combina 5-fluorouracilo, leucovorina, irinotecán y oxaliplatino, así como con la combinación de gemcitabina y nab-paclitaxel, que aprovecha la formulación ligada a albúmina para mejorar la entrega del fármaco. En pacientes que han recibido tratamientos previos, la administración de un esquema que incluye 5-fluorouracilo, leucovorina y nanoliposomal irinotecán ha demostrado prolongar la supervivencia en comparación con el uso de 5-fluorouracilo y leucovorina de manera aislada, reflejando avances en la segunda línea terapéutica.
Para el control del dolor, uno de los síntomas más debilitantes en esta enfermedad, se emplean técnicas intervencionistas como el bloqueo del plexo celíaco, que puede realizarse bajo guía de tomografía computarizada o mediante ultrasonido endoscópico, y la esplacnectomía toracoscópica. Estas intervenciones buscan interrumpir la transmisión nerviosa del dolor visceral, proporcionando alivio en pacientes con síntomas refractarios a analgesia convencional.
En cuanto a los tumores neuroendocrinos pancreáticos, la resección quirúrgica representa el tratamiento de elección cuando la extirpación completa es posible, siendo estos tumores generalmente más indolentes. En lesiones menores a un centímetro, no funcionantes y sin evidencia de invasión local o metástasis, se puede optar por un manejo expectante con vigilancia estricta. En presencia de enfermedad metastásica, el control se logra mediante terapias como análogos de somatostatina de acción prolongada, interferón, quimioterapia convencional, terapia con radionúclidos dirigida a receptores peptídicos y técnicas de chemoembolización, que buscan ralentizar la progresión tumoral y mejorar la calidad de vida.
Respecto a los quistes pancreáticos incidentales, existe un consenso en que aquellos menores o iguales a dos centímetros y asintomáticos presentan un riesgo bajo de malignidad invasiva. Estos quistes pueden ser monitoreados mediante estudios de imagen, preferentemente resonancia magnética, con evaluaciones iniciales al año y posteriores cada dos años si no se detectan cambios. La realización de ultrasonido endoscópico con aspiración con aguja fina se indica si el quiste aumenta a dos centímetros o más, o si aparecen características de alto riesgo como dilatación del conducto pancreático principal, componentes sólidos mayores o iguales a cinco milímetros o citología sospechosa. La detección de estas características debe orientar hacia la consideración de la resección quirúrgica, aunque el enfoque óptimo debe ser individualizado, favoreciendo la toma de decisiones compartida entre el equipo médico y el paciente.
La cirugía está indicada para neoplasias mucinosas quísticas, cistoadenomas serosos sintomáticos, tumores pseudopapilares sólidos (que presentan un riesgo de transformación maligna cercano al quince por ciento), y para aquellos tumores quísticos mayores de dos centímetros que no se hayan podido clasificar adecuadamente tras estudios con tomografía helicoidal, ultrasonido endoscópico y análisis del líquido quístico.
En cuanto a las neoplasias mucinosas papilares intraductales que involucran el conducto pancreático principal, se recomienda la resección en todos los casos debido a su alto potencial maligno. Por el contrario, las lesiones localizadas en los conductos secundarios pueden ser seguidas con imágenes seriadas siempre que cumplan ciertos criterios: ausencia de síntomas y características benignas, tamaño menor a tres centímetros (aunque algunos expertos sugieren un umbral más estricto de uno coma cinco centímetros, en pacientes mayores sin características preocupantes incluso lesiones mayores pueden ser vigiladas), y ausencia de nódulos murales no captantes, paredes engrosadas, cambios abruptos en el calibre del conducto pancreático con atrofia distal, o posibles dilataciones del conducto biliar y adenomiomatosis vesicular. La mayoría de estas lesiones benignas permanecen estables en el seguimiento, sin embargo, el riesgo de malignidad persiste a lo largo de más de una década. Además, este grupo de pacientes presenta un aumento del riesgo tanto para el desarrollo de carcinoma ductal pancreático como para otros cánceres no pancreáticos.
En ausencia de enfermedad localmente avanzada, la supervivencia de pacientes con neoplasias quísticas malignas es superior a la de aquellos con adenocarcinoma pancreático convencional.
Pronóstico
El pronóstico del carcinoma pancreático, especialmente cuando la lesión se localiza en el cuerpo o la cola del páncreas, es notablemente desfavorable. La mayoría de los pacientes, entre un 80 y 85%, son diagnosticados en estadios avanzados, con enfermedad localmente irresecable o con metástasis, lo que limita significativamente las opciones terapéuticas curativas. En consecuencia, la tasa de supervivencia a cinco años se mantiene baja, situándose entre el 2 y el 5%. Se ha observado una tendencia al descenso de las tasas de mortalidad, posiblemente vinculada a avances en diagnóstico temprano y tratamientos más efectivos.
Factores como la obesidad, particularmente en países occidentales, parecen influir negativamente en la mortalidad, probablemente por la asociación con un estado metabólico alterado que puede favorecer la progresión tumoral. Por otro lado, ciertos tratamientos farmacológicos han mostrado un impacto positivo en la supervivencia. Por ejemplo, en pacientes diabéticos con adenocarcinoma pancreático, el uso de metformina se ha relacionado con mejores resultados clínicos. Asimismo, la administración previa de estatinas, antes del diagnóstico de cáncer pancreático, podría estar asociada a una mejor supervivencia, lo que sugiere un posible efecto protector o modulador del tumor.
En contraste con el adenocarcinoma pancreático, los tumores de la ampolla de Vater presentan un pronóstico relativamente más favorable. Tras la resección quirúrgica, las tasas de supervivencia a cinco años oscilan entre el 20 y el 40%. Sin embargo, la presencia de ictericia y la afectación ganglionar son factores pronósticos adversos que disminuyen la probabilidad de supervivencia prolongada. En pacientes seleccionados con cáncer limitado a la cabeza pancreática, la resección quirúrgica puede ser factible y asociarse con una supervivencia razonablemente prolongada, lo que destaca la importancia de un diagnóstico oportuno y un abordaje multidisciplinario.
Para aquellos individuos con antecedentes familiares significativos, definidos por al menos dos familiares de primer grado con cáncer pancreático, o en presencia de síndromes genéticos que aumentan el riesgo de desarrollar esta neoplasia, se recomienda un programa de tamizaje anual. Este seguimiento debe incluir ultrasonido endoscópico y resonancia magnética en forma alternada, generalmente iniciándose a los 50 años. En portadores de variantes patogénicas específicas, como CKDN2A o PRSS1, la vigilancia debe adelantarse a los 40 años, mientras que en pacientes con síndrome de Peutz-Jeghers se sugiere comenzar a los 35 años. En todos los casos, la detección precoz es clave para mejorar el pronóstico, ya que permite la intervención quirúrgica en etapas más tempranas y potencialmente curativas.

Fuente y lecturas recomendadas:
- Abboud Y et al. Increasing pancreatic cancer incidence in young women in the United States: a population-based time-trend analysis, 2001-2018. Gastroenterology. 2023;164:978. [PMID: 36775072]
- Han Y et al. Optimal surveillance interval of branch duct intraductal papillary mucinous neoplasm of the pancreas. JAMA Surg. 2024:e237010. [PMID: 38231494]
- Marchegiani G et al. Surveillance for presumed BD-IPMN of the pancreas: stability, size, and age identify targets for discontinuation. Gastroenterology. 2023;165:1016. [PMID: 37406887]
- Redegalli M et al. Routine molecular profiling in both resectable and unresectable pancreatic adenocarcinoma: relevance of cytologic samples. Clin Gastroenterol Hepatol. 2023;21:2825. [PMID: 36280101]
- Sawhney MS et al. ASGE guideline on screening for pancreatic cancer in individuals with genetic susceptibility: summary and recommendations. Gastrointest Endosc. 2022;95:817. [PMID: 35183358]
- Wood LD et al. Pancreatic cancer: pathogenesis, screening, diagnosis, and treatment. Gastroenterology. 2022;163:386. [PMID: 35398344]