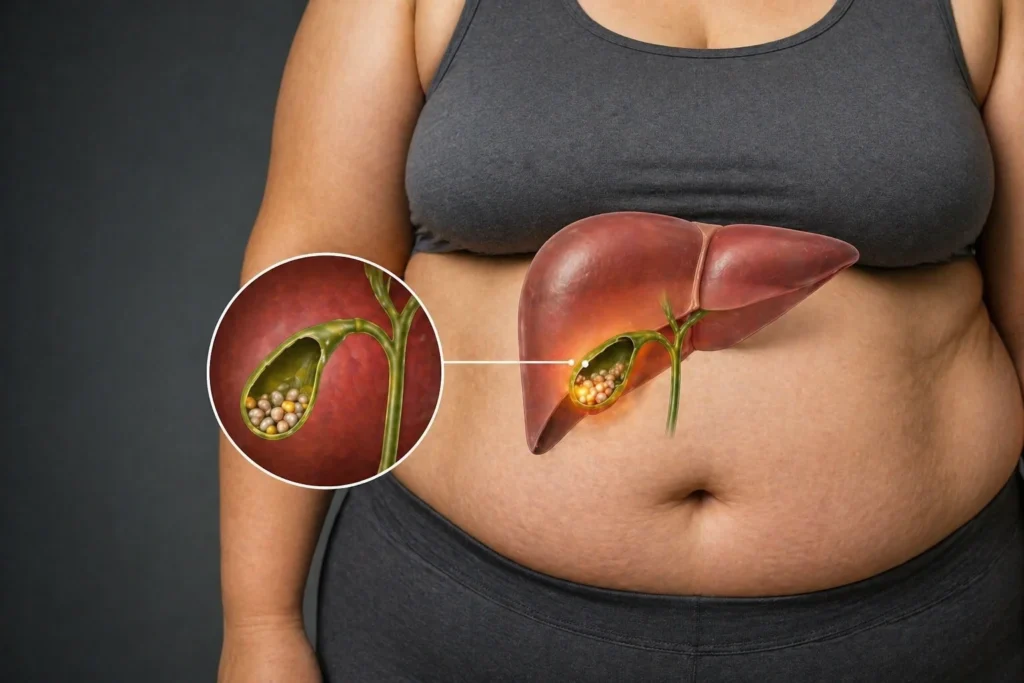
La enfermedad por cálculos biliares constituye una de las patologías digestivas más prevalentes a nivel mundial, con una tendencia creciente paralela al aumento de la obesidad. La transición epidemiológica hacia estilos de vida sedentarios y dietas hipercalóricas ha favorecido un incremento sostenido en la incidencia de litiasis biliar, particularmente en países industrializados y en regiones en desarrollo con rápida occidentalización dietética. Este fenómeno no es casual, ya que la obesidad altera de manera profunda el metabolismo hepático del colesterol, la composición de la bilis y la motilidad vesicular, generando un entorno altamente litogénico. Estudios poblacionales amplios han demostrado que el exceso de peso corporal es el determinante más importante en la formación de cálculos de colesterol, con un riesgo que aumenta proporcionalmente al índice de masa corporal y, de forma más precisa, a la adiposidad visceral.
El tejido adiposo, especialmente el visceral, actúa como un órgano endocrino que libera ácidos grasos libres y adipocinas que modulan la sensibilidad a la insulina y el metabolismo hepático. Este flujo aumentado de ácidos grasos hacia el hígado incrementa la síntesis de colesterol y su secreción en la bilis, favoreciendo la sobresaturación, paso inicial indispensable en la formación de cristales de colesterol. La asociación entre obesidad y litiasis biliar ha sido confirmada en múltiples cohortes, donde individuos con índice de masa corporal superior a 30 presentan hasta el doble de riesgo en comparación con sujetos normopeso, con una relación particularmente marcada en mujeres.
Factores dietéticos y su impacto en la composición biliar
El patrón dietético moderno, caracterizado por alto contenido calórico, abundancia de grasas saturadas y bajo aporte de fibra, desempeña un papel determinante en la fisiopatología de la enfermedad. La sobrenutrición induce hiperinsulinemia y estimula la actividad hepática de enzimas clave en la síntesis de colesterol, incrementando su secreción hacia la bilis. Este fenómeno conduce a una bilis sobresaturada, condición necesaria para la nucleación de cristales.
En contraste, la fibra dietética ejerce un efecto protector mediante varios mecanismos complementarios. Acelera el tránsito intestinal, lo que reduce el tiempo de contacto entre ácidos biliares y la microbiota intestinal, limitando su transformación y favoreciendo su excreción. Esto obliga al hígado a sintetizar nuevos ácidos biliares a partir de colesterol, disminuyendo así su concentración en la bilis. Además, la fibra puede interferir directamente con la absorción intestinal de colesterol, contribuyendo a una menor carga hepática.
El consumo de alcohol presenta una relación compleja con la litogénesis. Se ha observado que ingestas elevadas reducen la saturación de colesterol en la bilis, posiblemente mediante efectos sobre el metabolismo hepático lipídico y la secreción biliar, lo que confiere cierto efecto protector frente a cálculos de colesterol. Sin embargo, el consumo crónico induce daño hepático, altera la homeostasis de los ácidos biliares y favorece la formación de cálculos pigmentarios, evidenciando un efecto dual dependiente del contexto fisiopatológico.
En cuanto al café, se ha propuesto que estimula la liberación de colecistoquinina, aumentando la contracción vesicular y mejorando el flujo biliar. Este mecanismo podría reducir la estasis, uno de los factores clave en la formación de cálculos. No obstante, los resultados disponibles son heterogéneos y aún no permiten establecer una relación causal definitiva.
Medicamentos y estasis biliar
Diversas intervenciones farmacológicas y nutricionales influyen en la dinámica biliar. La nutrición parenteral total constituye un modelo paradigmático de estasis vesicular, ya que la ausencia de estímulos enterales reduce la liberación de colecistoquinina y, en consecuencia, la contracción de la vesícula biliar. Este estado favorece la acumulación de bilis concentrada y la formación de lodo biliar, que puede progresar a cálculos en un porcentaje considerable de pacientes. La introducción de alimentación oral, incluso en pequeñas cantidades, puede restaurar parcialmente la motilidad vesicular y disminuir este riesgo.
Fármacos como el octreótido y otros análogos de somatostatina reducen la secreción de colecistoquinina y enlentecen el tránsito intestinal, promoviendo la estasis biliar. Por el contrario, agentes hipolipemiantes como el ezetimiba disminuyen la absorción intestinal de colesterol, reduciendo su disponibilidad hepática, mientras que las estatinas inhiben la HMG-CoA reductasa, enzima limitante en la síntesis de colesterol. Ambos mecanismos disminuyen la saturación biliar y se han asociado con un menor riesgo de litiasis.
Enfermedad metabólica, resistencia a la insulina y litogénesis
La resistencia a la insulina representa un eje fisiopatológico central en la formación de cálculos de colesterol. La hiperinsulinemia crónica incrementa la captación hepática de colesterol y estimula su secreción hacia la bilis, al tiempo que reduce la síntesis y secreción de ácidos biliares. Este desequilibrio altera la proporción crítica entre colesterol, fosfolípidos y ácidos biliares, favoreciendo la sobresaturación.
Además, la insulina regula la actividad de la HMG-CoA reductasa, por lo que niveles elevados de esta hormona incrementan la producción endógena de colesterol. La combinación de mayor síntesis y mayor secreción biliar crea un entorno altamente propicio para la nucleación de cristales. Estudios metabólicos han demostrado que los pacientes con litiasis presentan concentraciones de insulina significativamente superiores a las de sujetos sanos, incluso en ausencia de diferencias en triglicéridos plasmáticos, lo que subraya el papel independiente de la resistencia a la insulina.
La distribución de la grasa corporal es un determinante más preciso que el peso total. La adiposidad abdominal, medida mediante circunferencia de cintura o índice cintura-cadera, se correlaciona estrechamente con la litogénesis debido a su asociación con mayor resistencia a la insulina y mayor flujo portal de ácidos grasos hacia el hígado.
Adicionalmente, las alteraciones en adipocinas contribuyen a la disfunción vesicular. La leptina, hormona implicada en la regulación del apetito y el metabolismo energético, también modula la motilidad de la vesícula biliar. Niveles disminuidos o resistencia a su acción pueden reducir la contractilidad vesicular, favoreciendo la estasis y, por ende, la formación de cálculos.
Inactividad física y dinámica enterohepática de los ácidos biliares
La actividad física ejerce efectos fisiológicos profundos sobre el eje intestino-hígado-vesícula biliar, modulando tanto la motilidad gastrointestinal como el metabolismo de los ácidos biliares. El ejercicio regular incrementa el peristaltismo intestinal, lo que reduce el tiempo de tránsito y limita la reabsorción excesiva de ácidos biliares en el íleon terminal. Este fenómeno favorece su excreción fecal y estimula la síntesis hepática compensatoria a partir de colesterol, disminuyendo así la carga de colesterol disponible para su secreción biliar. De manera paralela, la actividad física mejora la sensibilidad a la insulina, lo que atenúa la hiperinsulinemia y reduce la activación de vías lipogénicas hepáticas implicadas en la sobresaturación biliar.
La inactividad física, particularmente en individuos con periodos prolongados en posición sedente, induce una desaceleración del tránsito intestinal y una mayor eficiencia en la reabsorción de ácidos biliares. Esto reduce la necesidad de síntesis hepática de novo y contribuye a una acumulación relativa de colesterol en la bilis. Además, el sedentarismo favorece la resistencia a la insulina y la acumulación de grasa visceral, amplificando los mecanismos litogénicos previamente descritos. Estudios epidemiológicos han demostrado que un mayor gasto energético diario se asocia de manera inversa con la incidencia de enfermedad por cálculos biliares, lo que respalda el papel protector del ejercicio a través de mecanismos metabólicos y mecánicos bien definidos.
Pérdida rápida de peso y desestabilización del equilibrio biliar
La reducción acelerada de peso corporal, especialmente cuando supera 1.5 kg por semana, constituye una condición paradójicamente litogénica. Este fenómeno se observa tanto en dietas extremadamente hipocalóricas como en el contexto de cirugía bariátrica. Durante la pérdida rápida de peso, el tejido adiposo libera grandes cantidades de ácidos grasos hacia la circulación portal, lo que incrementa la captación hepática y estimula la síntesis de colesterol. Este exceso de colesterol es secretado en la bilis, generando sobresaturación.
Simultáneamente, la restricción calórica severa reduce la ingesta de grasas, lo que disminuye la liberación de colecistoquinina y, en consecuencia, la contracción vesicular. Este estado de hipomotilidad favorece la estasis biliar, permitiendo la nucleación y el crecimiento de cristales. La combinación de sobresaturación y estasis crea un entorno altamente propicio para la formación de cálculos en un periodo relativamente corto. Este mecanismo explica la elevada incidencia de litiasis observada en pacientes sometidos a procedimientos bariátricos, donde la rápida movilización de reservas lipídicas y la alteración de la motilidad gastrointestinal convergen de manera sinérgica.
Embarazo como estado litogénico transitorio
El embarazo representa un modelo fisiológico de litogénesis reversible. Los cambios hormonales, particularmente el aumento de estrógenos y progesterona, modifican de forma significativa la composición de la bilis y la motilidad vesicular. Los estrógenos incrementan la expresión de receptores hepáticos implicados en la captación de lipoproteínas y estimulan la síntesis de colesterol, lo que eleva su secreción biliar. Por otro lado, la progesterona ejerce un efecto relajante sobre el músculo liso, disminuyendo la contractilidad de la vesícula biliar y favoreciendo la estasis.
Este doble mecanismo genera una bilis sobresaturada en un contexto de vaciamiento ineficiente. Sin embargo, tras el parto, la normalización hormonal restablece gradualmente la motilidad vesicular y la composición biliar, lo que puede conducir a la resolución espontánea de lodo biliar o cálculos pequeños. Este carácter reversible subraya la importancia de factores funcionales y hormonales en la litogénesis, más allá de alteraciones estructurales permanentes.
Genética y regulación molecular del transporte de colesterol
La susceptibilidad genética desempeña un papel determinante en la formación de cálculos biliares, modulando procesos clave como la secreción de colesterol, la síntesis de ácidos biliares y la motilidad vesicular. Entre los determinantes más relevantes se encuentran las variantes en los transportadores ABCG5 y ABCG8, proteínas localizadas en la membrana canalicular de los hepatocitos que facilitan la excreción de colesterol hacia la bilis. La variante p.D19H se ha asociado con un incremento en la secreción de colesterol, lo que eleva la saturación biliar y favorece la nucleación de cristales.
Otros genes implicados incluyen aquellos que regulan la conversión de colesterol en ácidos biliares, como CYP7A1, enzima limitante en la vía clásica, y CYP27 y CYP7B1, involucrados en vías alternativas. Alteraciones en estos sistemas reducen la producción de ácidos biliares, alterando el equilibrio necesario para mantener el colesterol en solución.
El transportador ABCB4, responsable de la secreción de fosfolípidos hacia la bilis, también es fundamental, ya que los fosfolípidos estabilizan las micelas mixtas que solubilizan el colesterol. Su disfunción disminuye la capacidad de solubilización y favorece la precipitación.
El receptor de colecistoquinina tipo 1 participa en la regulación de la contracción vesicular y en la absorción intestinal de lípidos. Variantes que reducen su función pueden provocar hipomotilidad vesicular y mayor absorción de colesterol, contribuyendo a la litogénesis. Asimismo, asociaciones con ciertos antígenos HLA sugieren la participación de mecanismos inmunogenéticos en la susceptibilidad individual.
Microbiota intestinal y biogénesis de cálculos
La microbiota intestinal emerge como un modulador clave del metabolismo de los ácidos biliares y de la formación de cálculos. Las bacterias intestinales transforman los ácidos biliares primarios en secundarios mediante reacciones de desconjugación y deshidroxilación, alterando su hidrofobicidad y su capacidad para solubilizar colesterol. Estas modificaciones pueden influir en la composición del pool biliar y en su potencial litogénico.
Diversos géneros bacterianos han sido asociados con la enfermedad, incluyendo Clostridium, Bacteroides y Escherichia coli, los cuales poseen enzimas como β-glucuronidasa y fosfolipasa. Estas enzimas pueden hidrolizar compuestos biliares, generando productos menos solubles que favorecen la precipitación. Además, algunas bacterias forman biopelículas que actúan como núcleos para la agregación de cristales, facilitando la formación de cálculos pigmentarios y mixtos.
La presencia de microorganismos como Salmonella o Helicobacter pylori sugiere que infecciones crónicas pueden contribuir a la litogénesis mediante inflamación persistente y alteraciones en la secreción biliar. Aunque los mecanismos exactos aún se investigan, la evidencia apunta a una interacción compleja entre microbiota, metabolismo biliar e inmunidad local.


Fuente y lecturas recomendadas:
- Aune, D., Norat, T., Vatten, L. J., & Romundstad, P. R. (2016). Physical activity and the risk of gallbladder disease: A systematic review and meta-analysis. European Journal of Epidemiology, 31(7), 643–653.
- Biddinger, S. B., Haas, J. T., Yu, B. B., Bezy, O., Jing, E., Zhang, W., Unterman, T. G., Carey, M. C., & Kahn, C. R. (2008). Hepatic insulin resistance directly promotes formation of cholesterol gallstones. Nature Medicine, 14(7), 778–782.
- Everhart, J. E. (2004). Contributions of obesity and weight loss to gallstone disease. Annals of Internal Medicine, 140(7), 564–565.
- Ko, C. W., & Lee, S. P. (2002). Gallstones formation after rapid weight loss. Gastroenterology Clinics of North America, 31(4), 1033–1046.
- Lammert, F., Gurusamy, K., Ko, C. W., Miquel, J. F., Méndez-Sánchez, N., Portincasa, P., van Erpecum, K. J., van Laarhoven, C. J., Wang, D. Q., & Acalovschi, M. (2016). Gallstones. Nature Reviews Disease Primers, 2, 16024.
- Méndez-Sánchez, N., Zamora-Valdés, D., Flores-Rangel, J. A., Pérez-Sosa, J. A., Vásquez-Fernández, F., Lezama-Mora, J. I., & Uribe, M. (2004). Role of diet in cholesterol gallstone formation. Clinica Chimica Acta, 346(1), 1–12.
- Portincasa, P., Di Ciaula, A., Wang, D. Q. H., & Moschetta, A. (2012). An update on the pathogenesis and treatment of cholesterol gallstones. Nature Reviews Gastroenterology & Hepatology, 9(11), 662–673.
- Shiffman, M. L., Sugerman, H. J., Kellum, J. M., Moore, E. W., & Brewer, W. H. (1991). Gallstone formation after rapid weight loss: A prospective study in patients undergoing gastric bypass surgery. American Journal of Gastroenterology, 86(8), 1000–1005.
- Stinton, L. M., & Shaffer, E. A. (2012). Epidemiology of gallbladder disease: Cholelithiasis and cancer. Gut and Liver, 6(2), 172–187.
Wang, D. Q. H., Cohen, D. E., & Carey, M. C. (2009). Biliary lipids and cholesterol gallstone disease. Journal of Lipid Research, 50(Suppl), S406–S411.
Síguenos en X: @el_homomedicus y @enarm_intensivo Síguenos en instagram: homomedicus y en Treads.net como: Homomedicus