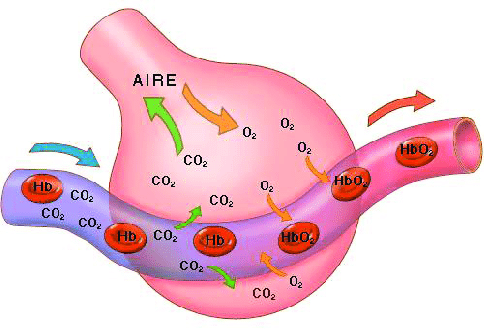
Después de la ventilación la siguiente fase de la respiración es la difusión del oxígeno desde los alvéolos hacia la sangre pulmonar y del dióxido de carbono desde la sangre a los alvéolos.
El proceso de difusión de gases a nivel alveolar es el movimiento aleatorio de moléculas en todas las direcciones a través de la membrana respiratoria y los líquidos adyacentes.
Cinética de los gases
Los gases importantes en fisiología respiratoria son moléculas simples que se mueven libremente entre por difusión.
La fuente de energía para que se produzca la difusión a nivel de la membrana alveolar procede del movimiento cinético de las propias partículas.
Las moléculas de los gases difunden desde un lado de la membrana respiratoria con una concentración elevada al otro lado donde exista una concentración más baja.
Presión parcial de los gases
La presión que ejerce un gas es directamente proporcional a la concentración de las moléculas del gas tanto en la sangre como en el aire alveolar.
En una mezcla de gases, la velocidad de difusión de cada uno de los gases que la conforman es directamente proporcional a la presión que genera el gas solo, lo que se denomina presión parcial de ese gas.
El aire que respiramos para fines prácticos tiene una composición aproximada del 79% de nitrógeno y el 21% de oxígeno.
El aire que respiramos, o aire atmosférico a nivel del mar, tiene una presión total de 760 mmHg.
A la presión total del aire atmosférico a nivel del mar contribuyen los siguientes gases:
👉el 79% por el nitrógeno (600 mmHg).
👉el 21% por el O2 (160 mmHg).
Los gases disueltos en agua o en los tejidos corporales también ejercen una presión.
La presión parcial de un gas en una solución está determinada:
👉por su concentración.
👉por el coeficiente de solubilidad del gas.
Coeficiente de solubilidad de los gases respiratorios
Oxígeno 0,024
Dióxido de carbono 0,57
Monóxido de carbono 0,018
Nitrógeno 0,012
Helio 0,008
En los líquidos cuando las moléculas de algún gas son atraídas por el agua se pueden disolver muchas más sin generar un exceso de presión parcial en el interior de la solución.
En los líquidos cuando las moléculas son repelidas por el agua, se generará una presión parcial elevada con menor cantidad de moléculas disueltas.
El dióxido de carbono es más de 20 veces más soluble que el oxígeno.
Como el CO2 es más soluble que el oxígeno, su presión parcial es menor de la que ejerce el O2.
La difusión neta de cada una de las sustancias entre el aire alveolar y la sangre está determinada por la diferencia entre las dos presiones parciales.
La presión parcial que ejercen las moléculas de agua para escapar a través de la superficie se denomina la presión de vapor del agua.
A la temperatura corporal normal (37 °C) la presión de vapor del agua en las vías respiratorias es de 47 mmHg.
Velocidad de difusión
Factores que afectan la velocidad de difusión de un gas en un líquido:
👉diferencia de presión.
👉solubilidad del gas en el líquido.
👉área transversal del líquido.
👉distancia a través de la cual debe difundir.
👉peso molecular del gas.
👉la temperatura del líquido.
Los gases importantes en fisiología respiratoria son muy solubles en lípidos por lo que son muy solubles en las membranas celulares.