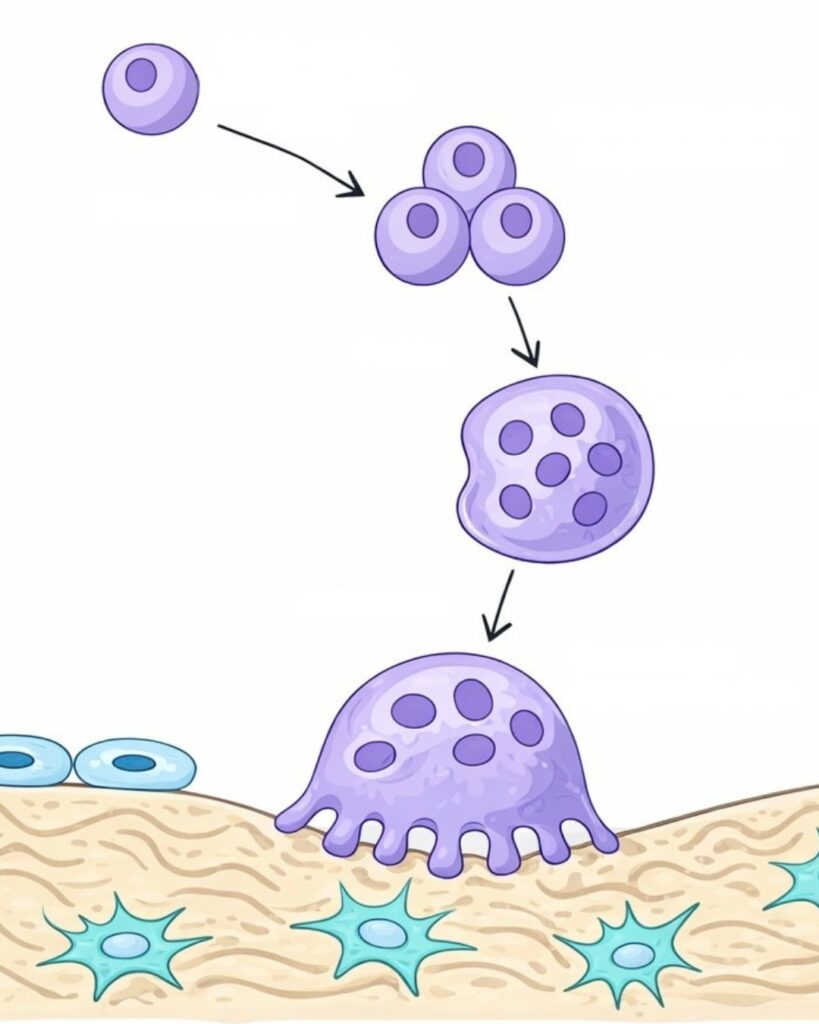
El origen de los osteoclastos constituye un ejemplo particularmente ilustrativo de cómo los sistemas biológicos integran información del desarrollo embrionario, la hematopoyesis y la regulación molecular para generar una célula altamente especializada. Comprender este origen requiere abandonar una visión lineal y simplificada, y en su lugar adoptar una perspectiva dinámica en la que convergen múltiples linajes celulares, señales ambientales y programas metabólicos.
En términos fundamentales, los osteoclastos no surgen de la estirpe osteoblástica ni de células propias del tejido óseo estructural, sino que derivan de la misma línea que origina a los monocitos y macrófagos. Esta procedencia revela una característica crucial: el hueso no es un tejido aislado, sino profundamente integrado con el sistema inmunológico y hematopoyético. Así, el osteoclasto puede entenderse como una célula inmunitaria altamente adaptada cuya función efectora ha sido redirigida hacia la degradación controlada de la matriz ósea.
Durante las primeras fases del desarrollo embrionario, antes de que la médula ósea asuma su papel hematopoyético definitivo, emergen en el saco vitelino poblaciones de progenitores eritromieloides. Estas células primitivas no solo participan en la formación inicial de elementos sanguíneos, sino que también generan macrófagos tisulares tempranos que colonizan diversos órganos en desarrollo. Entre estos macrófagos se encuentran aquellos que expresan el receptor del factor estimulante de colonias uno, lo que les confiere la capacidad de responder a señales proliferativas y de supervivencia esenciales. Estas células actúan como los primeros precursores de osteoclastos, contribuyendo de manera decisiva a la remodelación del esqueleto embrionario y, de forma especialmente relevante, a la creación de cavidades dentro del hueso que permitirán el establecimiento posterior de la hematopoyesis medular.
Con el avance hacia la vida postnatal, el sistema hematopoyético experimenta una transición hacia la médula ósea como órgano principal de producción celular. En este contexto, las células madre hematopoyéticas generan monocitos circulantes que conservan la capacidad de diferenciarse hacia la línea osteoclástica. Estos monocitos no actúan de manera independiente, sino que interactúan con poblaciones de osteoclastos de larga vida derivadas de los progenitores embrionarios. Esta interacción incluye procesos de fusión celular, mediante los cuales células mononucleares se incorporan a osteoclastos preexistentes, aumentando su tamaño, su contenido nuclear y su capacidad funcional. Este fenómeno establece un sistema híbrido en el que coexisten contribuciones embrionarias y adultas, garantizando tanto la persistencia como la adaptabilidad de la población osteoclástica.
El proceso mediante el cual estos precursores se convierten en osteoclastos funcionales está estrictamente regulado por señales moleculares específicas. Entre ellas destacan el factor estimulante de colonias de macrófagos y el ligando del receptor activador del factor nuclear kappa B. El primero asegura la supervivencia, proliferación y preparación de los precursores, mientras que el segundo actúa como el detonador de un programa de diferenciación altamente coordinado. La unión de este ligando a su receptor en la superficie de las células precursoras desencadena una cascada de señalización intracelular que culmina en la activación de factores de transcripción clave. Estos factores reorganizan el programa génico de la célula, promoviendo la adquisición de características distintivas del osteoclasto, como la capacidad de fusionarse, reorganizar su citoesqueleto y expresar enzimas especializadas en la degradación de la matriz ósea.
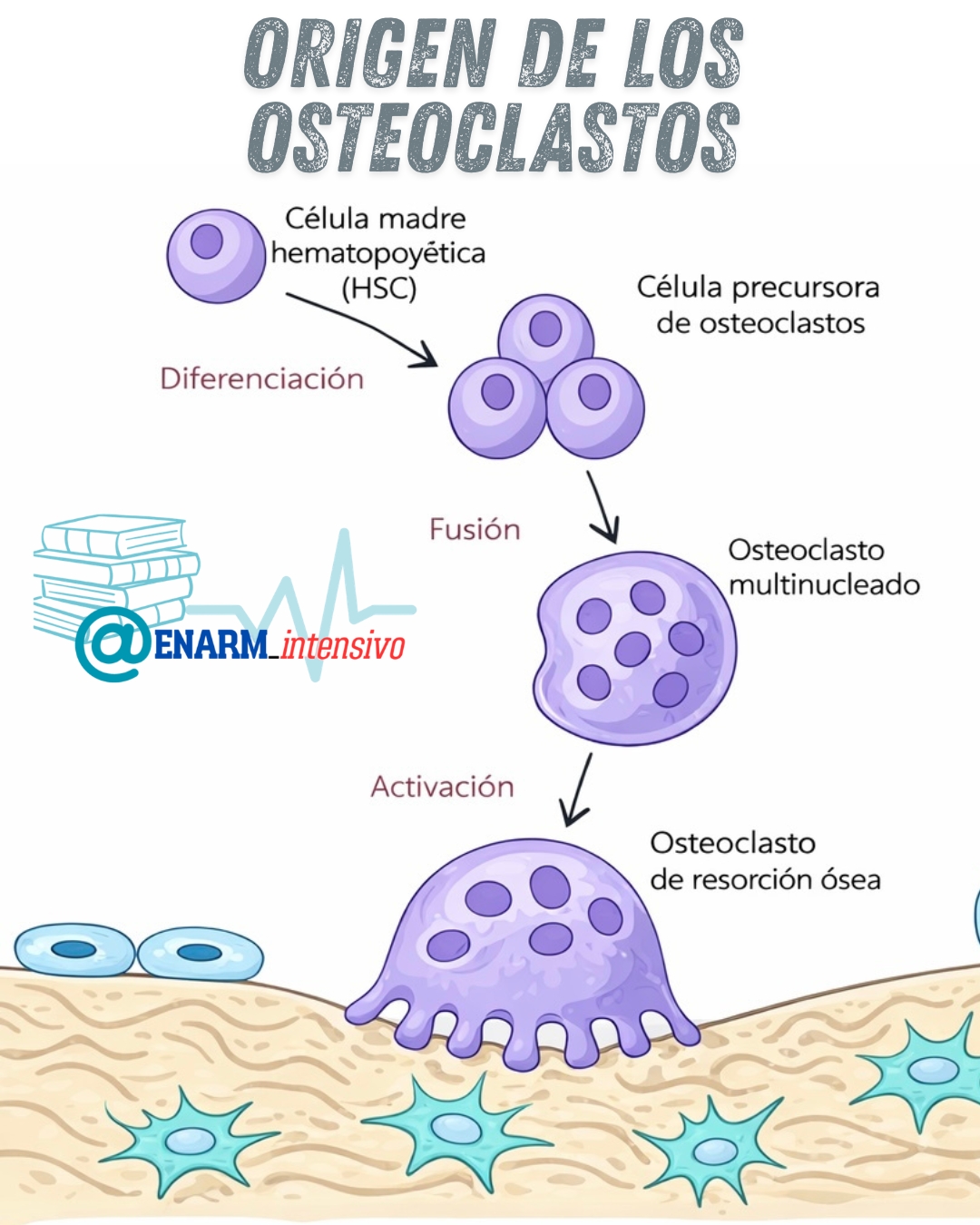
Sin embargo, la diferenciación osteoclástica no puede comprenderse únicamente en términos de señales genéticas. Un componente igualmente esencial es la reprogramación metabólica que acompaña a este proceso. A medida que los precursores avanzan hacia estados más diferenciados, experimentan una transformación en sus rutas de obtención y utilización de energía. Este cambio no es accesorio, sino constitutivo de su identidad funcional. La formación de células multinucleadas, la reorganización del citoesqueleto y la generación de compartimentos especializados para la resorción requieren una demanda energética considerable. En este contexto, diferentes rutas metabólicas contribuyen de manera secuencial o simultánea; no obstante, la glucólisis adquiere un papel predominante en las etapas en que la célula ejecuta activamente la resorción ósea, proporcionando energía de manera rápida y localizada.
La maduración del osteoclasto culmina con la adquisición de una polaridad funcional altamente especializada. La célula se adhiere firmemente a la superficie del hueso y establece una zona de sellado que delimita un microambiente cerrado. Dentro de este compartimento, el osteoclasto secreta protones y enzimas proteolíticas que disuelven los componentes minerales y degradan la matriz orgánica. Esta capacidad no solo depende de la expresión de proteínas específicas, sino también de la organización espacial de la célula, la cual es el resultado final de los complejos procesos de diferenciación y fusión previamente descritos.
El ciclo de vida de los osteoclastos no concluye necesariamente con su muerte. Tras completar su función, estas células pueden entrar en estados de inactividad, sufrir apoptosis o fragmentarse en unidades más pequeñas conocidas como osteomorfos. Estas estructuras conservan la capacidad de volver a fusionarse y regenerar osteoclastos funcionales, lo que introduce un nivel adicional de eficiencia y plasticidad en el sistema. Este mecanismo de reciclaje no solo optimiza el uso de recursos energéticos, sino que permite una respuesta rápida a las demandas cambiantes del tejido óseo.

Fuente y lecturas recomendadas:
- Gartner, L. P. (2020). Textbook of Histology (5th ed.). Elsevier.
- Karp, G., Iwasa, J., & Marshall, W. (2019). Biología celular y molecular: conceptos y experimentos (8.ª ed.). McGraw-Hill Interamericana.
- Ledesma-Colunga, M. G., Passin, V., Lademann, F., Hofbauer, L. C., & Rauner, M. (2023). Novel Insights into Osteoclast Energy Metabolism. Current osteoporosis reports, 21(6), 660–669. https://doi.org/10.1007/s11914-023-00825-3
- Ross, M. H. & Pawlina, W. (2020). Histología: texto y atlas: correlación con biología molecular y celular (8.ª ed.). Wolters Kluwer.