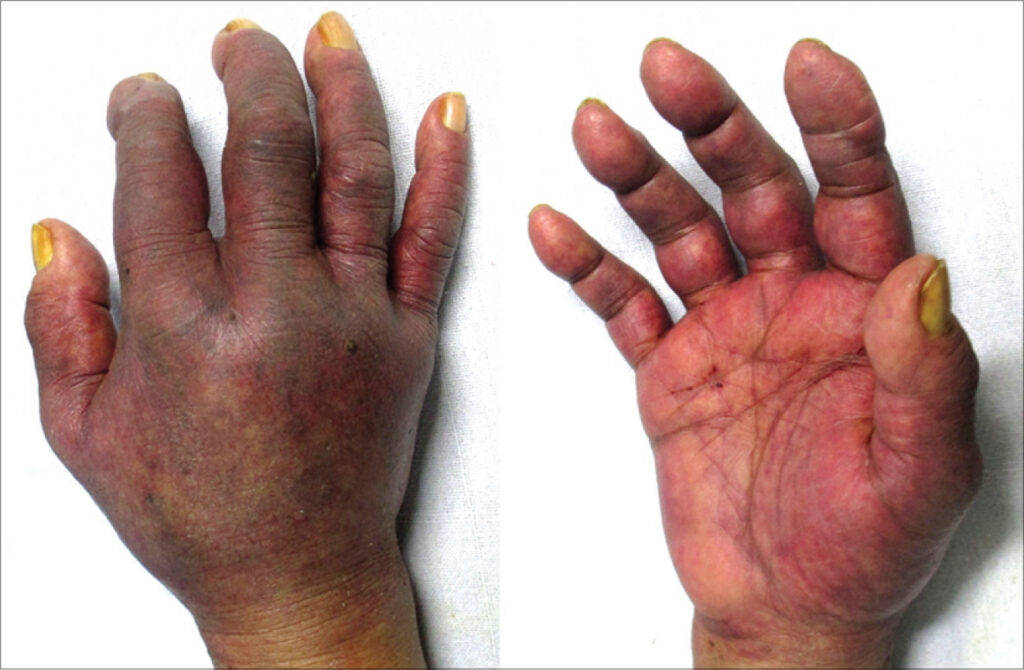
El síndrome del guante púrpura constituye una reacción adversa infrecuente pero clínicamente significativa, principalmente vinculada con la administración intravenosa de fenitoína, un anticonvulsivante empleado comúnmente en el tratamiento de crisis epilépticas. Esta entidad clínica se manifiesta por una llamativa decoloración purpúrea o azulada que rodea el sitio de inyección intravenosa, acompañada de edema periférico de rápida instauración y dolor localizado de intensidad variable. La afectación suele circunscribirse a la extremidad donde se ha administrado el fármaco, dando origen al nombre coloquial del síndrome, ya que la apariencia clínica simula la colocación de un guante teñido de púrpura.
Pese a ser reconocido desde hace varias décadas, el síndrome del guante púrpura sigue siendo una condición de etiología incierta. Su baja incidencia y su presentación clínica heterogénea han dificultado el esclarecimiento completo de sus mecanismos subyacentes. Sin embargo, se han identificado diversos factores de riesgo que parecen predisponer a su aparición. Entre ellos se destacan la edad avanzada, que puede asociarse a fragilidad capilar y disminución del flujo vascular periférico; el uso de dosis elevadas o múltiples de fenitoína en cortos periodos de tiempo; y la administración del medicamento en venas de pequeño calibre o en condiciones de perfusión comprometida.
Desde una perspectiva fisiopatológica, se ha postulado que la génesis del síndrome podría deberse, al menos en parte, a la irritación química local inducida por la composición de la formulación intravenosa de la fenitoína. Este fármaco, para mantenerse en solución, requiere un vehículo altamente alcalino, compuesto generalmente por propilenglicol y etanol, que permite su disolución pero le confiere una elevada osmolaridad y un pH significativamente básico. Estas características pueden desencadenar una serie de eventos adversos a nivel del endotelio vascular. Entre ellos, la vasoconstricción refleja, la disfunción endotelial y, eventualmente, la formación de microtrombos. Todo ello puede favorecer la extravasación del fármaco y sus excipientes hacia los tejidos circundantes, donde inducen una respuesta inflamatoria intensa, con aumento de la permeabilidad capilar, edema y decoloración característica debido a la estasis venosa y a la posible hemorragia dérmica local.
Además, se ha sugerido que la velocidad de infusión y el sitio anatómico de la administración pueden jugar un rol crítico. Las infusiones rápidas o en sitios distales, como el dorso de la mano, parecen incrementar el riesgo, probablemente por la menor capacidad de dilución del fármaco en estos vasos periféricos y la dificultad para disipar el daño químico local. El fenómeno resultante no solo compromete la integridad vascular, sino que también puede generar isquemia tisular en casos graves, requiriendo en ocasiones intervenciones quirúrgicas o tratamientos especializados para preservar la función del miembro afectado.
Es poco comprendido y solo se reportaron 82 casos entre 1984 y 2015.
Manifestaciones clínicas
El desarrollo del síndrome del guante púrpura parece estar influenciado por una serie de factores clínicos y fisiológicos que aumentan la vulnerabilidad del paciente a esta reacción adversa. Diversos perfiles de riesgo han sido identificados con mayor frecuencia en los casos documentados, incluyendo personas mayores de sesenta años, individuos de sexo femenino, pacientes con sepsis, aquellos con enfermedad vascular periférica, personas con antecedentes de enfermedades crónicas debilitantes y aquellos que reciben dosis elevadas o frecuentes de fenitoína por vía intravenosa.
En los adultos mayores, se presentan múltiples cambios fisiológicos que alteran la respuesta vascular y tisular frente a agentes irritantes. Con la edad, el sistema vascular experimenta un progresivo endurecimiento de las paredes arteriales, disminución del calibre capilar funcional y reducción de la perfusión tisular, lo que favorece una respuesta inadecuada frente a sustancias de alta alcalinidad o toxicidad local, como la fenitoína. Además, en estos pacientes es común la presencia de atrofia dérmica y disminución del tejido subcutáneo, factores que reducen la capacidad de amortiguación de los tejidos frente a la extravasación de fármacos.
El sexo femenino, por su parte, se ha asociado con mayor susceptibilidad, posiblemente debido a diferencias estructurales en la microcirculación y a la menor masa muscular en las extremidades, lo que puede facilitar la diseminación del fármaco extravasado en el espacio intersticial. Asimismo, se han propuesto factores hormonales y genéticos que podrían modular la respuesta inflamatoria o la integridad endotelial de forma distinta en mujeres.
La sepsis representa un estado clínico de inflamación sistémica severa, caracterizado por disfunción endotelial generalizada, aumento de la permeabilidad capilar y alteraciones en la coagulación. Estas condiciones hacen que los vasos sanguíneos sean más susceptibles a lesiones inducidas químicamente, como las que puede provocar la fenitoína intravenosa. La inflamación sistémica también puede exacerbar el daño local tras la extravasación del fármaco, favoreciendo el edema y el compromiso de la circulación tisular.
Por otro lado, la enfermedad vascular periférica compromete directamente la integridad del sistema circulatorio en las extremidades, disminuyendo la capacidad de respuesta del endotelio frente a agentes nocivos. La perfusión deficiente limita el aclaramiento local del fármaco y de sus excipientes tóxicos, prolongando el tiempo de exposición de los tejidos a sustancias potencialmente lesivas.
Los antecedentes de enfermedades crónicas debilitantes, como la diabetes mellitus, la insuficiencia renal o la insuficiencia cardíaca, también predisponen al desarrollo del síndrome. Estas patologías suelen asociarse a alteraciones microvasculares, neuropatías periféricas y estados de fragilidad tisular, que contribuyen a una menor tolerancia frente a agresiones químicas locales.
La administración de dosis elevadas o frecuentes de fenitoína intravenosa incrementa exponencialmente el riesgo de toxicidad local. La fenitoína, disuelta en una solución de alta alcalinidad con excipientes como el propilenglicol, ejerce un efecto cáustico sobre el endotelio vascular. Cuando se administra en grandes cantidades o en infusiones repetidas, la probabilidad de daño vascular, extravasación y reacción inflamatoria aumenta significativamente, facilitando la aparición de los signos clínicos característicos del síndrome.
Clínicamente, el síndrome del guante púrpura se manifiesta por una coloración azulada o violácea alrededor del sitio de infusión, acompañada de edema y dolor. Aunque en la mayoría de los casos la evolución es benigna con tratamiento conservador, en circunstancias más severas puede progresar hacia complicaciones como necrosis tisular, isquemia, compresión neurovascular o incluso síndrome compartimental, una urgencia médica que puede requerir intervención quirúrgica.
Tratamiento
La evolución clínica del síndrome del guante púrpura puede ser altamente variable, dependiendo de la extensión del daño vascular y tisular, así como de la rapidez con la que se identifique y se maneje la reacción adversa. En la mayoría de los casos reportados en la literatura médica, especialmente aquellos clasificados como leves, se ha documentado una recuperación progresiva con la implementación de medidas de soporte no invasivas. Estas intervenciones tienen como objetivo principal mitigar el daño local, promover la reabsorción del edema, aliviar el dolor y prevenir la progresión de la lesión.
La primera y más importante acción terapéutica consiste en la suspensión inmediata de la administración intravenosa de fenitoína al primer signo de reacción local. Dado que la presencia continua del agente irritante en la circulación o en el espacio intersticial podría agravar la lesión, interrumpir su infusión reduce la exposición tisular a la sustancia cáustica y previene una mayor extravasación. Posteriormente, la elevación del miembro comprometido favorece el retorno venoso y linfático, disminuyendo la presión intersticial y facilitando el drenaje de líquidos acumulados. Esta medida es especialmente útil para reducir el edema, que es uno de los signos más prominentes del síndrome.
La aplicación local de calor o frío también ha mostrado cierto beneficio, dependiendo del momento clínico y del juicio médico. El frío puede utilizarse en fases muy tempranas para inducir vasoconstricción, lo que limitaría la extravasación adicional del fármaco. Sin embargo, en fases más avanzadas, el calor superficial puede ser preferido, ya que promueve la vasodilatación y mejora la perfusión sanguínea en los tejidos comprometidos, lo que podría acelerar la resolución del proceso inflamatorio. Estas medidas conservadoras, aplicadas de forma oportuna, han demostrado en varios casos permitir una recuperación completa en un lapso que varía entre algunos días y varias semanas, sin secuelas funcionales significativas.
No obstante, cuando el síndrome del guante púrpura progresa a una forma más severa, caracterizada por síntomas como dolor desproporcionado, rigidez del miembro, pérdida de la función motora o sensitiva, disminución de pulsos periféricos o signos clínicos de isquemia, el manejo médico debe ser más agresivo. En estos escenarios, la acumulación de líquido y la inflamación dentro de los compartimentos musculares cerrados de la extremidad pueden generar un aumento significativo de la presión intracompartimental. Esta situación puede derivar en un síndrome compartimental, una urgencia quirúrgica que compromete de manera aguda la perfusión tisular y amenaza la viabilidad del miembro.
Ante la sospecha clínica de este desenlace, la intervención quirúrgica mediante fasciotomía puede ser indispensable. Esta técnica consiste en la incisión de las fascias que rodean los compartimentos musculares, con el propósito de liberar la presión acumulada, restaurar el flujo sanguíneo adecuado y evitar la necrosis muscular o la pérdida irreversible de la función neurológica. Si bien es un procedimiento invasivo, su realización oportuna puede marcar la diferencia entre la recuperación funcional del miembro y la aparición de complicaciones permanentes, como contracturas, amputación o disfunción motora severa.

Fuente y lecturas recomendadas:
- Perez Del Nogal, G., Rodaniche, A., & Saragadam, S. D. (2022). Purple Glove Syndrome: Recognizing a Rare Complication of Intravenous Phenytoin. Cureus, 14(4), e23958. https://doi.org/10.7759/cureus.23958
- Dogra, P. M., Pramanik, S. K., & Jana, S. (2016). Purple glove syndrome. Indian journal of dermatology, venereology and leprology, 82(1), 107–108. https://doi.org/10.4103/0378-6323.172908
Síguenos en X: @el_homomedicus y @enarm_intensivo Síguenos en instagram: homomedicus y en Treads.net como: Homomedicus