El shock se produce cuando la tasa de flujo sanguíneo arterial es inadecuada para satisfacer las necesidades metabólicas de los tejidos. Esto da como resultado hipoxia regional y posterior acidosis láctica del metabolismo anaeróbico en los tejidos periféricos, así como un eventual daño y fracaso de los órganos finales.
La clasificación del shock se basa principalmente en la causa subyacente y en las respuestas fisiopatológicas del cuerpo, permitiendo así un enfoque terapéutico específico y efectivo.
La utilidad de clasificar el shock radica en la capacidad para guiar rápidamente las decisiones terapéuticas críticas. Cada tipo de shock tiene una etiología distinta que requiere un enfoque específico para restaurar la perfusión tisular adecuada y evitar el deterioro orgánico irreversible.
Existen varias clasificaciones comúnmente utilizadas para el shock, que incluyen:
Shock Hipovolémico:
- Pérdida de volumen
- Quemaduras
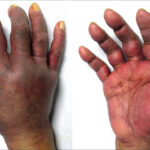
- Pérdida de integridad cutánea (necrólisis epidérmica tóxica)
- Vómitos
- Diarrea
- Estados hiperosmolares (por ejemplo, estado hiperosmolar hiperglucémico)
- Tercer espacio (por ejemplo, ascitis, pancreatitis)
- Disminución de la ingesta
- Pérdida de sangre
- Hemorragia traumática
- Exanguinación
- Hemotórax
- Hemoperitoneo
- Fractura (fémur y pelvis)
- Hemorragia no traumática
- Sangrado gastrointestinal
- Ruptura de AAA (aneurisma aórtico abdominal)
- Ruptura de embarazo ectópico
Shock Cardiogénico:
- Enfermedad miocárdica
- Infarto ventricular izquierdo o derecho
- Miocardiopatía dilatada
- Mecánico
- Disritmia
- Bradicardias y bloqueos
- Taquicardias
Shock Obstructivo:
- Neumotórax a tensión
- Enfermedad pericárdica
- Taponamiento cardíaco
- Pericarditis constrictiva
- EP (embolia pulmonar) de alto riesgo (masiva)
- Hipertensión pulmonar severa
- Auto-PEEP (presión positiva al final de la espiración) por ventilación mecánica
Shock Distributivo (Vasodilatador):
- Shock anafiláctico
- Shock séptico
- Shock neurogénico
- Vasodilatación inducida por fármacos
- Insuficiencia adrenal
Shock hipovolémico
El shock hipovolémico es una condición médica grave y potencialmente mortal que se caracteriza por una disminución significativa del volumen sanguíneo circulante en el cuerpo humano. Esta pérdida de volumen puede ocurrir por diversas causas, todas las cuales comparten el denominador común de reducir la cantidad total de líquido circulante y, por lo tanto, comprometer la perfusión adecuada de los tejidos y órganos vitales.
Una de las principales causas de shock hipovolémico es la pérdida de volumen sanguíneo debido a hemorragias importantes. Las hemorragias pueden ser traumáticas, como en el caso de accidentes automovilísticos que resultan en hemotórax o hemoperitoneo, o no traumáticas, como sangrado gastrointestinal por úlceras pépticas o ruptura de aneurismas aórticos abdominales. Estas situaciones pueden provocar una pérdida rápida y significativa de sangre, lo que reduce el volumen circulante y disminuye la presión arterial.
Otra causa frecuente de shock hipovolémico son las quemaduras extensas. Las quemaduras severas pueden provocar pérdida de líquidos a través de la piel dañada, exacerbando la hipovolemia y aumentando el riesgo de shock.
Además de las hemorragias y las quemaduras, otras condiciones médicas pueden contribuir al desarrollo de shock hipovolémico. La pérdida de integridad cutánea en condiciones como la necrólisis epidérmica tóxica resulta en una pérdida significativa de fluidos corporales y electrolitos. Asimismo, vómitos persistentes, diarrea severa y estados hiperosmolares, como el estado hiperosmolar hiperglucémico en pacientes diabéticos descompensados, pueden causar deshidratación grave y precipitar el shock hipovolémico.
El tercer espacio es otra condición en la cual el líquido se desplaza fuera del espacio vascular y se acumula en cavidades como el abdomen (ascitis) o alrededor de órganos inflamados, como ocurre en la pancreatitis aguda. Esta redistribución del líquido reduce efectivamente el volumen circulante, exacerbando la hipovolemia y predisponiendo al paciente al shock.
Además de las pérdidas agudas de líquido, la disminución crónica de la ingesta, ya sea por causas médicas o sociales, puede llevar a una disminución progresiva del volumen sanguíneo, predisponiendo al individuo a desarrollar hipovolemia y eventualmente shock.
Shock cardiogénico
El shock cardiogénico es una condición crítica y potencialmente mortal que se caracteriza por una disminución significativa en la función de bombeo del corazón, lo cual resulta en una perfusión tisular inadecuada y un suministro insuficiente de oxígeno a los tejidos del cuerpo. Esta disfunción cardiaca puede tener diversas causas, cada una de las cuales compromete la capacidad del corazón para mantener un adecuado gasto cardíaco y presión arterial suficiente.
Una de las causas más comunes de shock cardiogénico es la enfermedad miocárdica aguda, como el infarto de miocardio. El infarto agudo de miocardio, especialmente si afecta al ventrículo izquierdo o derecho de manera extensa, puede comprometer severamente la función contráctil del corazón y llevar al desarrollo de shock cardiogénico.
Además del infarto de miocardio, la miocardiopatía dilatada es otra condición que puede predisponer al shock cardiogénico. Esta enfermedad provoca un agrandamiento y debilitamiento de las cavidades del corazón, reduciendo su capacidad para bombear sangre de manera efectiva.
Los problemas mecánicos del corazón también pueden desencadenar shock cardiogénico. Por ejemplo, una válvula cardíaca dañada, como en la regurgitación aórtica causada por disección aórtica o ruptura de músculo papilar por isquemia, puede comprometer la función valvular y resultar en una insuficiencia cardíaca aguda.
Las complicaciones estructurales del corazón, como la ruptura de un aneurisma ventricular o septal, también pueden llevar al desarrollo de shock cardiogénico al comprometer la integridad de las paredes del corazón y reducir la eficiencia de la contracción cardíaca.
Además de las causas mecánicas y estructurales, las disritmias cardíacas son otro factor importante en el shock cardiogénico. Tanto las bradicardias graves y los bloqueos cardiacos que reducen el ritmo cardíaco, como las taquicardias severas que comprometen el llenado ventricular adecuado, pueden resultar en una disminución significativa del gasto cardíaco y contribuir al desarrollo de shock cardiogénico.
Shock obstructivo
El shock obstructivo es una condición médica crítica caracterizada por una obstrucción mecánica al flujo sanguíneo dentro del sistema cardiovascular o pulmonar, lo que compromete el adecuado llenado cardíaco y la función circulatoria. Esta obstrucción puede ocurrir en diversas localizaciones dentro del sistema cardiovascular y respiratorio, cada una con sus propias implicaciones fisiopatológicas y clínicas.
Una causa importante de shock obstructivo es el neumotórax a tensión. Esta condición ocurre cuando el aire ingresa en el espacio pleural y se acumula bajo presión, comprimiendo los vasos sanguíneos y el tejido pulmonar sano. La compresión resultante reduce el retorno venoso al corazón, disminuyendo así el volumen de sangre que el corazón puede bombear efectivamente y llevando al desarrollo de shock.
Las enfermedades pericárdicas también pueden provocar shock obstructivo, principalmente a través del taponamiento cardíaco. El taponamiento cardíaco se desarrolla cuando el líquido, generalmente sangre o fluido pericárdico, se acumula en el espacio pericárdico alrededor del corazón y comprime las cámaras cardíacas. Esto impide que el corazón se llene adecuadamente durante el ciclo cardíaco, reduciendo así el gasto cardíaco y provocando signos de shock.
Otra manifestación de enfermedad pericárdica que puede causar shock obstructivo es la pericarditis constrictiva. Esta condición se caracteriza por una inflamación crónica del pericardio que lleva a la formación de tejido fibroso y a la rigidez del pericardio. Esta rigidez puede restringir el llenado cardíaco durante la diástole, disminuyendo el volumen de sangre que el corazón puede bombear hacia la circulación sistémica.
La embolia pulmonar de alto riesgo, también conocida como embolia pulmonar masiva, es otra causa significativa de shock obstructivo. Esta condición se produce cuando un coágulo sanguíneo grande bloquea una arteria pulmonar principal o múltiples arterias pulmonares, impidiendo el flujo sanguíneo hacia los pulmones para la oxigenación adecuada. La reducción drástica en el intercambio de gases y en la capacidad de bombeo del corazón puede llevar rápidamente al deterioro hemodinámico y al shock.
La hipertensión pulmonar severa también puede conducir al shock obstructivo. En este caso, la presión arterial elevada en la circulación pulmonar ejerce una carga adicional sobre el ventrículo derecho del corazón, comprometiendo su capacidad para bombear sangre eficazmente hacia los pulmones y el resto del cuerpo.
Finalmente, el auto-PEEP generado por la ventilación mecánica puede causar una forma de shock obstructivo. El auto-PEEP ocurre cuando la presión positiva al final de la espiración no se disipa completamente antes de que comience el siguiente ciclo respiratorio, lo que puede reducir el retorno venoso al corazón y disminuir el volumen sistólico, afectando así el gasto cardíaco y la perfusión tisular.
Shock distributivo
El shock distributivo, también conocido como shock vasodilatador, es una condición clínica grave caracterizada por una redistribución anormal del flujo sanguíneo dentro del sistema cardiovascular. Este tipo de shock se diferencia de otros por la presencia de vasodilatación generalizada y una disminución en la resistencia vascular periférica, lo que resulta en una distribución ineficaz del volumen sanguíneo circulante y una disminución del retorno venoso al corazón.
Una de las causas más comunes de shock distributivo es el shock anafiláctico, una reacción alérgica severa que desencadena la liberación masiva de mediadores inflamatorios, como histamina, bradicinina y prostaglandinas. Estos mediadores provocan una vasodilatación generalizada y aumento de la permeabilidad capilar, lo que resulta en una rápida caída de la presión arterial y compromiso hemodinámico.
El shock séptico es otra forma importante de shock distributivo, causado por una respuesta inflamatoria sistémica exagerada frente a una infección bacteriana, fúngica o viral. Los patógenos y sus productos (endotoxinas y exotoxinas) activan los sistemas inmunológicos del huésped, desencadenando una cascada de eventos que incluyen la producción de citocinas proinflamatorias. Estas citocinas inducen una vasodilatación sistémica y alteran la permeabilidad vascular, lo que conduce a una disminución del retorno venoso y una caída en la presión arterial.
El shock neurogénico se produce cuando hay una pérdida repentina de tono simpático debido a lesiones de la médula espinal, anestesia espinal o lesiones del sistema nervioso central. Esta pérdida de tono simpático conduce a una vasodilatación periférica generalizada, reduciendo la resistencia vascular y disminuyendo la presión arterial efectiva.
La vasodilatación inducida por fármacos puede también provocar shock distributivo, especialmente en casos de intoxicación por medicamentos que actúan como vasodilatadores directos, como algunos agentes antihipertensivos o relajantes musculares. La dilatación de los vasos sanguíneos periféricos reduce la resistencia vascular total y puede llevar a una hipotensión severa y compromiso circulatorio.
Finalmente, la insuficiencia adrenal, particularmente en su forma aguda llamada crisis suprarrenal, puede causar shock distributivo. En esta condición, hay una deficiencia aguda de cortisol, una hormona esencial para mantener la presión arterial y la respuesta vascular adecuada. La falta de cortisol conduce a una vasodilatación periférica significativa y una disminución en la capacidad del organismo para responder eficazmente al estrés fisiológico.

Fuentes y lecturas recomendadas:
- Khanna A et al; ATHOS-3 Investigators. Angiotensin II for the treatment of vasodilatory shock. N Engl J Med. 2017;377:419. [PMID: 28528561]
- Mathew R et al. Milrinone as compared with dobutamine in the treatment of cardiogenic shock. N Engl J Med. 2021;385:516. [PMID: 34347952]
- Meyhoff TS et al. Restriction of intravenous fluid in ICU patients with septic shock. N Engl J Med. 2022;386:2459. [PMID: 35709019]
- Sevransky JE et al; VICTAS Investigators. Effect of vitamin C, thiamine, and hydrocortisone on ventilator- and vasopressor-free days in patients with sepsis: the VICTAS randomized clinical trial. JAMA. 2021;325:742. [PMID: 33620405]
- Evans L et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med. 2021;47:1181. [PMID: 34599691]
- Gando S et al; Japanese Association for Acute Medicine (JAAM) Sepsis Prognostication in Intensive Care Unit and Emergency Room (SPICE) (JAAM SPICE) Study Group. The SIRS criteria have better performance for predicting infection than qSOFA scores in the emergency department. Sci Rep. 2020;10:8095. [PMID: 32415144]
- Hammond DA et al. Balanced crystalloids versus saline in critically ill adults: a systematic review with meta-analysis. Ann Pharmacother. 2020;54:5. [PMID: 31364382]