Las infecciones por Coxsackievirus causan una variedad de síndromes clínicos debido a las características biológicas de estos virus y su capacidad para afectar diferentes órganos y tejidos dentro del cuerpo humano. Los Coxsackievirus son parte de la familia Picornaviridae y se incluyen en el grupo de los enterovirus, un grupo de virus que también comprende al virus poliomielítico y al virus de la hepatitis A. Estas infecciones son más prevalentes durante los meses de verano, fenómeno que se ha asociado con la mayor incidencia de enfermedades transmitidas por vías fecales-orales, ya que los enterovirus pueden encontrarse en el agua y en alimentos contaminados, lo que facilita su propagación.
Los Coxsackievirus se dividen en dos grupos principales: el grupo A y el grupo B. Esta clasificación puede realizarse de dos maneras principales: mediante el análisis serológico, que consiste en la identificación de anticuerpos específicos generados por el sistema inmunológico del huésped frente a cada tipo de virus, o bien mediante un ensayo biológico realizado en ratones, conocido como el bioensayo en ratón. El grupo A es conocido por producir afecciones más superficiales y con síntomas menos graves, mientras que el grupo B puede estar asociado con manifestaciones clínicas más serias.
Dentro de estos dos grupos, se han identificado más de 50 serotipos distintos de Coxsackievirus, lo que contribuye a la amplia diversidad de síndromes clínicos que pueden provocar. Cada serotipo posee una especificidad en cuanto a los tejidos que infecta, lo que explica por qué los Coxsackievirus pueden causar una amplia gama de manifestaciones clínicas, desde enfermedades leves como exantemas hasta afecciones más graves que afectan a órganos vitales.
Los Coxsackievirus poseen una afinidad particular por las células del tracto gastrointestinal y del sistema respiratorio. Al ingresar al cuerpo humano, estos virus se replican inicialmente en el intestino, de donde pueden diseminarse hacia otros órganos a través del torrente sanguíneo, un proceso conocido como viremia. La capacidad del virus para infectar y replicarse en múltiples tejidos es uno de los factores que subyace a la diversidad de enfermedades que puede inducir.
La diversidad de los síntomas causados por las infecciones por Coxsackievirus se debe en parte a los factores biológicos relacionados con el virus y el huésped. El tropismo viral, o la afinidad de los virus por ciertos tejidos, varía según el serotipo y la respuesta inmunológica del individuo infectado. Además, el sistema inmunológico del huésped juega un papel crucial en la manifestación de la enfermedad; por ejemplo, un individuo con un sistema inmunológico debilitado o con una inmunidad preexistente insuficiente puede presentar una forma más grave de la enfermedad.
Asimismo, la interacción entre los factores ambientales, como las condiciones de higiene, la calidad del agua y los alimentos, y la estación del año (en particular durante los meses de verano, cuando las condiciones de propagación del virus son más favorables) puede contribuir al aumento de la prevalencia de estas infecciones.
El sistema inmunológico del huésped responde a la infección por Coxsackievirus mediante la producción de anticuerpos específicos contra los serotipos infectantes. Sin embargo, debido a la alta variabilidad genética de estos virus, la inmunidad adquirida frente a un serotipo específico no confiere protección frente a otros serotipos, lo que facilita la propagación continua del virus en la población.
En términos de tratamiento, la mayoría de las infecciones por Coxsackievirus son autolimitadas y no requieren un tratamiento específico. Sin embargo, en los casos más graves, como en la miocarditis o la meningitis, pueden ser necesarios cuidados intensivos y terapia antiviral específica.
Manifestaciones clínicas
Los síndromes clínicos asociados con la infección por coxsackievirus son gripe de verano; herpangina; pleurodinia epidémica; meningitis aséptica y otros síndromes neurológicos; pericarditis aguda no específica; miocarditis; enfermedad mano-pie-boca; conjuntivitis epidémica; y otros síndromes.
1. Gripe de verano (tipos A y B)
La gripe de verano es una enfermedad febril que afecta principalmente a niños y que tiene una duración de 1 a 4 días. Generalmente, los síntomas incluyen una infección leve del tracto respiratorio superior, como rinorrea o faringitis, aunque pueden ser relativamente benignos. La fiebre es el principal síntoma, acompañada de malestar general. A pesar de la presencia de síntomas respiratorios menores, la evolución de la enfermedad es rápida y generalmente no provoca complicaciones graves.
2. Herpangina (tipos A2–6, 10; B3)
La herpangina se caracteriza por un inicio repentino de fiebre, que en algunos casos puede alcanzar los 40.6°C, y que a veces se acompaña de convulsiones febrilmente. Además, los pacientes pueden presentar cefalea, mialgia y vómitos. Un hallazgo clave en esta afección es el dolor de garganta, que suele ir acompañado de petequias o pápulas en el paladar blando, las cuales posteriormente ulceran en aproximadamente 3 días y finalmente sanan. La herpangina es una enfermedad autolimitada, por lo que el tratamiento generalmente es sintomático, centrado en la reducción de la fiebre y el alivio del dolor.
3. Pleurodinia epidémica (enfermedad de Bornholm) (tipos B1–5)
La pleurodinia epidémica se caracteriza por un dolor pleurítico agudo, localizado en la región torácica, y que se acentúa con la respiración profunda o los movimientos del torso. A este dolor se asocia con sensibilidad, hiperestesia y edema muscular en la zona de inserción del diafragma. Otros síntomas comunes son cefalea, dolor de garganta, malestar general, náuseas y fiebre. Aunque en menos del 10% de los casos se presentan complicaciones como orquitis (inflamación de los testículos) o meningitis aséptica, la enfermedad suele durar entre 4 y 6 días en la mayoría de los pacientes. Este síndrome es típicamente benigno y se resuelve sin tratamiento antiviral específico.
4. Meningitis aséptica y otros síndromes neurológicos (tipos A y B)
La meningitis aséptica es una de las complicaciones más graves asociadas a la infección por coxsackievirus. Se manifiesta con fiebre, cefalea intensa, náuseas, vómitos, rigidez en el cuello, somnolencia y leucocitosis en el líquido cefalorraquídeo (LCR) sin alteraciones bioquímicas. En algunas ocasiones, se han descrito clusters de meningitis por el grupo B, especialmente por el subgrupo B5, que afectan a grupos pediátricos. Además, pueden ocurrir encefalitis focal y mielitis transversa asociadas a la infección por el grupo A, mientras que la mielitis flácida aguda ha sido reportada en India en pacientes infectados con el grupo B. En algunos casos, se ha observado encefalitis diseminada y mielitis flácida aguda, afecciones que, aunque raras, son graves y requieren un manejo especializado.
5. Pericarditis aguda no específica (tipos B)
La pericarditis aguda no específica es una afección que se caracteriza por un inicio súbito de dolor torácico anterior, generalmente agravado con la inspiración y en la posición supina. Este dolor es el síntoma principal y se asocia con fiebre, mialgia, cefalea y un roce pericárdico, que se detecta con la auscultación cardíaca en las primeras etapas de la enfermedad. El roce pericárdico, que se describe como un sonido áspero y chirriante, es a menudo transitorio, pero su presencia es un hallazgo característico. En la mayoría de los casos, los estudios de imagen revelan evidencia de un derrame pericárdico, es decir, la acumulación de líquido en el espacio pericárdico, lo que aumenta la presión sobre el corazón y puede interferir con su función. En algunos pacientes, se observa un pulso paradójico, que es una disminución anormal de la presión arterial durante la inspiración. Además, el electrocardiograma frecuentemente muestra alteraciones típicas de la pericarditis, como la elevación difusa del segmento ST. Aunque la mayoría de los casos se resuelven sin complicaciones graves, las recaídas pueden ocurrir, especialmente en aquellos pacientes con un sistema inmunológico comprometido o en aquellos que no responden adecuadamente al tratamiento inicial.
6. Miocarditis (tipos B1–5)
La miocarditis es una inflamación del músculo cardíaco que puede tener consecuencias graves dependiendo de su gravedad y la rapidez del diagnóstico. En el caso de las infecciones por coxsackievirus tipo B, se ha observado que la miocarditis es responsable de la insuficiencia cardíaca en el período neonatal, lo que sugiere que la infección intrauterina puede desencadenar una inflamación en el corazón del feto. De manera más general, más del 20% de los casos de miocarditis en adultos y en cardiomiopatía dilatada están relacionados con infecciones por el grupo B de coxsackievirus, especialmente el subgrupo B3. Esta condición provoca una respuesta inflamatoria en el tejido cardíaco que puede interferir con la función normal del corazón, llevando a una disfunción cardíaca que varía desde síntomas leves de insuficiencia cardíaca hasta cuadros graves de falla multiorgánica. El diagnóstico temprano y el tratamiento adecuado son fundamentales para evitar daños permanentes en el corazón.
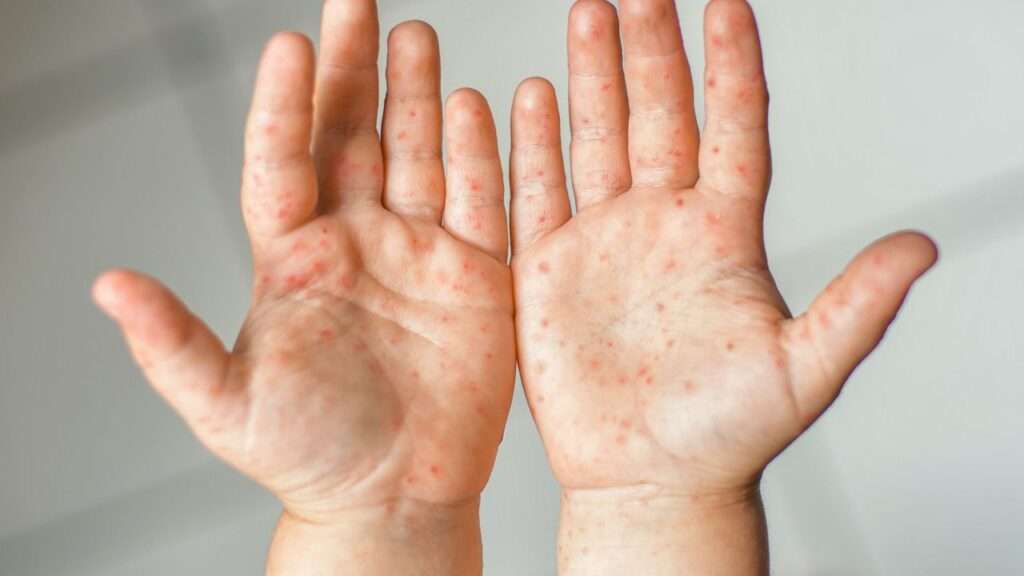
7. Enfermedad mano-pie-boca (tipos A5, 6, 10, 12, 16 y B5)
La enfermedad mano-pie-boca es una infección viral que puede presentarse de forma epidémica, especialmente en áreas donde las condiciones de hacinamiento y falta de higiene favorecen su propagación. Esta enfermedad se caracteriza por la aparición de estomatitis (inflamación de las mucosas orales) acompañada de una erupción vesicular en las manos y los pies, que puede extenderse a otras áreas del cuerpo. Además, en algunos casos, se observan alteraciones en las uñas, como distrofias ungueales y onicomadesis, que es la caída de las uñas. La enfermedad suele ser autolimitada y en la mayoría de los casos, los síntomas son leves, aunque algunos pacientes pueden experimentar fiebre alta, una duración prolongada de la enfermedad y manifestaciones cutáneas más graves. Además de los coxsackievirus, otros enterovirus como el enterovirus 71 y el enterovirus 33 también son causantes de la enfermedad, siendo el enterovirus 71 el responsable de formas más graves de la enfermedad, incluidas complicaciones neurológicas como la encefalitis. Por otro lado, la infección por el serotipo A16 suele presentar un cuadro clínico más leve, y el tipo A6, aunque puede tener manifestaciones atípicas, también es en general autolimitado. En raros casos, se han reportado muertes en programas de vigilancia en China, donde se han identificado patrones recombinantes entre los coxsackievirus y los echovirus, lo que sugiere una mayor complejidad en la evolución de estas cepas virales y su potencial para generar formas más severas de la enfermedad.
8. Conjuntivitis epidémica
La conjuntivitis epidémica hemorrágica aguda es una infección ocular altamente contagiosa que se asocia principalmente con el enterovirus 70, pero también con la variante A24 del coxsackievirus. Este tipo de conjuntivitis se caracteriza por un inicio rápido y la aparición de síntomas severos como enrojecimiento ocular, dolor, secreción y, en casos más graves, hemorragias en la conjuntiva, lo que le da el nombre de “hemorrágica”. Se ha observado una mayor prevalencia de brotes de esta enfermedad en áreas tropicales, donde las condiciones de hacinamiento y contacto cercano favorecen su transmisión, como en el sur de China, Pakistán, el sur de Sudán, las Comoras, Uganda, Cuba y Tailandia. Este fenómeno es especialmente relevante en las regiones donde los climas cálidos y húmedos crean un ambiente propicio para la propagación del virus.
Además de su vínculo con los brotes epidémicos de conjuntivitis, la variante A24 del coxsackievirus también se ha implicado en la endotelitis corneal, una condición que afecta la capa más interna de la córnea. Esta afección ha sido reportada como una complicación posterior a la cirugía de cataratas, en donde el virus podría inducir una inflamación del endotelio corneal, lo que afecta la función visual. Si bien esta complicación es poco común, subraya la capacidad del coxsackievirus para involucrarse en una variedad de trastornos oculares, algunos de los cuales requieren tratamiento médico específico para prevenir daño a largo plazo en la visión.
9. Encefalomielitis miálgica/síndrome de fatiga crónica
El síndrome de encefalomielitis miálgica, también conocido como síndrome de fatiga crónica, se ha asociado en ciertos estudios con el Borna disease virus, un agente viral distinto del coxsackievirus. Sin embargo, investigaciones posteriores que intentaron identificar vínculos entre este síndrome y otros enterovirus, así como con virus como el herpes y los parvovirus, no han demostrado ninguna relación consistente. Aunque la literatura científica aún no establece una conexión clara entre el coxsackievirus y el síndrome de fatiga crónica, algunos estudios han sugerido que infecciones virales, en general, podrían jugar un papel en la génesis de este trastorno, que se caracteriza por una fatiga profunda y persistente que no mejora con el descanso, así como otros síntomas como dolores musculares, alteraciones cognitivas y problemas del sueño. La etiología de esta enfermedad sigue siendo un tema de investigación activa, y los enterovirus, en general, continúan siendo considerados como posibles contribuyentes, aunque no se ha establecido una causalidad definitiva.
10. Otros síndromes asociados con infecciones por coxsackievirus
Las infecciones por coxsackievirus, especialmente los tipos del grupo B, están implicadas en una amplia gama de síndromes clínicos, algunos de los cuales son poco frecuentes pero graves. Entre estos se incluyen:
-
Rabdomiolisis: La destrucción del tejido muscular, que libera proteínas como la mioglobina en la sangre, es una complicación que puede ocurrir en el contexto de infecciones virales, incluidas aquellas causadas por coxsackievirus. Esta condición puede llevar a insuficiencia renal aguda si no se trata adecuadamente.
-
Hepatitis neonatal fulminante: Aunque rara, la hepatitis aguda en neonatos, inducida por coxsackievirus, es una condición grave que puede comprometer la función hepática en el recién nacido, provocando insuficiencia hepática y, en algunos casos, la necesidad de un trasplante hepático.
-
Pancreatitis con hepatitis concomitante y miocarditis (tipo A4): Las infecciones por el coxsackievirus tipo A4 han sido asociadas con la aparición de pancreatitis junto con hepatitis y miocarditis, lo que subraya la capacidad del virus para afectar múltiples órganos simultáneamente.
-
Glomerulopatía (infecciones por el grupo B): Las infecciones por el grupo B de coxsackievirus pueden inducir alteraciones renales, como glomerulonefritis, que afectan la función renal y pueden llevar a complicaciones graves si no se tratan.
-
Onicomadesis (tipo B1): Este trastorno se caracteriza por la pérdida de las uñas, que se ha observado en algunos pacientes con infecciones por el coxsackievirus B1.
-
Linfocitosis hemofagocítica neonatal (tipo B1): Esta rara afección se presenta con una reacción inmunitaria descontrolada en el recién nacido, lo que puede llevar a daño orgánico generalizado y a una respuesta inflamatoria excesiva.
-
Diabetes mellitus tipo 1 y 2 (principalmente infecciones por el grupo B): Aunque la causalidad aún no está completamente establecida, se ha sugerido que las infecciones por coxsackievirus, particularmente las del grupo B, podrían tener un papel en el desarrollo de diabetes mellitus, especialmente en los tipos autoinmunes (tipo 1).
-
Enfermedades tiroideas (grupo B4): Algunos estudios han propuesto una posible relación entre las infecciones por coxsackievirus y trastornos tiroideos, aunque la evidencia no es concluyente.
-
Síndrome de Sjögren primario y infarto de miocardio (miocarditis aguda): En investigaciones recientes, se ha sugerido que las infecciones por el grupo B de coxsackievirus podrían tener un papel patogénico en el síndrome de Sjögren, una enfermedad autoinmune que afecta las glándulas exocrinas, y en la miocarditis aguda, que puede llevar a complicaciones cardiovasculares graves.
Una de las observaciones más interesantes proviene de un informe de endocarditis infecciosa confirmada, atribuida al coxsackievirus B2, en un paciente con un parche cardíaco protésico utilizado para reparar un defecto septal atrioventricular en un niño. Este caso sugiere que las etiologías virales deben ser consideradas incluso en casos de endocarditis infecciosa en los que los cultivos resulten negativos, especialmente en pacientes que han pasado por intervenciones quirúrgicas cardíacas. Esto resalta la importancia de no descartar posibles infecciones virales como causa de endocarditis, particularmente en situaciones de cirugía cardíaca, donde los métodos convencionales de diagnóstico pueden no detectar todos los agentes patógenos involucrados.
Exámenes diagnósticos
Los estudios de laboratorio rutinarios no suelen revelar anormalidades características en las infecciones por coxsackievirus, lo que dificulta el diagnóstico basado únicamente en análisis bioquímicos o hematológicos convencionales. En la mayoría de los casos, los parámetros sanguíneos, como el recuento de glóbulos blancos o los niveles de enzimas hepáticas, no muestran alteraciones significativas que permitan diferenciar estas infecciones de otras de origen viral o bacteriano. Sin embargo, durante la fase de convalecencia, es común la aparición de anticuerpos neutralizantes específicos, lo que indica que el sistema inmunológico ha comenzado a responder al patógeno. La detección de estos anticuerpos puede ser útil para confirmar una infección pasada, aunque no es un método adecuado para el diagnóstico temprano de la enfermedad.
El diagnóstico microbiológico de la infección por coxsackievirus implica la identificación del virus a través de métodos de aislamiento viral, que, si bien son específicos, requieren de procedimientos complejos y costosos. El virus puede ser aislado a partir de muestras de lavado faríngeo o de heces, que se inoculan en ratones lactantes, un modelo animal sensible a este tipo de infecciones. Sin embargo, este enfoque tiene varias limitaciones, entre ellas el alto costo, la necesidad de personal especializado y el tiempo considerable requerido para obtener resultados, ya que el cultivo viral puede tardar varios días en arrojar una respuesta.
En los últimos años, la reacción en cadena de la polimerasa (PCR) ha emergido como una herramienta diagnóstica más rápida y accesible para la detección de infecciones por enterovirus, incluidos los coxsackievirus. Esta prueba molecular es capaz de identificar el material genético del virus (RNA viral) en las muestras clínicas, lo que la convierte en una alternativa valiosa para el diagnóstico, especialmente en casos de meningitis viral. Aunque la PCR proporciona un diagnóstico más rápido que el cultivo viral, tiene la limitación de no poder identificar el serotipo específico del virus, lo que puede ser importante en ciertos contextos epidemiológicos o clínicos. No obstante, la PCR sigue siendo una herramienta útil para confirmar la presencia del virus en el organismo, particularmente cuando se presentan síntomas como fiebre, cefalea, náuseas y signos neurológicos que sugieren una posible infección del sistema nervioso central.
Tratamiento y pronóstico
El tratamiento de las infecciones causadas por coxsackievirus generalmente se basa en el manejo sintomático, ya que la mayoría de las afecciones asociadas con este virus son benignas y autolimitadas. Es decir, los síntomas suelen resolverse por sí mismos sin necesidad de intervenciones terapéuticas complejas. Estas infecciones, como la enfermedad mano-pie-boca, la gripe veraniega, la herpangina y otras formas leves de enfermedad, no requieren tratamiento antiviral específico, ya que la respuesta inmunitaria del paciente es suficiente para resolver la infección en un período de tiempo relativamente corto.
Sin embargo, existen algunas excepciones notables, en las que las infecciones por coxsackievirus pueden evolucionar a formas más graves que requieren un manejo más intensivo. Estos casos incluyen la meningitis, la miocarditis, la pericarditis, la diabetes mellitus y otras enfermedades raras como la pancreatitis o los cuadros similares a la poliomielitis. Estas condiciones pueden generar complicaciones significativas y requieren tratamiento especializado y, en algunos casos, terapias específicas.
En cuanto al tratamiento antiviral, ha habido investigaciones sobre la efectividad de medicamentos como el pleconaril, un fármaco que muestra un potencial beneficio clínico en el tratamiento de la meningitis enteroviral. Dos ensayos controlados han mostrado que pleconaril puede reducir la duración y la gravedad de los síntomas en pacientes con meningitis causada por enterovirus, aunque el uso compasivo de este medicamento ha sido suspendido. Actualmente, los clínicos pueden ponerse en contacto con la empresa farmacéutica Schering Plough para obtener actualizaciones sobre la disponibilidad y el uso de este fármaco.
Por otro lado, se han reportado algunos casos anecdóticos en los que el uso de inmunoglobulina intravenosa (IVIG) ha demostrado ser exitoso en el tratamiento de enfermedades graves asociadas con el coxsackievirus. Esta terapia, que implica la administración de anticuerpos derivados de donantes humanos, puede ser útil en situaciones de enfermedad severa, como la miocarditis o la encefalitis, aunque la evidencia sobre su eficacia sigue siendo limitada y se necesita más investigación para confirmar su rol en el tratamiento de infecciones graves por coxsackievirus.
En cuanto a la prevención, se han desarrollado vacunas contra los agentes etiológicos más comunes en diversas regiones, como las vacunas para la enfermedad mano-pie-boca en China en 2016. Estas vacunas han mostrado un éxito considerable en la reducción de la incidencia de la enfermedad en áreas específicas. Sin embargo, la implementación de vacunas contra coxsackievirus presenta un desafío significativo debido a la circulación simultánea de múltiples serotipos de enterovirus en una misma región. Este hecho hace que las vacunas basadas en un solo agente, como aquellas dirigidas a un serotipo específico del coxsackievirus, sean relativamente ineficaces, ya que no protegen contra todos los serotipos que pueden estar en circulación al mismo tiempo. Este fenómeno resalta la complejidad de desarrollar una vacuna universal para el coxsackievirus, ya que cada serotipo presenta características antigénicas distintas que dificultan la creación de una respuesta inmune efectiva frente a todos los posibles agentes causantes de la infección.

Fuente y lecturas recomendadas:
- Hwang JH et al. Evaluation of viral infection as an etiology of ME/CFS: a systematic review and meta-analysis. J Transl Med. 2023;21:763. [PMID: 37898798]
- Yuan X et al. Recent advances in anti-coxsackievirus A16 viral drug research. Future Med Chem. 2023;15:97. [PMID: 36538291]
- Zhang X et al. Hand-foot-and-mouth disease-associated enterovirus and the development of multivalent HFMD vaccines. Int J Mol Sci. 2022;24:169. [PMID: 36613612]