La osificación intramembranosa constituye un mecanismo de formación ósea en el cual el tejido óseo surge de manera directa a partir del mesénquima embrionario, sin la intermediación de un molde cartilaginoso. Este proceso refleja una estrategia de diferenciación celular altamente coordinada, en la que señales moleculares, interacciones célula-matriz y cambios en el microambiente tisular conducen progresivamente a la generación de un tejido mineralizado funcional.
En las primeras etapas del desarrollo embrionario, aproximadamente hacia la octava semana de gestación, se observa en regiones específicas del mesénquima una concentración localizada de células mesenquimatosas. Estas células, que poseen un alto grado de plasticidad, migran y se agrupan en zonas predeterminadas, especialmente en aquellas que darán origen a los huesos planos del cráneo y la cara. Esta condensación celular no es un fenómeno aleatorio, sino el resultado de gradientes de factores de crecimiento, interacciones de adhesión celular y señales provenientes del entorno extracelular que delimitan con precisión los futuros centros de osificación.
Una vez establecidas estas condensaciones, las células mesenquimatosas comienzan a diferenciarse en células osteoprogenitoras. Este cambio de identidad celular está regulado por la activación de programas genéticos específicos, entre los cuales destaca la expresión del factor de transcripción conocido como CBFA1, también denominado RUNX2. Este factor es fundamental porque actúa como un regulador maestro de la osteogénesis, activando genes que codifican proteínas esenciales para la síntesis de la matriz ósea. Sin esta señalización, la diferenciación hacia osteoblastos no puede llevarse a cabo de manera adecuada.
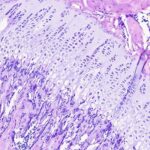
Las células osteoprogenitoras, una vez comprometidas con la línea osteogénica, se transforman en osteoblastos funcionales. Estas células adquieren la capacidad de sintetizar y secretar los componentes orgánicos de la matriz ósea, conocida como osteoide. Entre estos componentes predomina el colágeno tipo uno, que forma la estructura fibrilar básica, junto con proteínas no colágenas como la osteocalcina y las sialoproteínas óseas, que participan en la regulación de la mineralización. La secreción de osteoide ocurre inicialmente en el centro de los nódulos celulares, mientras que los osteoblastos se disponen en la periferia, organizando la expansión del tejido en formación.
A medida que el osteoide se acumula, comienza un proceso de mineralización en el cual se depositan cristales de hidroxiapatita dentro de la matriz orgánica. Este fenómeno transforma progresivamente el tejido blando en una estructura rígida. Durante este proceso, algunos osteoblastos quedan rodeados por la matriz que ellos mismos han producido, lo que induce su diferenciación en osteocitos. Estas células, ahora atrapadas en lagunas dentro del tejido mineralizado, desarrollan prolongaciones citoplasmáticas que se extienden a través de finos canales denominados canalículos. Este sistema de interconexión permite la comunicación intercelular y el intercambio de nutrientes, compensando la falta de vascularización directa en la matriz mineralizada.
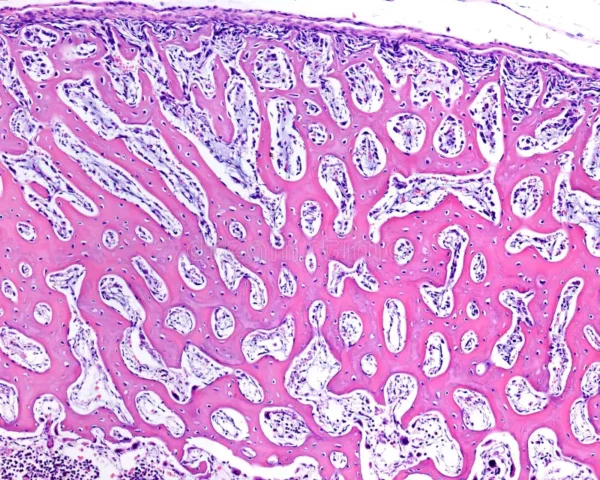
Conforme continúa la deposición de matriz, los osteocitos quedan cada vez más separados entre sí, pero mantienen su red funcional gracias a estas prolongaciones. Histológicamente, en esta etapa inicial, el tejido óseo presenta una organización irregular, formando espículas y cordones que se entrelazan. Esta disposición corresponde al llamado hueso inmaduro o hueso primario, caracterizado por una disposición desorganizada de las fibras de colágeno y una menor resistencia mecánica en comparación con el hueso maduro.
El crecimiento del tejido óseo en este contexto ocurre principalmente por aposición, es decir, mediante la adición de nuevas capas de matriz sobre superficies ya existentes. Las células osteoprogenitoras situadas en la periferia de las espículas se dividen activamente y generan nuevos osteoblastos, los cuales continúan depositando osteoide. Este mecanismo permite que las espículas aumenten de tamaño y se fusionen entre sí, formando una red tridimensional de trabéculas que define la arquitectura básica del hueso en desarrollo.
Entre estas trabéculas quedan espacios interconectados que inicialmente contienen tejido conjuntivo laxo y vasos sanguíneos. La invasión vascular es un elemento clave, ya que no solo aporta nutrientes y oxígeno, sino que también introduce células hematopoyéticas que darán origen a la médula ósea. Con el tiempo, estos espacios se organizan para constituir cavidades medulares funcionales.
A medida que el proceso avanza, el hueso inmaduro sufre una transformación progresiva mediante mecanismos de remodelación. En la periferia del hueso en desarrollo, la actividad osteoblástica se orienta hacia la formación de hueso compacto, caracterizado por una organización laminar más densa y resistente. En el interior, en cambio, persiste una estructura trabecular que da lugar al hueso esponjoso. Esta diferenciación estructural responde a las demandas mecánicas y metabólicas del tejido, optimizando tanto la resistencia como la ligereza del hueso.

Fuente y lecturas recomendadas:
- Ross, M. H. & Pawlina, W. (2020). Histología: texto y atlas: correlación con biología molecular y celular (8.ª ed.). Wolters Kluwer.
- Gartner, L. P. (2020). Textbook of Histology (5th ed.). Elsevier.
- Karp, G., Iwasa, J., & Marshall, W. (2019). Biología celular y molecular: conceptos y experimentos (8.ª ed.). McGraw-Hill Interamericana.