La trombocitopenia en el contexto de neoplasias hematológicas constituye una alteración hematológica compleja en la que confluyen mecanismos fisiopatológicos múltiples, con implicaciones clínicas que trascienden la simple disminución cuantitativa de plaquetas. Desde una perspectiva científica, este fenómeno no debe interpretarse únicamente como una consecuencia secundaria del proceso neoplásico o de su tratamiento, sino como una manifestación integrada de disrupción medular, alteraciones del microambiente hematopoyético y efectos farmacológicos acumulativos.
En las neoplasias hematológicas, tales como leucemias agudas, síndromes mielodisplásicos o linfomas con infiltración medular, la trombocitopenia puede originarse por reemplazo clonal del nicho hematopoyético. Este reemplazo reduce la capacidad funcional de los progenitores megacariocíticos, altera la arquitectura del estroma medular y modifica la señalización de citocinas esenciales para la trombopoyesis. Adicionalmente, la propia enfermedad puede inducir consumo periférico de plaquetas o disfunción inmunomediada, lo que agrava el déficit cuantitativo. A ello se suma el impacto iatrogénico de la quimioterapia intensiva, cuyo efecto citotóxico no es selectivo y compromete de manera significativa las líneas celulares de rápida proliferación, incluyendo los megacariocitos y sus precursores.
Cuando la trombocitopenia se vuelve persistente en este contexto, el riesgo clínico adquiere una dimensión crítica. La reducción sostenida del recuento plaquetario se asocia con un aumento exponencial del riesgo de hemorragias graves, incluidas hemorragias intracraneales o gastrointestinales, las cuales constituyen causas relevantes de morbilidad y mortalidad en estos pacientes. Diversos estudios clínicos han demostrado que la profundidad y duración de la trombocitopenia se correlacionan de manera directa con eventos hemorrágicos clínicamente significativos, especialmente cuando los recuentos se mantienen por debajo de umbrales críticos de hemostasia primaria.
Sin embargo, el manejo convencional presenta limitaciones importantes. La transfusión de plaquetas, aunque constituye el estándar de soporte inmediato, posee un efecto transitorio debido a la vida media corta de las plaquetas transfundidas y a su rápida eliminación en contextos inflamatorios o inmunológicos. Además, su eficacia es variable, particularmente en pacientes con refractariedad inmunológica o con activación endotelial sistémica. A esto se suman efectos adversos como reacciones febriles no hemolíticas, aloinmunización y, en algunos casos, riesgos infecciosos residuales. Por otra parte, la estrategia de reducir o retrasar la quimioterapia con el objetivo de mejorar la trombocitopenia puede comprometer el control tumoral, favoreciendo la progresión de la enfermedad o reduciendo la probabilidad de remisión completa, lo cual representa un dilema terapéutico fundamental en oncología hematológica.
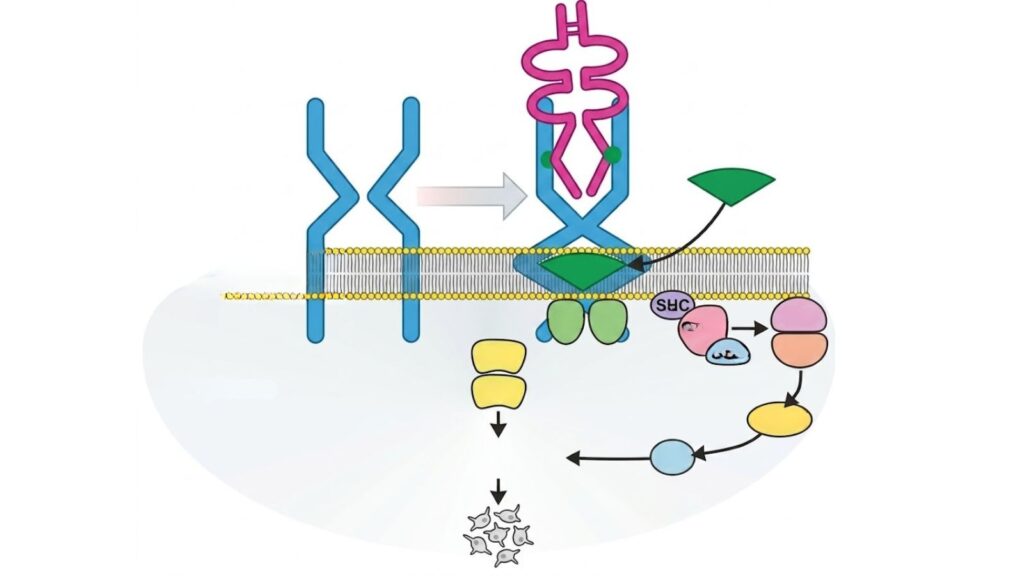
Los agonistas del receptor de trombopoyetina emergen como una estrategia farmacológica racional basada en la fisiología de la megacariopoyesis. Estos fármacos actúan mediante la activación del receptor c-MPL, presente en células progenitoras megacariocíticas y en megacariocitos maduros, lo que desencadena cascadas de señalización intracelular, principalmente a través de vías como JAK-STAT y MAPK. El resultado funcional es un aumento en la proliferación, diferenciación y maduración de megacariocitos, con incremento subsecuente en la producción de plaquetas circulantes. Este enfoque no sustituye las plaquetas periféricas, sino que estimula la trombopoyesis endógena, lo que representa una diferencia conceptual relevante frente a la transfusión.
Entre los fármacos disponibles destacan romiplostim, administrado por vía subcutánea, y los agonistas orales eltrombopag, avatrombopag y lusutrombopag. Aunque comparten el mismo objetivo farmacodinámico general, presentan diferencias estructurales y farmacocinéticas que influyen en su uso clínico. Romiplostim es una proteína de fusión peptídica, mientras que eltrombopag, avatrombopag y lusutrombopag son moléculas pequeñas no peptídicas con distinta afinidad por el receptor y diferente perfil de interacción con alimentos y cationes divalentes.
En cuanto a sus indicaciones aprobadas, estos agentes han demostrado eficacia en entidades como la púrpura trombocitopénica inmune crónica, la aplasia medular, la trombocitopenia asociada a enfermedad hepática en el contexto perioperatorio y la trombocitopenia relacionada con hepatitis en adultos. En estos escenarios, la evidencia clínica ha mostrado incrementos sostenidos del recuento plaquetario y reducción del riesgo hemorrágico, con un perfil de seguridad generalmente favorable en el seguimiento a largo plazo. No obstante, su uso no está exento de controversias, particularmente en relación con el riesgo teórico de trombosis o de estimulación clonal en enfermedades hematológicas subyacentes, aunque estos eventos son infrecuentes en los estudios disponibles.
En el contexto específico de la trombocitopenia inducida por quimioterapia, estos fármacos no cuentan con aprobación formal universal. Sin embargo, la evidencia emergente en tumores sólidos ha mostrado resultados clínicamente relevantes. Estudios clínicos y series prospectivas han demostrado que su administración puede incrementar de manera significativa los recuentos plaquetarios, reducir la necesidad de transfusiones y disminuir los retrasos o reducciones de dosis de quimioterapia, lo cual tiene implicaciones directas sobre la intensidad de tratamiento oncológico. Importante es destacar que, en estos estudios, no se ha observado un incremento significativo de toxicidad grave atribuible a los agonistas del receptor de trombopoyetina, lo que sugiere un perfil de seguridad aceptable en este contexto.
En escenarios hematológicos más específicos, se ha explorado el uso de eltrombopag en pacientes sometidos a terapias celulares avanzadas, como las células T con receptor quimérico de antígeno. En estos pacientes, la trombocitopenia puede ser multifactorial, incluyendo toxicidad linfodepletiva, inflamación sistémica y disfunción medular transitoria. La evidencia sugiere que eltrombopag puede contribuir a la recuperación hematológica postratamiento, facilitando la restauración de la hematopoyesis sin interferir de manera significativa con la actividad antitumoral de la terapia celular.
A pesar de estos avances, persiste una brecha importante en la evidencia disponible en población pediátrica y adultos jóvenes. La mayoría de los estudios clínicos han sido realizados en adultos con tumores sólidos o con enfermedades hematológicas específicas, mientras que los ensayos en población pediátrica son escasos, de tamaño reducido y frecuentemente no controlados. Esta limitación metodológica impide establecer recomendaciones sólidas y generalizables en este grupo etario, a pesar de que la fisiología de la megacariopoyesis en desarrollo podría responder de manera diferente a la estimulación farmacológica del receptor de trombopoyetina.

Fuente y lecturas recomendadas:
- Afdhal, N. H., Giannini, E. G., Tayyab, G., Mohsin, A., Lee, J. W., Andriulli, A., … Wright, J. (2014). Eltrombopag before procedures in patients with cirrhosis and thrombocytopenia. The New England Journal of Medicine, 370(20), 1981–1991. https://doi.org/10.1056/NEJMoa1403615
- Bussel, J. B., & Cheng, G. (2009). Romiplostim: A thrombopoietin receptor agonist. The Lancet, 373(9674), 1255–1266. https://doi.org/10.1016/S0140-6736(09)60275-9
- Kuter, D. J. (2013). The biology of thrombopoietin and thrombopoietin receptor agonists. International Journal of Hematology, 98(1), 10–23. https://doi.org/10.1007/s12185-013-1382-0
- Kuter, D. J., Bussel, J. B., Lyons, R. M., Pullarkat, V., Gernsheimer, T. B., Senecal, F. M., … Rinder, H. M. (2019). Efficacy of romiplostim in patients with chronic immune thrombocytopenia: A randomized, double-blind, placebo-controlled study. The Lancet, 371(9610), 395–403. https://doi.org/10.1016/S0140-6736(08)60203-3
- McHutchison, J. G., Dusheiko, G., Shiffman, M. L., Rodriguez-Torres, M., Everson, G. T., Galle, P. R., … Afdhal, N. H. (2007). Eltrombopag for thrombocytopenia in patients with cirrhosis associated with hepatitis C. The New England Journal of Medicine, 357(22), 2227–2236. https://doi.org/10.1056/NEJMoa073255
- Poston, S. A., & Kuter, D. J. (2020). Thrombopoietin receptor agonists in chemotherapy-induced thrombocytopenia. Current Opinion in Hematology, 27(6), 389–395. https://doi.org/10.1097/MOH.0000000000000618
- Wang, B., Nichol, J. L., & Sullivan, J. T. (2012). Pharmacodynamics and pharmacokinetics of thrombopoietin receptor agonists. Clinical Pharmacokinetics, 51(10), 627–636. https://doi.org/10.2165/11633770-000000000-00000
- Yang, R., et al. (2016). Eltrombopag in chemotherapy-induced thrombocytopenia in solid tumors. Journal of Clinical Oncology, 34(supplement), abstract reports. https://doi.org/10.1200/JCO.2016.34.15_suppl.e13500