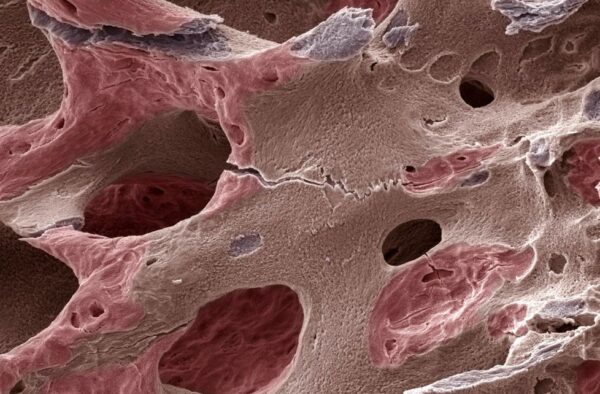
La integridad estructural del tejido óseo depende de un delicado equilibrio entre formación y resorción, regulado por poblaciones celulares altamente especializadas y por un microentorno bioquímico preciso. Cuando este equilibrio se ve alterado por eventos como traumatismos de alta energía, fracturas complejas, anomalías congénitas o procesos neoplásicos, se generan defectos óseos cuya magnitud y complejidad pueden exceder la capacidad intrínseca de regeneración del organismo. En particular, los defectos de gran tamaño en huesos largos representan un desafío significativo, debido a que el volumen de tejido perdido supera el umbral crítico a partir del cual los mecanismos endógenos de reparación dejan de ser eficaces.
En condiciones fisiológicas, la regeneración ósea está mediada principalmente por osteoblastos, células derivadas de precursores mesenquimales que sintetizan matriz extracelular y promueven su mineralización. Sin embargo, cuando el defecto óseo es extenso, la distancia entre los bordes del tejido viable impide una colonización celular adecuada, limita la difusión de nutrientes y reduce la señalización molecular necesaria para inducir la diferenciación osteogénica. Además, la vascularización insuficiente en el sitio lesionado compromete el suministro de oxígeno y factores tróficos, lo que agrava la incapacidad de los osteoblastos para restaurar el tejido perdido.
En este contexto, los injertos óseos autólogos han sido históricamente considerados el estándar terapéutico de referencia. Este enfoque consiste en la recolección de tejido óseo del propio paciente, generalmente de sitios anatómicos como la cresta ilíaca, y su posterior implantación en el área defectuosa. La eficacia de este método radica en que el injerto conserva las propiedades biológicas esenciales del hueso nativo: contiene células osteogénicas viables, una matriz extracelular que actúa como soporte estructural y reservorio de factores de crecimiento, y una arquitectura que facilita la conducción del crecimiento óseo. Estas características confieren al injerto autólogo una triple capacidad funcional: osteogénesis, osteoinducción y osteoconducción.
No obstante, este procedimiento presenta limitaciones importantes. La cantidad de tejido disponible es finita, lo que restringe su aplicación en defectos extensos. Además, la obtención del injerto implica una intervención quirúrgica adicional, que puede generar complicaciones en el sitio donante, tales como dolor crónico, infección, sangrado o debilidad estructural. Estas desventajas han motivado la búsqueda de alternativas terapéuticas más eficientes y menos invasivas.
El uso de injertos alogénicos, provenientes de donantes humanos, representa una de estas alternativas. Desde el punto de vista estructural, este tipo de tejido puede reproducir adecuadamente las propiedades mecánicas del hueso original, proporcionando soporte inmediato en el sitio de implantación. Sin embargo, al tratarse de material biológico externo, existe el riesgo inherente de transmisión de patógenos, a pesar de los rigurosos procesos de esterilización. Asimismo, las diferencias antigénicas entre donante y receptor pueden desencadenar respuestas inmunológicas que comprometan la integración del injerto y reduzcan su eficacia a largo plazo.
En las últimas décadas, la ingeniería de tejidos ha emergido como un campo interdisciplinario capaz de ofrecer soluciones innovadoras para la regeneración ósea. Mediante la combinación de biomateriales, células y señales bioquímicas, esta tecnología permite la fabricación de constructos tridimensionales que imitan las propiedades del tejido óseo natural. Estos sustitutos artificiales tienen el potencial de superar las limitaciones de los injertos tradicionales, ya que pueden producirse en cantidades controladas y diseñarse con características específicas adaptadas a las necesidades del paciente.
La creación de un constructo eficaz en ingeniería de tejidos se basa en tres componentes fundamentales. En primer lugar, los andamios, que constituyen la estructura física sobre la cual se organizan las células. Estos materiales deben poseer una arquitectura porosa que facilite la infiltración celular y la formación de vasos sanguíneos, además de presentar propiedades mecánicas compatibles con el entorno óseo. En segundo lugar, las citocinas y factores de crecimiento, que actúan como señales regulatorias capaces de inducir la proliferación y diferenciación celular. Finalmente, las células semilla, frecuentemente derivadas de poblaciones de células madre mesenquimales, que tienen la capacidad de diferenciarse en osteoblastos y contribuir activamente a la formación de nuevo tejido.
Un andamio ideal no solo debe proporcionar soporte estructural, sino también recrear el microambiente bioquímico del hueso. Esto implica la capacidad de interactuar con las células a nivel molecular, promoviendo su adhesión mediante proteínas específicas, facilitando su migración a través de gradientes químicos y estimulando su proliferación y diferenciación hacia linajes osteogénicos. Además, el material debe ser biocompatible y, en muchos casos, biodegradable, de modo que se degrade progresivamente a medida que el tejido nuevo se forma y asume la función mecánica.
Durante el proceso de regeneración, se desencadena una secuencia altamente coordinada de eventos celulares y moleculares. Inicialmente, las células madre mesenquimales son reclutadas al sitio de lesión mediante señales quimiotácticas. Posteriormente, estas células proliferan y se diferencian en osteoblastos, que comienzan a sintetizar matriz extracelular rica en colágeno tipo uno y otras proteínas estructurales. Esta matriz, conocida como osteoide, sufre un proceso de mineralización mediante la deposición de cristales de hidroxiapatita, lo que confiere rigidez al tejido. Con el tiempo, algunos osteoblastos quedan atrapados en la matriz mineralizada y se transforman en osteocitos, células terminalmente diferenciadas que participan en la regulación del metabolismo óseo.
La matriz extracelular ósea como sistema dinámico regulador en la regeneración y la ingeniería de tejidos
La matriz extracelular constituye una red tridimensional altamente organizada que, lejos de ser un simple soporte pasivo, funciona como un sistema bioactivo esencial para la regulación del comportamiento celular. Esta estructura, sintetizada y secretada por las propias células hacia el espacio extracelular, está formada por una compleja combinación de macromoléculas, principalmente proteínas fibrosas y polisacáridos especializados, cuya disposición espacial y composición química varían de manera precisa según el tipo de tejido y la etapa del desarrollo. En el caso del tejido óseo, esta variabilidad no solo refleja diferencias estructurales, sino también adaptaciones funcionales a demandas mecánicas y metabólicas específicas.
Una de las propiedades más relevantes de la matriz extracelular es su capacidad para conferir integridad estructural y elasticidad al tejido, al mismo tiempo que actúa como un entorno instructivo que modula la adhesión, migración, proliferación y diferenciación celular. Esta función reguladora se basa en interacciones moleculares altamente específicas entre componentes de la matriz y receptores celulares, como las integrinas, así como en la capacidad de la matriz para secuestrar y liberar factores de crecimiento de manera controlada. Además, la matriz extracelular se encuentra en constante remodelación, un proceso dinámico influido por variaciones en el microambiente, incluyendo cambios en el potencial de hidrógeno, la concentración de citocinas y la expresión de receptores celulares. Esta plasticidad permite que la matriz participe activamente en la homeostasis tisular y en la respuesta a lesiones.
En el contexto de la ingeniería de tejidos óseos, la matriz extracelular ha adquirido un papel conceptual central, al ser considerada un cuarto componente fundamental junto con los andamios, las células y las señales bioquímicas. Este reconocimiento surge de la comprensión de que la simple presencia de una estructura física no es suficiente para inducir regeneración funcional; es necesario recrear también el microambiente bioquímico y biomecánico que la matriz proporciona de forma natural. Por ello, el diseño de biomateriales avanzados busca imitar tanto la composición como la organización jerárquica de la matriz ósea nativa.
Desde el punto de vista composicional, la matriz extracelular del hueso presenta una organización bifásica claramente definida. Aproximadamente el sesenta por ciento de su masa corresponde a componentes inorgánicos, principalmente cristales de apatita con deficiencia de calcio, acompañados por diversos elementos traza que modulan sus propiedades fisicoquímicas. Esta fracción mineral es responsable de la rigidez y resistencia a la compresión del tejido. Por otro lado, el cuarenta por ciento restante está constituido por componentes orgánicos, cuya complejidad estructural y funcional es considerablemente mayor. La mayor parte de esta fracción orgánica está formada por colágeno tipo uno, que representa alrededor del noventa por ciento, organizándose en fibras que proporcionan resistencia a la tracción y sirven como andamiaje para la deposición mineral.
El diez por ciento restante de la matriz orgánica está compuesto por proteínas no colágenas, un conjunto heterogéneo de moléculas con funciones reguladoras clave. Estas proteínas pueden agruparse en varias categorías funcionales. Entre ellas se encuentran las proteínas que contienen residuos de ácido γ-carboxiglutámico, que tienen alta afinidad por el calcio y participan en la nucleación de cristales minerales. También destacan los proteoglucanos, que regulan la hidratación de la matriz y modulan la difusión de moléculas señalizadoras. Las glicoproteínas, por su parte, intervienen en la adhesión celular y en la organización de la matriz, mientras que las glicoproteínas pequeñas de unión a integrinas, conocidas como SIBLINs, desempeñan un papel crucial en la señalización celular mediada por integrinas y en la regulación de la mineralización.
Es importante subrayar que la síntesis de la matriz extracelular ósea es llevada a cabo principalmente por los osteoblastos, células especializadas que secretan inicialmente una matriz orgánica no mineralizada denominada osteoide. Este osteoide constituye el sustrato sobre el cual se depositan posteriormente los minerales, en un proceso altamente regulado que da lugar a la formación de tejido óseo maduro. La composición exacta de la matriz puede variar en función de factores biológicos como la edad, el sexo y el estado de salud, lo que refleja la naturaleza adaptable del tejido óseo.
Durante la regeneración ósea, la matriz extracelular no solo actúa como soporte estructural, sino también como mediador activo de la comunicación entre células. Existe una interacción bidireccional constante entre la matriz y las células de la línea osteoblástica, así como con los osteoclastos, responsables de la resorción ósea. Esta interacción permite coordinar los procesos de formación y degradación del tejido, asegurando una remodelación equilibrada. La matriz puede influir en la diferenciación celular mediante señales mecánicas y bioquímicas, mientras que las células, a su vez, modifican la composición y organización de la matriz a través de la secreción de enzimas y nuevos componentes.

Fuente y lecturas recomendadas:
- Lin, X., Patil, S., Gao, Y. G., & Qian, A. (2020). The Bone Extracellular Matrix in Bone Formation and Regeneration. Frontiers in pharmacology, 11, 757. https://doi.org/10.3389/fphar.2020.00757