La pared celular bacteriana constituye una de las estructuras más determinantes para la biología, la fisiología, la ecología y la relevancia médica de las bacterias. Su composición química, su organización tridimensional y su relación con otras envolturas celulares permiten no solo distinguir con claridad a las bacterias Gram positivas de las Gram negativas, sino también explicar cómo estos microorganismos mantienen su integridad estructural, interactúan con el ambiente, resisten agresiones externas y desencadenan respuestas inmunitarias innatas en los organismos hospedadores. A diferencia de las células eucariotas humanas, la pared celular bacteriana contiene componentes exclusivos de los procariotas, con patrones moleculares repetitivos que son reconocidos por receptores del sistema inmunitario innato, lo que convierte a esta estructura en un punto clave de la interacción hospedador-patógeno.
Desde una perspectiva estructural, la pared celular cumple una función esencial de rigidez y soporte. Las bacterias viven sometidas a altas presiones osmóticas internas debido a la elevada concentración de solutos en el citoplasma. Sin una pared celular resistente, la membrana plasmática sería incapaz de contener el contenido celular y la célula sufriría lisis. El principal responsable de esta resistencia mecánica es el peptidoglucano, un polímero exclusivo de bacterias formado por cadenas alternantes de N-acetilglucosamina y ácido N-acetilmurámico, unidas entre sí mediante enlaces glucosídicos y reforzadas por puentes peptídicos. Esta red tridimensional actúa como un armazón rígido que define la forma celular y protege frente a cambios ambientales bruscos.
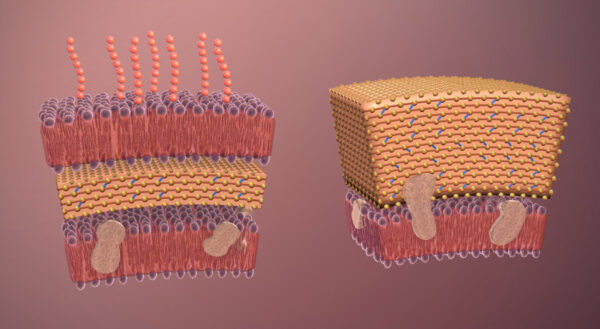
En las bacterias Gram positivas, la pared celular se caracteriza por la presencia de múltiples capas de peptidoglucano, que forman una estructura gruesa y altamente reticulada. Esta abundancia de peptidoglucano no solo confiere gran resistencia mecánica, sino que también protege a la bacteria frente a la acción del sistema del complemento y frente a agresiones físicas y químicas del entorno. Integrados en esta matriz se encuentran los ácidos teicoicos, polímeros de fosfato de glicerol o de fosfato de ribitol que se enlazan covalentemente al peptidoglucano. Estos compuestos refuerzan la pared celular, contribuyen a la carga negativa de la superficie bacteriana y participan en la captación y secuestro de iones como el calcio, fundamentales para la estabilidad estructural. Una variante de estos polímeros, los ácidos lipoteicoicos, se anclan además a la membrana plasmática mediante un componente lipídico, actuando como potentes señales para el sistema inmunitario innato del hospedador.
Las proteínas asociadas a la pared celular de las bacterias Gram positivas desempeñan funciones especializadas que van más allá del soporte estructural. Muchas de ellas intervienen en la adhesión a tejidos del hospedador, facilitando la colonización; otras permiten la evasión del sistema inmunitario, por ejemplo mediante la interferencia con la opsonización o la inhibición de la fagocitosis. En conjunto, la pared celular de las bacterias Gram positivas funciona como una barrera protectora robusta y, al mismo tiempo, como una plataforma activa de interacción biológica.
En contraste, las bacterias Gram negativas presentan una organización de la envoltura celular más compleja y estratificada. Su peptidoglucano es mucho más delgado que el de las Gram positivas y se localiza en un compartimento denominado espacio periplásmico, situado entre la membrana plasmática interna y una membrana externa adicional. Aunque esta capa fina de peptidoglucano sigue siendo esencial para mantener la forma celular, su función estructural se complementa con la membrana externa, que aporta una barrera adicional frente a sustancias tóxicas y defensas del hospedador.
El espacio periplásmico de las bacterias Gram negativas alberga una amplia variedad de proteínas y enzimas implicadas en el transporte de nutrientes, la degradación de moléculas externas y la síntesis de componentes de la pared celular. Este compartimento actúa como una zona funcional altamente especializada, donde se procesan sustancias antes de su entrada al citoplasma o de su expulsión al exterior.
La membrana externa de las bacterias Gram negativas posee una composición química singular. En su cara externa se encuentra el lipopolisacárido, una molécula compleja formada por un lípido A, un núcleo polisacarídico y un antígeno O altamente variable. El lípido A constituye una de las señales inmunológicas más potentes conocidas, ya que es reconocido por receptores del sistema inmunitario innato humano y desencadena respuestas inflamatorias intensas. Esta capacidad explica el papel central de las bacterias Gram negativas en procesos como la sepsis. Además, el lipopolisacárido contribuye de manera decisiva a la función de barrera de la membrana externa, dificultando la entrada de antibióticos y otras sustancias nocivas.
Insertadas en la membrana externa se encuentran proteínas especializadas, como las porinas, que forman canales que permiten el paso selectivo de pequeñas moléculas hidrofílicas, y otros sistemas de secreción que atraviesan una o ambas membranas para transportar proteínas, incluidas toxinas y factores de virulencia, directamente al exterior o al interior de las células del hospedador. Los lipoproteínas que conectan la membrana externa con el peptidoglucano aseguran la estabilidad de toda la envoltura celular.
Más allá de la pared celular propiamente dicha, muchas bacterias presentan estructuras adicionales que amplían sus capacidades biológicas. La cápsula, compuesta generalmente por polisacáridos y en algunos casos por polipéptidos, rodea la pared celular y confiere una potente protección frente a la fagocitosis. Los biofilms, formados por matrices polisacarídicas producidas por comunidades bacterianas, crean microambientes protectores que aumentan la resistencia a antimicrobianos y a la respuesta inmunitaria. Los pili permiten la adhesión a superficies y la transferencia de material genético durante la conjugación, mientras que los flagelos proporcionan motilidad y capacidad de quimiotaxis, facilitando la búsqueda de nichos favorables.
Desde el punto de vista funcional, la pared celular bacteriana integra múltiples roles esenciales. Proporciona rigidez, mantiene el empaquetamiento de los contenidos internos y actúa como una barrera de permeabilidad selectiva. En coordinación con las membranas, regula la captación de metabolitos, participa indirectamente en la producción de energía y posibilita funciones complejas como la motilidad y la reproducción. En la interacción con el hospedador, la pared celular y las estructuras asociadas median la adhesión a células humanas, la activación del sistema inmunitario innato y, en algunos casos, la evasión de las defensas inmunológicas.
La relevancia médica de la pared celular bacteriana es extraordinaria. Muchos antibióticos actúan interfiriendo con la síntesis del peptidoglucano, debilitando la estructura de la pared celular y provocando la muerte bacteriana. Sin embargo, las diferencias entre bacterias Gram positivas y Gram negativas, en particular la presencia de la membrana externa en estas últimas, explican variaciones importantes en la sensibilidad y resistencia a los antibióticos. Así, la pared celular no solo define la identidad estructural de las bacterias, sino que también condiciona su comportamiento patogénico y las estrategias terapéuticas para combatirlas.
Diferencias fundamentales de la pared celular entre bacterias Gram positivas y Gram negativas.
Las bacterias se caracterizan por poseer una envoltura celular rígida que les permite mantener su integridad estructural, resistir fuerzas osmóticas internas y adoptar una morfología definida. El elemento central de esta envoltura es el peptidoglucano, también denominado mureína, un polímero exclusivo de la mayoría de los procariotas. La organización, el espesor y los componentes asociados a este polímero constituyen el criterio fundamental que permite diferenciar a las bacterias Gram positivas de las Gram negativas, y explican profundas diferencias en su comportamiento biológico, su interacción con el hospedador y su respuesta frente a agentes antimicrobianos.
En términos generales, el peptidoglucano forma una malla rígida que rodea la membrana citoplasmática y actúa como un exoesqueleto celular. Esta red tridimensional proporciona resistencia mecánica, evita la lisis osmótica y contribuye de manera decisiva a la determinación de la forma bacteriana, ya sea cocácea, bacilar, helicoidal u otra. Además, el peptidoglucano sirve como plataforma de anclaje para numerosas proteínas y macromoléculas que participan en funciones de adhesión, evasión inmunitaria y comunicación con el entorno.
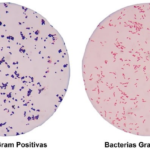
En las bacterias Gram positivas, la pared celular está dominada por una capa muy gruesa de peptidoglucano, formada por múltiples láminas superpuestas y altamente entrecruzadas. Esta estructura maciza constituye la mayor parte de la envoltura celular y es responsable de la intensa retención del colorante cristal violeta durante la tinción de Gram. La ausencia de una membrana externa hace que el peptidoglucano quede directamente expuesto al medio, lo que incrementa su interacción tanto con factores ambientales como con componentes del sistema inmunitario del hospedador.
Un rasgo distintivo de muchas bacterias Gram positivas es la presencia de ácidos teicoicos y lipoteicoicos, polímeros aniónicos que se insertan en la matriz de peptidoglucano o se anclan a la membrana citoplasmática. Estas moléculas contribuyen a la estabilidad estructural de la pared, regulan la carga superficial de la célula y desempeñan un papel clave en la adhesión a tejidos del hospedador. Además, actúan como patrones moleculares reconocidos por receptores inmunitarios innatos, lo que desencadena respuestas inflamatorias protectoras.
Desde el punto de vista funcional, la pared celular gruesa confiere a las bacterias Gram positivas una mayor resistencia frente a la desecación y a la disrupción física. Al mismo tiempo, la exposición directa del peptidoglucano las hace más sensibles a enzimas como la lisozima, que rompe los enlaces del polímero, y a antibióticos como la penicilina, cuyo mecanismo de acción se basa en inhibir la síntesis del peptidoglucano. En algunas especies Gram positivas, esta robustez estructural permite además la formación de endosporas, estructuras altamente resistentes que garantizan la supervivencia en condiciones ambientales extremas.
En contraste, las bacterias Gram negativas presentan una arquitectura de la pared celular más compleja y menos homogénea. Su peptidoglucano es considerablemente más delgado y se localiza en un compartimento específico denominado espacio periplásmico, situado entre la membrana citoplasmática interna y una membrana externa adicional. Esta capa fina de peptidoglucano sigue siendo esencial para la forma y la estabilidad celular, pero su función estructural se ve complementada por la presencia de la membrana externa.
La membrana externa es una característica exclusiva de las bacterias Gram negativas y representa una diferencia crítica respecto a las Gram positivas. Su composición asimétrica incluye fosfolípidos en la cara interna y lipopolisacárido en la cara externa. El lipopolisacárido es una macromolécula compleja que cumple funciones estructurales y defensivas, y cuyo componente lipídico, conocido como lípido A, actúa como endotoxina. Esta endotoxina es un potente activador del sistema inmunitario innato humano y está implicada en respuestas inflamatorias sistémicas severas.
La presencia del lipopolisacárido y de la membrana externa en general confiere a las bacterias Gram negativas una barrera de permeabilidad muy eficaz. Esta barrera limita la entrada de muchas sustancias, incluidos numerosos antibióticos, lo que explica su mayor resistencia relativa a la penicilina y a otros agentes antimicrobianos. Asimismo, esta organización hace que las bacterias Gram negativas sean menos sensibles a la acción de la lisozima, ya que el peptidoglucano queda protegido en el espacio periplásmico.
Desde el punto de vista ecológico y patogénico, la membrana externa también alberga proteínas especializadas, como las porinas, que regulan el paso selectivo de pequeñas moléculas, y sistemas de secreción que permiten la liberación de factores de virulencia. Estas adaptaciones favorecen la supervivencia en ambientes hostiles y la colonización del hospedador, aunque a costa de una menor resistencia frente a la desecación y a la disrupción física en comparación con las bacterias Gram positivas.
Es importante señalar que no todos los procariotas siguen este esquema estructural clásico. Las arqueas poseen paredes celulares formadas por pseudomureínas o pseudoglicanos, químicamente distintos del peptidoglucano bacteriano, mientras que los micoplasmas carecen por completo de pared celular. Estas excepciones refuerzan la idea de que el peptidoglucano es un rasgo definitorio de la mayoría de las bacterias verdaderas y un elemento central para comprender sus diferencias estructurales y funcionales.

Fuente y lecturas recomendadas:
- Madigan, M. T., Martinko, J. M., Bender, K. S., Buckley, D. H., & Stahl, D. A. (2018). Brock biology of microorganisms (15th ed.). Pearson.
- Murray, P. R., Rosenthal, K. S., & Pfaller, M. A. (2025). Medical microbiology (10th ed.). Elsevier.
- Carroll, K. C., & Pfaller, M. A. (2023). Manual of clinical microbiology (13th ed.). American Society for Microbiology Press.
- Riedel, S., Hobden, J. A., Miller, S., Morse, S. A., Mietzner, T. A., Detrick, B., Mitchell, T. G., Sakanari, J. A., Hotez, P., & Mejía, R. (2020). Microbiología médica (28ª ed.). McGraw-Hill Interamericana Editores.