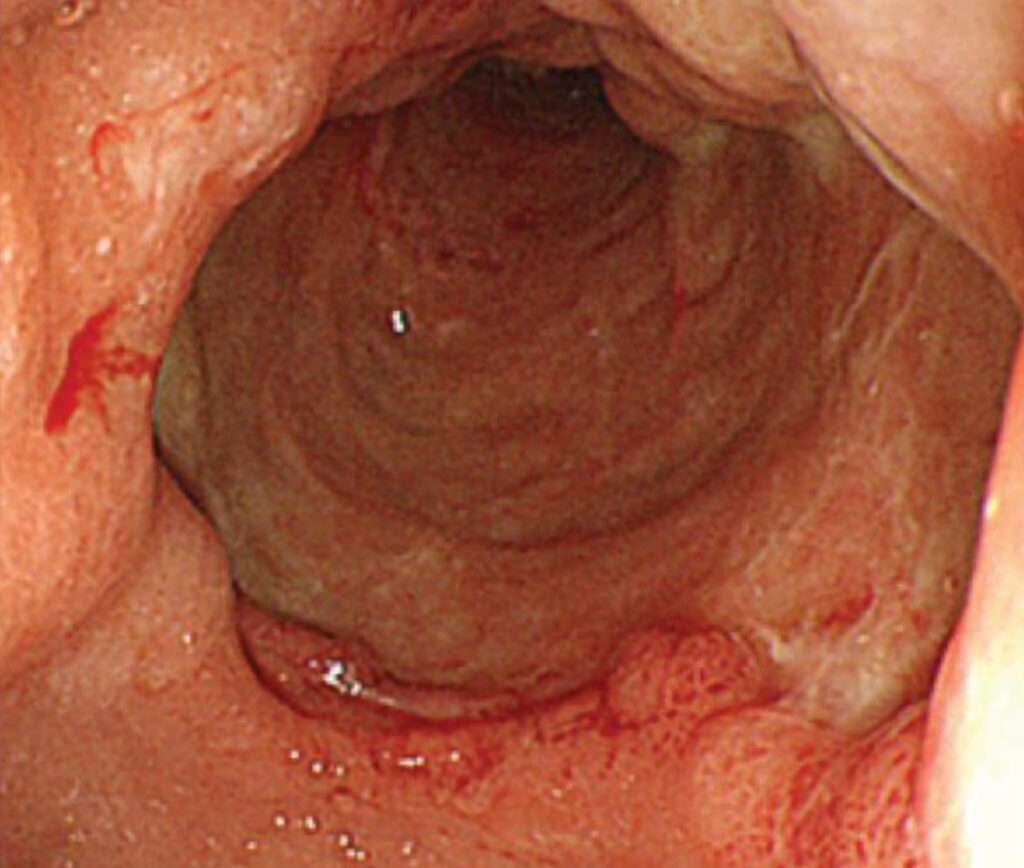
La gastritis flemonosa o necrosante es una condición patológica rara, pero de grave pronóstico, caracterizada por la infección aguda de la submucosa gástrica y de la capa muscularis del estómago. Esta enfermedad, que implica una progresión rápida, está asociada con un proceso inflamatorio y necrosante que afecta las estructuras profundas de la pared gástrica. La infección es causada por una amplia variedad de organismos patógenos, tanto aeróbicos como anaeróbicos, los cuales son capaces de inducir un proceso infeccioso en las capas gástricas profundas, desencadenando una respuesta inflamatoria y la posterior destrucción tisular.
Los microorganismos que pueden estar involucrados en la gastritis flemonosa incluyen bacterias de diversos tipos, como Clostridium, Escherichia coli, y Streptococcus, entre otros, que son capaces de penetrar y proliferar en los tejidos gástricos, comprometiendo la integridad de las mucosas y las estructuras subyacentes. Estos patógenos, al producir toxinas y mediadores inflamatorios, inducen una respuesta inmune exacerbada, lo que lleva a la formación de abscesos y áreas de necrosis en la mucosa gástrica y en las capas musculares. Este daño progresivo puede conducir a una perforación gástrica, hemorragias internas, y un rápido deterioro del estado clínico del paciente, lo que hace de la gastritis flemosa una condición con un riesgo muy alto de mortalidad si no se trata adecuadamente y de forma temprana.
La identificación temprana y el tratamiento oportuno son esenciales para el manejo de esta enfermedad. La terapia antibiótica de amplio espectro es fundamental para controlar la infección bacteriana subyacente, debido a la diversidad de los patógenos que pueden estar involucrados en su etiología. Los antibióticos de amplio espectro permiten cubrir una gama extensa de microorganismos, tanto aeróbicos como anaeróbicos, y pueden ser cruciales para detener la propagación de la infección. En muchos casos, debido a la naturaleza destructiva de la enfermedad, es necesario realizar una resección gástrica de emergencia para eliminar las áreas afectadas de tejido necrosado y evitar complicaciones graves como la perforación o el shock séptico.
En algunos contextos específicos, como en pacientes inmunocomprometidos, la gastritis necrosante puede ser causada por infecciones virales, entre las que destaca el citomegalovirus (CMV). Este virus pertenece a la familia de los herpesvirus y, en condiciones de inmunosupresión, como aquellas que se observan en pacientes con síndrome de inmunodeficiencia adquirida (SIDA) o en aquellos que han recibido un trasplante de médula ósea u órganos sólidos, puede reactivarse y provocar infecciones graves. El CMV tiene una particular afinidad por los tejidos con una alta carga celular, lo que incluye la mucosa gástrica, y su replicación dentro de las células gástricas puede causar daño directo a las estructuras de la mucosa y la submucosa, induciendo una inflamación crónica, úlceras, y eventualmente necrosis.
En estos casos, la infección por CMV puede complicarse con una gastritis crónica, con úlceras gástricas que no responden a tratamientos convencionales. Además, el daño asociado a la infección viral puede ser exacerbado en los pacientes inmunocomprometidos, quienes tienen una capacidad limitada para generar una respuesta inmunitaria eficaz frente a la infección. El manejo de la gastritis viral, en estos pacientes, implica el uso de fármacos antivirales específicos como el valganciclovir o el ganciclovir, que actúan inhibiendo la replicación del virus y ayudando a controlar la progresión de la enfermedad.
Los hallazgos endoscópicos en diversas condiciones patológicas gástricas pueden variar en función del agente causal y de la respuesta inmunitaria del individuo afectado. Entre los hallazgos más característicos de diversas infecciones y trastornos gástricos se incluyen los pliegues gástricos engrosados y las ulceraciones, los cuales son indicadores visuales de una inflamación activa y de daño a la mucosa gástrica. Estas alteraciones son especialmente significativas en el contexto de infecciones fúngicas, parasitarias y ciertos tipos de infestaciones, donde los cambios estructurales en la mucosa pueden ser más pronunciados.
En el caso de las infecciones fúngicas, tanto la mucormicosis como las infecciones por Candida son de particular relevancia en pacientes inmunocomprometidos, como aquellos con enfermedades autoinmunes, receptores de trasplantes, o personas con síndrome de inmunodeficiencia adquirida. La mucormicosis, que es causada por hongos del filo Mucorales, y las infecciones por Candida, que son provocadas por levaduras del género Candida, pueden invadir las mucosas gástricas en individuos cuyas defensas inmunológicas están comprometidas. En estos pacientes, la inmunosupresión o la falta de una respuesta inmunitaria eficaz facilita la colonización y la proliferación de estos hongos patógenos, que pueden inducir un proceso inflamatorio severo.
La infección fúngica se manifiesta endoscópicamente mediante la presencia de pliegues gástricos engrosados, que reflejan la inflamación crónica o aguda de la mucosa gástrica, y ulceraciones que son el resultado del daño tisular directo causado por la invasión de los hongos en los tejidos. Estas ulceraciones pueden ser profundas y pueden comprometer las capas más internas de la mucosa, lo que genera síntomas como dolor abdominal, hemorragias, y en algunos casos, perforaciones gástricas. El tratamiento de estas infecciones fúngicas suele incluir el uso de antifúngicos sistémicos, como el anfotericin B o el fluconazol, y en algunos casos puede requerir procedimientos quirúrgicos para resecar áreas de tejido necrótico o gravemente infectado.
En paralelo, las personas con diabetes, que presentan un mayor riesgo de infecciones fúngicas debido a la alteración en la función inmunológica asociada a niveles elevados de glucosa en sangre, también pueden ser propensas a infecciones por Candida. Estas infecciones en el tracto gastrointestinal pueden provocar síntomas similares, aunque la intervención terapéutica sigue siendo basada en el uso de antifúngicos adecuados y un control exhaustivo de los niveles de glucosa para optimizar la respuesta inmune del paciente.
Por otro lado, las infestaciones parasitarias en el tracto gastrointestinal también pueden ser responsables de alteraciones en la mucosa gástrica. Un ejemplo claro de esto es la infección por larvas de Anisakis marina, un parásito nematodo que se encuentra en peces de aguas frías y que puede ser transmitido a los seres humanos al consumir pescado crudo o mal cocido, como el sushi. Las larvas de Anisakis pueden penetrar en la mucosa gástrica y submucosa del estómago humano, causando una serie de reacciones inflamatorias locales que se traducen en síntomas de dolor abdominal severo.
El dolor abdominal producido por la infestación de Anisakis es típicamente agudo y se localiza en la región epigástrica. La persistencia de los síntomas durante varios días se debe a que las larvas permanecen vivas en la mucosa gástrica mientras no son eliminadas. Sin embargo, a medida que las larvas mueren o son expulsadas por el sistema inmunológico del huésped, el dolor tiende a disminuir y eventualmente se resuelve. Este tipo de infestación se puede observar en una endoscopia, donde las larvas pueden ser visualizadas directamente adheridas a la mucosa gástrica. El tratamiento de esta condición implica la eliminación endoscópica de las larvas, lo cual proporciona un alivio sintomático casi inmediato, ya que se retira el agente causal y se alivia la inflamación y el daño tisular local.
La eliminación endoscópica de las larvas es generalmente un procedimiento seguro y eficaz, que permite la resolución rápida de los síntomas y previene complicaciones adicionales, como úlceras o perforaciones gástricas. En algunos casos, si las larvas no son localizadas o el dolor persiste después de su extracción, pueden ser necesarias otras estrategias terapéuticas, como la administración de medicamentos antihelmínticos o el uso de antiinflamatorios para controlar la inflamación residual.

Fuente y lecturas recomendadas:
- Goldman, L., & Schafer, A. I. (Eds.). (2020). Goldman-Cecil Medicine (26th ed.). Elsevier.
- Loscalzo, J., Fauci, A. S., Kasper, D. L., Hauser, S. L., Longo, D. L., & Jameson, J. L. (Eds.). (2022). Harrison. Principios de medicina interna (21.ª ed.). McGraw-Hill Education.
- Papadakis, M. A., McPhee, S. J., Rabow, M. W., & McQuaid, K. R. (Eds.). (2024). Diagnóstico clínico y tratamiento 2025. McGraw Hill.