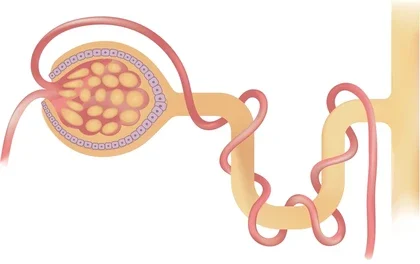
La reabsorción de sodio a lo largo de la nefrona constituye uno de los procesos más finamente regulados de la fisiología humana, ya que determina en gran medida el volumen del líquido extracelular, la presión arterial y la composición iónica del medio interno. Este proceso no es uniforme, sino que está segmentado y especializado, de modo que cada porción de la nefrona expresa transportadores específicos cuya actividad se integra en una arquitectura funcional altamente coordinada. La base energética común a todos estos mecanismos es la actividad de la Na⁺/K⁺-ATPasa localizada en la membrana basolateral de las células epiteliales tubulares, la cual mantiene un gradiente electroquímico de sodio que favorece su entrada desde la luz tubular. Este principio ha sido descrito extensamente en estudios clásicos de fisiología renal, incluyendo los desarrollos experimentales de Homer Smith y posteriores revisiones en textos como el de Brenner y Rector.
En el túbulo proximal, que representa el segmento con mayor capacidad de reabsorción, ocurre aproximadamente el sesenta a setenta por ciento de la recuperación del sodio filtrado. Este proceso se caracteriza por ser isoosmótico, lo que implica que el agua sigue pasivamente al sodio debido a gradientes osmóticos generados por su transporte. Aunque el cotransporte sodio-glucosa constituye un mecanismo relevante, especialmente en la porción inicial del túbulo proximal, no es el único ni el predominante en términos cuantitativos. En realidad, la entrada de sodio a la célula tubular ocurre a través de múltiples sistemas, incluyendo intercambiadores sodio-hidrógeno, cotransportadores con aminoácidos y fosfatos, y mecanismos electrogénicos acoplados al transporte de solutos orgánicos. El cotransportador sodio-glucosa, identificado molecularmente como SGLT2 en el segmento S1, es responsable de la reabsorción casi completa de la glucosa filtrada en condiciones normales, como fue demostrado en estudios moleculares y funcionales sintetizados por Wright y colaboradores. Este sistema ilustra el principio de transporte activo secundario, en el cual el gradiente de sodio generado por la Na⁺/K⁺-ATPasa impulsa la captación de glucosa contra su gradiente de concentración.
La salida del sodio desde la célula hacia el intersticio en el túbulo proximal depende de la actividad continua de la Na⁺/K⁺-ATPasa, mientras que la glucosa utiliza transportadores facilitados de la familia GLUT en la membrana basolateral. Este acoplamiento asegura una transferencia vectorial eficiente de solutos desde el lumen tubular hacia la sangre peritubular, contribuyendo a la recuperación masiva de filtrado sin alterar significativamente la osmolaridad del fluido tubular en este segmento. Guyton y Hall describen este fenómeno como un ejemplo paradigmático de transporte masivo y proporcional, en el cual la reabsorción está estrechamente ligada a la carga filtrada.
En el asa de Henle, particularmente en su rama ascendente gruesa, la reabsorción de sodio adquiere características distintas. Este segmento es impermeable al agua, lo que permite la dilución progresiva del líquido tubular mientras se reabsorben solutos. El principal mecanismo de entrada de sodio es el cotransportador Na⁺-K⁺-2Cl⁻, conocido como NKCC2, localizado en la membrana apical. Este transportador ha sido caracterizado en estudios fisiológicos y genéticos, incluyendo aquellos que analizan el síndrome de Bartter, en el cual mutaciones en NKCC2 alteran la reabsorción de sodio. Una vez dentro de la célula, el sodio es extruido hacia el intersticio por la Na⁺/K⁺-ATPasa, mientras que el potasio puede reciclarse hacia la luz tubular a través de canales específicos, generando un potencial transepitelial positivo que favorece la reabsorción paracelular de cationes como calcio y magnesio. Este conjunto de procesos contribuye de manera decisiva a la generación del gradiente osmótico corticomedular, mecanismo fundamental para la concentración urinaria, como fue formalizado en el modelo de multiplicación por contracorriente descrito por Kokko y Rector.
En los segmentos distales de la nefrona, incluyendo el túbulo contorneado distal y el conducto colector, la reabsorción de sodio es más fina y regulada, en contraste con la reabsorción masiva de los segmentos proximales. En el túbulo distal, el sodio ingresa principalmente a través del cotransportador Na⁺-Cl⁻ sensible a tiazidas, identificado como NCC, cuya importancia clínica se evidencia en el efecto de los diuréticos tiazídicos. Más distalmente, en las células principales del conducto colector, el sodio entra a través de canales epiteliales de sodio, conocidos como ENaC. Estos canales permiten una entrada electrogénica de sodio que está estrechamente acoplada a la secreción de potasio, proceso esencial para el equilibrio electrolítico.
La regulación hormonal en este segmento es determinante. La aldosterona, una hormona esteroidea sintetizada en la corteza suprarrenal, incrementa la reabsorción de sodio al inducir la expresión y actividad de ENaC y de la Na⁺/K⁺-ATPasa. Este efecto ha sido demostrado en estudios clásicos de fisiología endocrina y renal, incluyendo los trabajos de Edelman sobre el control del sodio corporal. La acción de la aldosterona no solo aumenta la reabsorción de sodio, sino que también promueve la secreción de potasio, lo que establece un vínculo directo entre el manejo renal de estos dos iones.
Desde una perspectiva clínica, la segmentación de los mecanismos de transporte de sodio ha permitido el desarrollo de diuréticos que actúan de manera selectiva sobre diferentes porciones de la nefrona. Los diuréticos de asa, como la furosemida, inhiben el cotransportador NKCC2 en la rama ascendente gruesa, produciendo una natriuresis intensa y una reducción significativa del volumen extracelular. Los diuréticos tiazídicos actúan sobre el cotransportador NCC en el túbulo distal, mientras que los diuréticos ahorradores de potasio, como la espironolactona o la amilorida, interfieren con la acción de la aldosterona o con los canales ENaC en el conducto colector. La eficacia de estos fármacos ha sido ampliamente documentada en el tratamiento de la hipertensión arterial y de estados edematosos, como se describe en revisiones clínicas publicadas en revistas como The New England Journal of Medicine.

Fuente y lecturas recomendadas:
- Brenner, B. M., & Rector, F. C. (Eds.). (2011). Brenner & Rector’s The Kidney (9th ed.). Elsevier Saunders.
- Edelman, I. S. (1972). Mechanisms of action of aldosterone. American Journal of Medicine, 53(5), 597–610.
- Guyton, A. C., & Hall, J. E. (2021). Textbook of Medical Physiology (14th ed.). Elsevier.
- Kokko, J. P., & Rector, F. C. (1972). Countercurrent multiplication system without active transport in inner medulla. Kidney International, 2(4), 214–223.
- Palmer, L. G., & Schnermann, J. (2015). Integrated control of Na transport along the nephron. Clinical Journal of the American Society of Nephrology, 10(4), 676–687.
- Wright, E. M., Loo, D. D. F., & Hirayama, B. A. (2011). Biology of human sodium glucose transporters. Physiological Reviews, 91(2), 733–794.