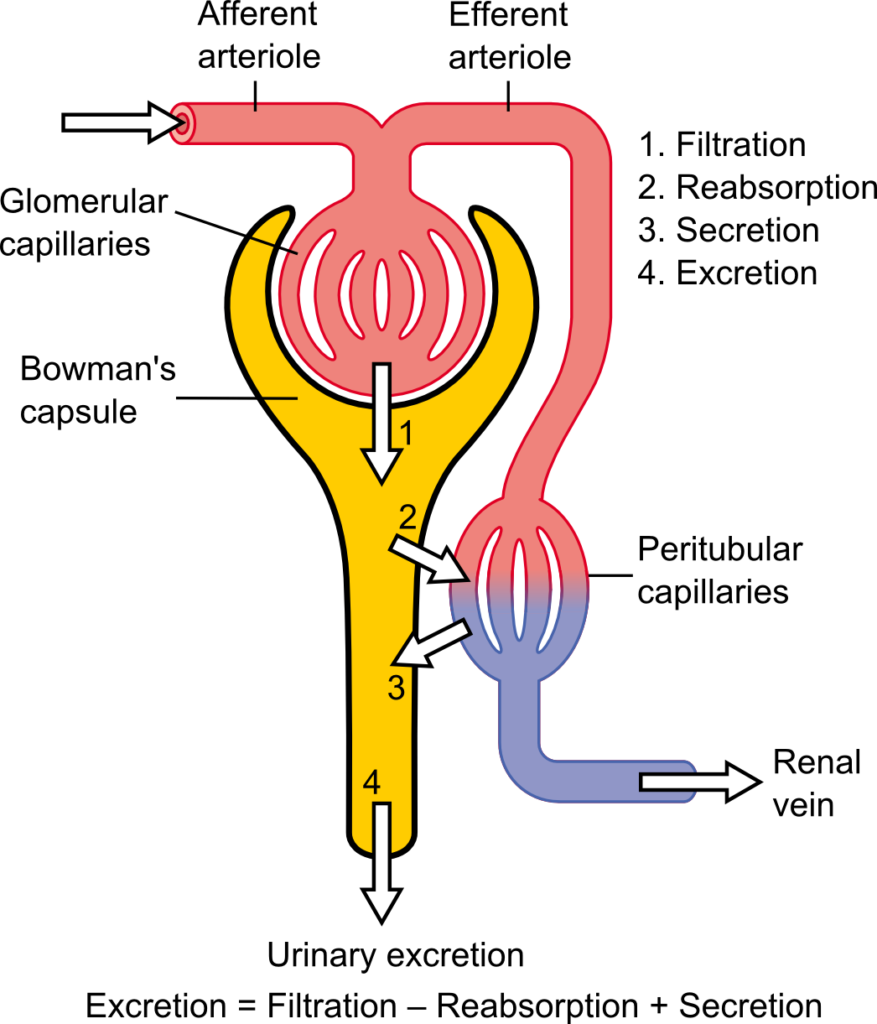
La tasa de filtración glomerular constituye uno de los parámetros fisiológicos centrales para comprender la función renal, ya que cuantifica el volumen de plasma que es depurado por los glomérulos por unidad de tiempo. Este concepto se fundamenta en la organización microanatómica del riñón, donde cada nefrona contiene un glomérulo que actúa como una barrera de filtración altamente especializada, formada por endotelio fenestrado, membrana basal glomerular y podocitos. La combinación de estas estructuras permite el paso selectivo de agua y solutos pequeños desde el plasma hacia el espacio de Bowman, mientras retiene proteínas y elementos formes sanguíneos.
En condiciones fisiológicas, la tasa de filtración glomerular media en adultos sanos se sitúa aproximadamente en 125 mililitros por minuto en hombres y alrededor de 105 a 110 mililitros por minuto en mujeres, cuando se normaliza a una superficie corporal estándar de 1,73 metros cuadrados. Esta diferencia ha sido descrita de manera consistente en la literatura clínica y se atribuye principalmente a variaciones en tamaño corporal, masa renal funcional y composición corporal, más que a una diferencia intrínseca en la eficiencia de la barrera de filtración. Levey y colaboradores, en el desarrollo de ecuaciones de estimación como CKD-EPI, demostraron que el sexo actúa como un modificador estadístico del filtrado estimado, reflejando diferencias promedio de creatinina y masa muscular entre hombres y mujeres, lo cual influye indirectamente en la estimación del filtrado glomerular.
La magnitud de la tasa de filtración glomerular adquiere especial relevancia cuando se compara con el volumen total de los compartimentos líquidos del organismo. El volumen de plasma en un adulto promedio se aproxima a 3 litros, mientras que el líquido extracelular total se sitúa en torno a 14 litros. Sin embargo, el riñón filtra diariamente cerca de 180 litros de plasma en el caso de un varón adulto, según las estimaciones clásicas de Guyton y Hall en su tratado de fisiología médica. Esta cifra implica que el volumen plasmático es filtrado múltiples veces al día, lo que evidencia que la filtración glomerular no tiene como finalidad la pérdida neta de líquido, sino la renovación continua del medio interno.
Este fenómeno se explica por la elevada perfusión renal. Aproximadamente el 20 a 25 por ciento del gasto cardíaco es dirigido hacia los riñones, lo que representa una de las mayores fracciones de flujo sanguíneo por órgano en el cuerpo humano. De ese flujo renal, cerca del 20 por ciento del plasma que entra en los capilares glomerulares es filtrado hacia el espacio de Bowman, lo que se conoce como fracción de filtración. Este valor ha sido descrito de manera consistente en modelos fisiológicos clásicos, incluyendo los desarrollados por Arthur Guyton, y refleja el equilibrio entre las fuerzas de Starling a nivel glomerular: presión hidrostática capilar glomerular, presión oncótica plasmática y presión en el espacio de Bowman.
La importancia fisiológica de esta elevada tasa de filtración no radica únicamente en la eliminación de desechos metabólicos, sino en la capacidad del organismo para ajustar con gran precisión la composición del líquido extracelular. El filtrado glomerular inicial contiene prácticamente todos los solutos libres del plasma, incluyendo electrolitos, glucosa, aminoácidos y productos nitrogenados, con excepción de macromoléculas y proteínas plasmáticas en condiciones normales, como ha sido descrito en los trabajos de Robert W. Schrier y en el tratado de Brenner y Rector sobre el riñón.
Sin embargo, la producción diaria de aproximadamente 180 litros de filtrado haría incompatible la vida si no existiera un mecanismo altamente eficiente de recuperación. Aquí es donde la reabsorción tubular adquiere un papel esencial. Más del 99 por ciento del agua filtrada es reabsorbida a lo largo del sistema tubular renal, junto con proporciones variables de solutos específicos según las necesidades homeostáticas del organismo. Este proceso ocurre mediante mecanismos activos y pasivos distribuidos a lo largo de segmentos especializados de la nefrona, incluyendo el túbulo proximal, el asa de Henle, el túbulo distal y el túbulo colector.
El túbulo proximal es responsable de la reabsorción masiva e isoosmótica de aproximadamente dos tercios del sodio y del agua filtrados, así como casi la totalidad de la glucosa y aminoácidos en condiciones normales. Este hecho ha sido documentado en estudios clásicos de fisiología renal, incluyendo las investigaciones de Homer Smith sobre la función renal en salud y enfermedad. La reabsorción en este segmento ocurre mediante cotransportadores dependientes de sodio y mecanismos de transporte activo secundario que aprovechan el gradiente electroquímico generado por la Na⁺/K⁺-ATPasa basolateral.
El asa de Henle contribuye a la generación del gradiente osmótico medular mediante el mecanismo de multiplicación contracorriente, permitiendo la producción de orina concentrada o diluida según el estado de hidratación del organismo. Este sistema fue descrito y modelado posteriormente en términos cuantitativos por Kokko y Rector, quienes explicaron cómo la permeabilidad diferencial de sus segmentos contribuye a la conservación del agua.
La reabsorción tubular no es un proceso meramente de recuperación pasiva, sino un sistema altamente regulado por hormonas como la aldosterona, la hormona antidiurética y el péptido natriurético auricular. Estas señales permiten ajustar la excreción final de sodio y agua en función de las necesidades hemodinámicas del organismo, lo que confiere a los riñones un papel central en la regulación de la presión arterial y del volumen circulante efectivo, como ha sido ampliamente demostrado en los estudios de Guyton sobre el control renal de la presión arterial.
La relevancia de este sistema se hace evidente cuando se considera que, sin la reabsorción tubular, el organismo perdería diariamente un volumen de líquido equivalente a varias veces el volumen plasmático total. Esto conduciría a una deshidratación severa en pocas horas, acompañada de colapso circulatorio y alteraciones críticas del equilibrio electrolítico. Por ello, la reabsorción tubular representa un mecanismo evolutivamente conservado que permite desacoplar la filtración masiva del plasma de la excreción real de agua y solutos.

Fuente y lecturas recomendadas:
- Brenner, B. M., & Rector, F. C. (Eds.). (2011). Brenner & Rector’s The Kidney (9th ed.). Elsevier Saunders.
- Guyton, A. C., & Hall, J. E. (2021). Textbook of Medical Physiology (14th ed.). Elsevier.
- Kokko, J. P., & Rector, F. C. (1972). Countercurrent multiplication system without active transport in inner medulla. Kidney International, 2(4), 214–223.
- Levey, A. S., Stevens, L. A., Schmid, C. H., Zhang, Y. L., Castro, A. F., Feldman, H. I., … Coresh, J. (2009). A new equation to estimate glomerular filtration rate. Annals of Internal Medicine, 150(9), 604–612.
- Schrier, R. W. (Ed.). (2007). Diseases of the Kidney and Urinary Tract (8th ed.). Lippincott Williams & Wilkins.
- Smith, H. W. (1951). The Kidney: Structure and Function in Health and Disease. Oxford University Press.