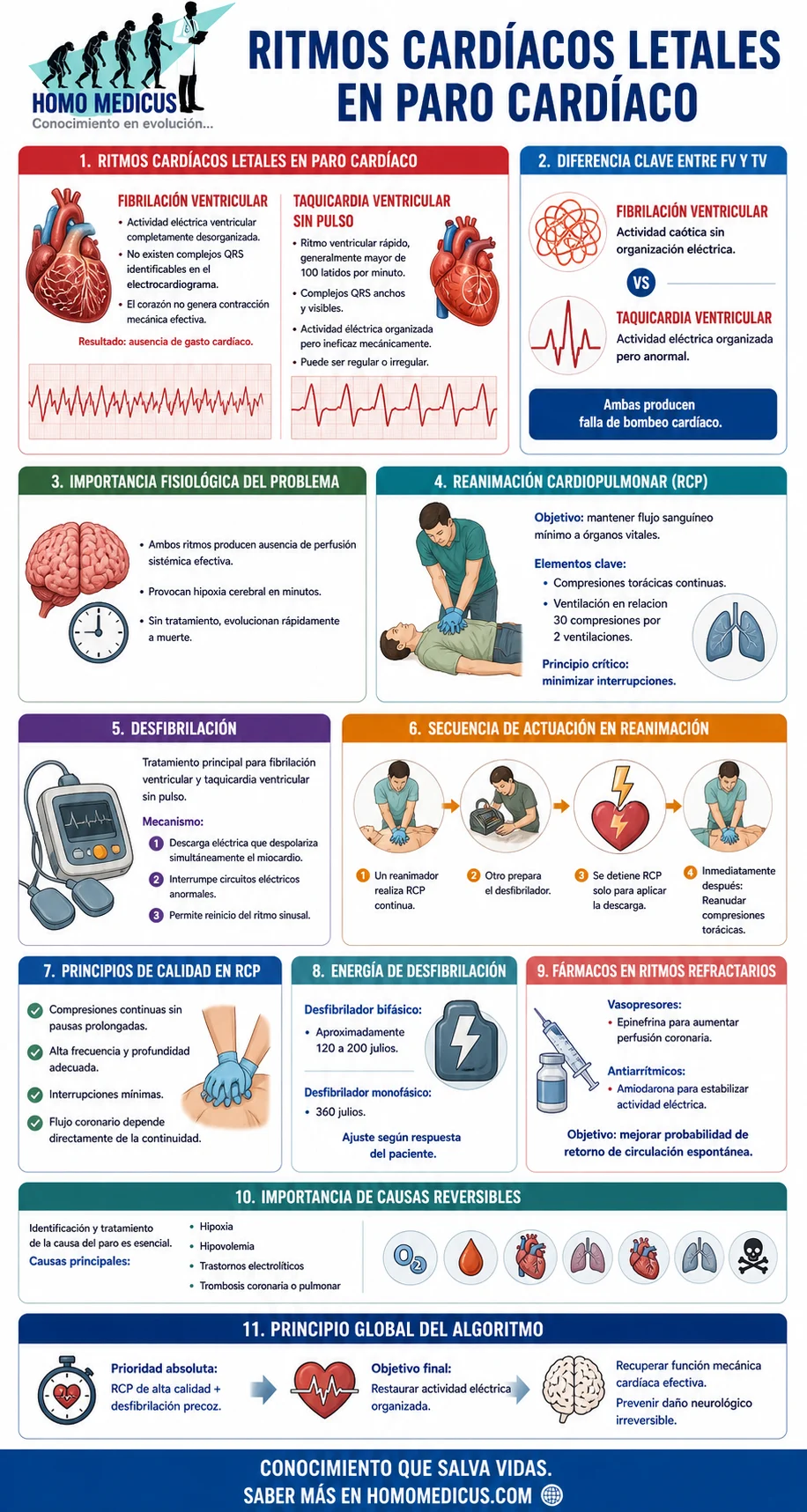
La fibrilación ventricular y la taquicardia ventricular constituyen dos manifestaciones distintas de arritmias ventriculares malignas que comparten un sustrato fisiopatológico común relacionado con la alteración crítica de la propagación del impulso eléctrico en el miocardio ventricular, pero difieren de manera fundamental en la organización espacial y temporal de dicha actividad eléctrica, lo que se traduce en patrones electrocardiográficos claramente distinguibles y en implicaciones terapéuticas inmediatas en el contexto del paro cardíaco.
La fibrilación ventricular se define como una actividad eléctrica ventricular completamente desorganizada, caracterizada por la coexistencia simultánea de múltiples frentes de activación eléctrica que se propagan de forma caótica en el miocardio, lo cual impide la sincronización mecánica efectiva de la contracción ventricular. Las guías clínicas de soporte vital cardiovascular avanzado de la American Heart Association describen este ritmo como una condición en la que la activación eléctrica ventricular pierde toda coordinación funcional, generando una contracción mecánica ineficaz incompatible con el gasto cardíaco efectivo. En términos electrocardiográficos, esta desorganización se expresa como la ausencia de complejos ventriculares identificables, dado que no existe una despolarización ventricular global coherente que produzca complejos QRS discernibles, observándose en su lugar oscilaciones continuas de la línea de base con amplitud y morfología variables. Esta característica ha sido atribuida en la literatura electrofisiológica a mecanismos de reentrada múltiple simultánea, también denominados múltiples ondas de reentrada, que fragmentan la actividad eléctrica en numerosos circuitos funcionales inestables dentro del ventrículo, tal como se describe en revisiones fisiopatológicas de arritmias ventriculares publicadas en la literatura cardiológica de referencia.
La taquicardia ventricular, en contraste, corresponde a una arritmia organizada originada en los ventrículos, caracterizada por la activación repetitiva y rápida del miocardio ventricular a una frecuencia superior a cien latidos por minuto, con presencia de complejos QRS anchos debido a la conducción anómala del impulso eléctrico a través del tejido ventricular en lugar del sistema normal de conducción His Purkinje. Las guías de la Sociedad Europea de Cardiología sobre arritmias ventriculares y prevención de muerte súbita cardíaca describen que este ritmo puede ser monomorfo o polimorfo, dependiendo de si el foco o circuito de reentrada es único y estable o variable, pero en ambos casos se mantiene una cierta organización eléctrica que permite la identificación de complejos QRS bien definidos, aunque ensanchados. El ensanchamiento del complejo QRS, definido convencionalmente como una duración superior a ciento veinte milisegundos, refleja la conducción lenta y anómala del impulso a través del miocardio ventricular, lo que genera una activación no fisiológica del ventrículo y una contracción mecánica ineficiente.
Desde el punto de vista electrofisiológico, la diferencia fundamental entre ambas entidades radica en el grado de organización del frente de despolarización ventricular. En la fibrilación ventricular, la actividad eléctrica es completamente fragmentada y caótica debido a la coexistencia de múltiples circuitos de reentrada que se perpetúan de manera independiente, lo que impide cualquier sincronización global del miocardio. En la taquicardia ventricular, en cambio, la actividad eléctrica suele estar sostenida por un circuito de reentrada único o por un foco ectópico dominante, lo que permite cierta regularidad en la activación ventricular, aunque esta sea patológica. Esta distinción ha sido ampliamente documentada en estudios experimentales de mapeo electrofisiológico que demuestran que la fibrilación ventricular se asocia a activación simultánea en múltiples direcciones sin patrón dominante, mientras que la taquicardia ventricular presenta trayectorias de activación más estables y repetitivas.
Las implicaciones clínicas de estas diferencias son críticas en el contexto del paro cardíaco. Las guías de la American Heart Association para reanimación cardiopulmonar y atención cardiovascular de emergencia establecen que tanto la fibrilación ventricular como la taquicardia ventricular sin pulso constituyen ritmos desfibrilables, debido a que la actividad eléctrica anómala puede ser interrumpida mediante la aplicación de una descarga eléctrica no sincronizada que despolariza de manera simultánea una masa crítica del miocardio ventricular. Este fenómeno permite la interrupción de los circuitos de reentrada y ofrece la posibilidad de que el nodo sinusal recupere el control del ritmo cardíaco. La evidencia clínica acumulada en estudios de reanimación cardiovascular ha demostrado que la desfibrilación precoz en estos ritmos se asocia de manera consistente con una mayor probabilidad de retorno de la circulación espontánea y supervivencia neurológicamente favorable.
La necesidad de intervención inmediata se fundamenta en el hecho de que, tanto en fibrilación ventricular como en taquicardia ventricular sin pulso, la contracción ventricular es ineficaz para generar gasto cardíaco suficiente, lo que conduce rápidamente a hipoperfusión cerebral y sistémica. La literatura de medicina de emergencia describe que la probabilidad de supervivencia disminuye de forma significativa con cada minuto de retraso en la desfibrilación, debido a la progresión de la inestabilidad eléctrica y al agotamiento energético del miocardio.
En el contexto del soporte vital cardiovascular avanzado, la identificación precisa del ritmo mediante monitorización electrocardiográfica o desfibrilador es esencial para la toma de decisiones terapéuticas inmediatas. La diferenciación entre fibrilación ventricular y taquicardia ventricular no solo tiene valor diagnóstico, sino que determina de manera directa la indicación de desfibrilación no sincronizada como intervención prioritaria, acompañada de maniobras de reanimación cardiopulmonar de alta calidad y administración de fármacos vasoactivos según los algoritmos establecidos por las guías internacionales.
Acciones recomendadas
La secuencia de acciones recomendada en la reanimación de pacientes en fibrilación ventricular o taquicardia ventricular sin pulso se fundamenta en principios fisiológicos relacionados con la perfusión coronaria, la preservación del metabolismo cerebral y la reversibilidad de la desorganización eléctrica miocárdica, tal como se establece en las guías internacionales contemporáneas de reanimación cardiopulmonar publicadas por la American Heart Association y por el European Resuscitation Council.
Durante la reanimación cardiopulmonar, las compresiones torácicas generan un gradiente de presión intratorácica que permite un flujo sanguíneo artificial hacia el corazón y el cerebro, lo que mantiene un nivel mínimo de perfusión coronaria necesario para aumentar la probabilidad de éxito de la desfibrilación posterior. Este mecanismo ha sido descrito en estudios experimentales que demuestran que la presión de perfusión coronaria es uno de los determinantes más importantes del retorno de la circulación espontánea. Por esta razón, la interrupción de las compresiones reduce de forma inmediata dicha presión, disminuyendo la probabilidad de restaurar un ritmo cardíaco organizado.
La recomendación de que un rescatador continúe las compresiones torácicas mientras otro prepara el desfibrilador responde al principio de minimizar la fracción de tiempo sin compresiones, ya que incluso pausas breves se asocian con una disminución significativa del flujo coronario. Las guías de reanimación cardiopulmonar establecen que la calidad de las compresiones, definida por profundidad adecuada, frecuencia constante y mínima interrupción, es un predictor directo de supervivencia.
Cuando el desfibrilador se encuentra listo, la interrupción transitoria de las compresiones tiene un objetivo estrictamente fisiológico: permitir la entrega de una descarga eléctrica a nivel global del miocardio ventricular. Esta descarga produce una despolarización simultánea de la mayoría de las células miocárdicas, lo que interrumpe los circuitos de reentrada responsables de la fibrilación ventricular y permite que el nodo sinusal retome el control del ritmo cardíaco. Este mecanismo ha sido demostrado en estudios electrofisiológicos que describen la desfibrilación como una interrupción crítica de la actividad eléctrica caótica mediante la homogeneización transitoria del potencial de membrana miocárdico.
Tras la descarga, la reanudación inmediata de las compresiones torácicas es esencial incluso antes de la reevaluación del ritmo, ya que el miocardio posdesfibrilación puede permanecer eléctricamente inestable y con perfusión insuficiente. La evidencia clínica muestra que la reanudación precoz de las compresiones mejora la probabilidad de recuperación de la actividad mecánica efectiva del corazón. El ciclo de treinta compresiones seguidas de dos ventilaciones se basa en estudios que optimizan el balance entre oxigenación y perfusión, evitando tanto la hipoxia como la reducción del retorno venoso causada por ventilación excesiva.
El modelo de aproximadamente cinco ciclos en dos minutos se relaciona con la necesidad de mantener una frecuencia de compresiones suficiente para sostener la presión de perfusión coronaria, la cual requiere varios segundos de compresiones continuas para alcanzar niveles adecuados. La evidencia experimental demuestra que la presión de perfusión coronaria aumenta progresivamente con compresiones ininterrumpidas y disminuye rápidamente durante las pausas.
En escenarios con un único reanimador, la prioridad de la desfibrilación se mantiene debido a la naturaleza potencialmente reversible de la fibrilación ventricular y la taquicardia ventricular sin pulso mediante choque eléctrico. Las guías de reanimación cardiopulmonar establecen que, en ausencia de asistencia adicional, la identificación rápida del ritmo y la administración de descarga deben prevalecer sobre otras intervenciones, debido a la alta sensibilidad de estos ritmos a la desfibrilación precoz.
La selección de la energía de desfibrilación depende del tipo de onda del dispositivo. En desfibriladores bifásicos, estudios clínicos han demostrado eficacia con energías iniciales entre ciento veinte julios y doscientos julios, con variaciones según el fabricante y el tipo de onda, manteniendo la recomendación de aumentar progresivamente la energía si las descargas iniciales no son efectivas. En desfibriladores monofásicos, la evidencia histórica establece una energía fija de trescientos sesenta julios como estándar, basada en su capacidad para lograr despolarización miocárdica completa en una sola descarga.
Si la fibrilación ventricular o la taquicardia ventricular sin pulso persisten tras desfibrilaciones repetidas, se recomienda la administración de fármacos vasoactivos para mejorar la perfusión coronaria. La epinefrina ha demostrado en ensayos clínicos mejorar el retorno de la circulación espontánea mediante vasoconstricción periférica que incrementa la presión de perfusión coronaria, aunque su impacto en la supervivencia neurológica a largo plazo es más complejo, como se evidenció en el ensayo clínico aleatorizado de gran escala sobre epinefrina en paro cardíaco extrahospitalario.
En casos refractarios, los fármacos antiarrítmicos como la amiodarona se utilizan para estabilizar la excitabilidad miocárdica y reducir la recurrencia de fibrilación ventricular. El ensayo clínico sobre amiodarona, lidocaína o placebo en paro cardíaco extrahospitalario demostró que estos fármacos pueden mejorar la probabilidad de retorno de la circulación espontánea en determinados subgrupos de pacientes con fibrilación ventricular persistente. La dosis inicial de amiodarona de trescientos miligramos intravenosa en bolo se basa en estos hallazgos clínicos y en su perfil electrofisiológico de prolongación de la repolarización ventricular.
Finalmente, la importancia de identificar y tratar la causa subyacente del paro cardíaco se fundamenta en el concepto de causas reversibles, que incluyen hipoxia, hipovolemia, trastornos electrolíticos, trombosis coronaria, trombosis pulmonar, taponamiento cardíaco, neumotórax a tensión y toxinas. Las guías de reanimación cardiopulmonar enfatizan que la supervivencia a largo plazo depende no solo de la restauración del ritmo, sino de la corrección de la alteración fisiopatológica primaria que desencadenó la arritmia.

Fuente y lecturas recomendadas
- American Heart Association. (2020). 2020 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation, 142(16_suppl_2), S337–S357.
- Panchal, A. R., Berg, K. M., Kudenchuk, P. J., et al. (2020). Adult Advanced Cardiovascular Life Support: 2020 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation, 142(16_suppl_2), S366–S468.
- Priori, S. G., Blomström-Lundqvist, C., Mazzanti, A., et al. (2015). 2015 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. European Heart Journal, 36(41), 2793–2867.
- Zipes, D. P., & Wellens, H. J. J. (1998). Sudden cardiac death. New England Journal of Medicine, 339(15), 1070–1076.
- Katzung, B. G. (2021). Basic and Clinical Pharmacology. McGraw-Hill Education.
- Surawicz, B., Childers, R., Deal, B. J., & Gettes, L. S. (2009). AHA/ACCF/HRS recommendations for the standardization and interpretation of the electrocardiogram. Journal of the American College of Cardiology, 53(11), 976–981.
Síguenos en X: @el_homomedicus y @enarm_intensivo Síguenos en instagram: homomedicus y en Treads.net como: Homomedicus