La nefropatía membranosa es la causa más común de síndrome nefrótico en adultos, con una prevalencia especialmente destacada en las décadas quinta y sexta de la vida. Esta enfermedad se clasifica en dos tipos principales: primaria y secundaria, cada una con características patológicas y mecanismos subyacentes distintivos.
La nefropatía membranosa primaria es una enfermedad autoinmune en la cual el sistema inmunológico del cuerpo dirige su respuesta contra varios antígenos posibles en los podocitos, las células especializadas en la barrera de filtración glomerular. Esta alteración inmune provoca un daño a la membrana basal glomerular, lo que resulta en un aumento de la permeabilidad a las proteínas plasmáticas, manifestándose clínicamente como proteinuria masiva, uno de los signos característicos del síndrome nefrótico. Aunque el proceso patológico involucra la formación de complejos inmunes que se depositan en la membrana basal glomerular, la etiología exacta de la enfermedad primaria aún no está completamente esclarecida, pero se reconoce que la reactividad inmunitaria juega un papel crucial.
Por otro lado, la nefropatía membranosa secundaria se asocia con diversas condiciones subyacentes. Infecciones virales como las hepatitis B y C, endocarditis y sífilis se encuentran entre las causas infecciosas más comunes. Además, la enfermedad puede ser consecuencia de neoplasias subyacentes, como el cáncer de pulmón o de colon, así como de enfermedades autoinmunitarias, como el lupus eritematoso sistémico, particularmente en su forma clasificada como tipo V. Ciertos medicamentos también pueden inducir nefropatía membranosa secundaria, siendo los antiinflamatorios no esteroides (AINEs), el captopril y algunos medicamentos tradicionales indígenas los más frecuentemente implicados.
El curso clínico de la nefropatía membranosa primaria es altamente variable. Aproximadamente el 30% de los pacientes experimentan una remisión espontánea de la enfermedad, mientras que en alrededor del 50% de los casos, la enfermedad progresa hacia una insuficiencia renal terminal (ESKD, por sus siglas en inglés) en un período de entre tres y diez años. Esta progresión está influenciada por varios factores, entre los que destacan la presencia concomitante de fibrosis tubulointersticial, el sexo masculino, la elevación de la creatinina sérica en el momento de la presentación clínica, la hipertensión y la proteinuria superior a 10 gramos por día, factores que se asocian con un peor pronóstico.
En comparación con otras causas de síndrome nefrótico, los pacientes con nefropatía membranosa tienen un mayor riesgo de desarrollar un estado de hipercoagulabilidad, lo que aumenta su predisposición a la trombosis de la vena renal. Este fenómeno puede ser consecuencia de la pérdida de proteínas anticoagulantes naturales en la orina, como la antitrombina III, lo que favorece la formación de coágulos. La trombosis de la vena renal es una complicación grave que puede agravar aún más el curso clínico de la enfermedad y empeorar la función renal.
Manifestaciones clínicas
Los pacientes con nefropatía membranosa pueden presentar una amplia variedad de síntomas, que van desde una total ausencia de manifestaciones clínicas hasta la aparición de signos evidentes de la enfermedad. En muchos casos, la presentación inicial de la nefropatía membranosa es asintomática, lo que hace que el diagnóstico sea un desafío temprano. Sin embargo, la mayoría de los pacientes desarrollan síntomas relacionados con la acumulación de líquido en el cuerpo, lo que se manifiesta clínicamente como edema. Este edema puede ser generalizado, afectando a los miembros inferiores, la cara o incluso a otras áreas del cuerpo, dependiendo de la severidad de la retención de líquidos. En algunos casos, también puede observarse la presencia de orina espumosa, que es un signo de la excreción de grandes cantidades de proteínas en la orina, un hallazgo característico del síndrome nefrótico.
La proteinuria masiva, que es una de las características principales de la nefropatía membranosa, se asocia con la alteración de la barrera de filtración renal, lo que permite la fuga de proteínas plasmáticas, como la albúmina, a través de los glomérulos hacia la orina. Esta pérdida de proteínas en la orina resulta en una disminución de los niveles plasmáticos de albúmina, lo que a su vez favorece la acumulación de líquidos en los tejidos intersticiales, produciendo edema. La orina espumosa es un síntoma indirecto de esta proteinuria, ya que la presencia de proteínas en la orina genera burbujas debido a la interacción con el aire.
En algunos pacientes, la trombosis venosa puede ser el primer signo clínico observado. La nefropatía membranosa, al alterar el equilibrio entre los factores anticoagulantes y procoagulantes, induce un estado de hipercoagulabilidad. Esto incrementa el riesgo de formación de coágulos en los vasos sanguíneos, siendo la trombosis de la vena renal una de las complicaciones más comunes. Además de esta, los pacientes también pueden desarrollar trombosis en otras localizaciones, como la trombosis venosa profunda o la embolia pulmonar. En casos severos, estos eventos trombóticos pueden presentarse como un signo inicial de la enfermedad, antes de que se diagnostique la nefropatía membranosa.
En el contexto de la nefropatía membranosa secundaria, es fundamental considerar que los síntomas del síndrome nefrótico pueden coexistir con los signos o síntomas de una enfermedad subyacente que cause la condición. Por ejemplo, en casos secundarios a infecciones, los pacientes pueden experimentar manifestaciones clínicas relacionadas con la infección en cuestión, como fiebre, malestar general o alteraciones en los resultados de los análisis microbiológicos. En particular, infecciones virales como la hepatitis B o C, o bacterianas como la endocarditis, pueden acompañarse de síntomas propios de la infección. Además, cuando la nefropatía membranosa se asocia con cáncer, los síntomas relacionados con el tumor subyacente, como dolor, pérdida de peso inexplicada, fatiga o masas palpables, pueden ser evidentes. Los cánceres de pulmón, estómago, mama y colon son algunos de los más frecuentemente asociados con la nefropatía membranosa secundaria.
Exámenes diagnósticos
La hipoalbuminemia y la hiperlipidemia son hallazgos de laboratorio característicos en el síndrome nefrótico, y su presencia refleja los efectos patológicos de la alteración en la función renal. La hipoalbuminemia ocurre como consecuencia de la pérdida masiva de albúmina en la orina debido a la disfunción de la barrera de filtración glomerular, lo que provoca una disminución significativa de los niveles de albúmina en la sangre. Esta reducción en los niveles de albúmina genera un descenso en la presión oncótica plasmática, favoreciendo la extravasación de líquido hacia los espacios intersticiales, lo que a su vez causa el edema, una característica clínica del síndrome nefrótico. En respuesta a esta hipoalbuminemia, el hígado aumenta la producción de lipoproteínas, lo que lleva al desarrollo de hiperlipidemia, otro hallazgo clásico en estos pacientes. La hiperlipidemia se debe al aumento de las lipoproteínas de baja densidad (LDL) y de las lipoproteínas de muy baja densidad (VLDL), lo que se asocia con un riesgo elevado de aterosclerosis y enfermedades cardiovasculares en el largo plazo.
El diagnóstico de síndrome nefrótico debe incluir una evaluación para causas secundarias, ya que existen diversas condiciones que pueden inducir este síndrome. Esto incluye pruebas serológicas para enfermedades autoinmunes como el lupus eritematoso sistémico (SLE), infecciones como la sífilis y las hepatopatías virales (por ejemplo, hepatitis B y C). Además, es crucial realizar un tamizaje adecuado para neoplasias, particularmente aquellas que con mayor frecuencia están asociadas con la nefropatía membranosa secundaria, como los cánceres de pulmón, mama, estómago y colon. Esta evaluación amplia es fundamental para identificar posibles causas subyacentes y orientar el tratamiento adecuado del paciente, ya que el manejo del síndrome nefrótico puede variar considerablemente dependiendo de la etiología subyacente.
En el caso de la nefropatía membranosa primaria, la presencia de anticuerpos circulantes contra el receptor de fosfolipasa A2 (PLA2R) es considerada diagnóstica y puede eliminar la necesidad de realizar una biopsia renal. La identificación de estos anticuerpos específicos en el suero del paciente, mediante pruebas serológicas, proporciona un marcador altamente sensible y específico para la forma primaria de la enfermedad, lo que facilita el diagnóstico sin la necesidad de procedimientos invasivos. La detección de anticuerpos PLA2R ha revolucionado el enfoque diagnóstico de la nefropatía membranosa, permitiendo un diagnóstico más rápido y preciso.
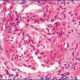
En cuanto a la biopsia renal, los hallazgos característicos en la nefropatía membranosa incluyen un engrosamiento de las paredes capilares glomerulares sin cambios inflamatorios o proliferación celular significativa. Este engrosamiento es el resultado de la deposición de complejos inmunes en la membrana basal glomerular (GBM). Cuando se tiñe la muestra de biopsia con metenamina de plata, se observa un patrón denominado «pico y cúpula» («spike and dome»), que describe la proyección de la membrana basal glomerular entre los depósitos subepiteliales de complejos inmunes. Este patrón es una manifestación histológica distintiva de la enfermedad y refleja la interacción entre los complejos inmunes y la membrana basal glomerular.
La inmunofluorescencia en biopsias renales muestra una tinción positiva de inmunoglobulina G (IgG), C3 (un componente del sistema del complemento) y posiblemente anticuerpos PLA2R a lo largo de los bucles capilares. Esta tinción en la membrana basal glomerular indica la presencia de complejos inmunes que se depositan en el espacio subepitelial, lo cual es característico de la nefropatía membranosa.
En la microscopía electrónica, los depósitos densos de los complejos inmunes en la membrana basal glomerular se visualizan como una distribución discontinuada a lo largo de la superficie subepitelial de la membrana basal. Estos depósitos son intensamente electron-densos, lo que permite su identificación precisa y diferenciación de otras formas de glomerulopatías.
Tratamiento
El tratamiento de la nefropatía membranosa debe basarse en un enfoque diagnóstico y terapéutico meticuloso, comenzando por considerar primero las causas secundarias de la enfermedad antes de proceder con el tratamiento específico para la enfermedad primaria. Esto se debe a que el síndrome nefrótico puede ser el resultado de una amplia gama de condiciones subyacentes, como infecciones, neoplasias, enfermedades autoinmunitarias o reacciones a medicamentos. Por lo tanto, una evaluación exhaustiva para descartar o confirmar causas secundarias, tales como lupus eritematoso sistémico, hepatitis viral o cáncer, es esencial antes de que se inicie un tratamiento específico para la nefropatía membranosa primaria.
Una vez que se ha confirmado que la enfermedad es primaria, el tratamiento debe estar determinado por el riesgo de progresión hacia insuficiencia renal terminal. Este riesgo está fuertemente influenciado por el grado de proteinuria y el funcionamiento renal al momento del diagnóstico. Aproximadamente el 30% de los pacientes con nefropatía membranosa presentan proteinuria subnefrótica, es decir, con niveles inferiores a 3 gramos por día. Estos pacientes, generalmente, tienen un pronóstico favorable y pueden ser manejados de manera conservadora. La terapia antiproteinúrica con inhibidores de la enzima convertidora de angiotensina (ACE) o bloqueadores de los receptores de angiotensina (ARB) es recomendable si la presión arterial es superior a 120/80 mm Hg. Estos fármacos no solo ayudan a controlar la presión arterial, sino que también reducen la proteinuria, lo que contribuye a proteger la función renal.
En algunos casos, incluso aquellos con proteinuria masiva pueden experimentar una remisión espontánea de la enfermedad, un fenómeno que ocurre aproximadamente en el 30% de los pacientes. Esto subraya la importancia de un enfoque cauteloso en el tratamiento inicial, reservando los medicamentos inmunosupresores solo para aquellos pacientes con mayor riesgo de progresión hacia insuficiencia renal terminal. Los pacientes de alto riesgo incluyen aquellos con síndrome nefrótico evidente y función renal aún salvable, es decir, con niveles de creatinina sérica inferiores a 3 gramos por decilitro.
Para los pacientes con mayor riesgo de progresión, el tratamiento inmunosupresor se considera, y las opciones más comunes incluyen el uso de rituximab, corticosteroides y ciclofosfamida. Este tratamiento se administra durante un período de aproximadamente seis meses. Rituximab, un anticuerpo monoclonal dirigido contra las células B, ha demostrado ser eficaz en la reducción de la proteinuria y en la mejora de la función renal en algunos pacientes con nefropatía membranosa. Sin embargo, su efecto puede tardar hasta seis meses en manifestarse completamente, lo que resalta la necesidad de un seguimiento prolongado. En algunos casos, los inhibidores de la calcineurina, tales como tacrolimus, pueden ser una opción terapéutica, con o sin corticosteroides. No obstante, el uso de este régimen de tratamiento se asocia con un mayor riesgo de recaídas, lo que debe ser considerado al momento de tomar decisiones terapéuticas.
El tratamiento debe ser cuidadosamente monitorizado, y los pacientes deben ser evaluados regularmente para determinar la respuesta al tratamiento y el impacto en la función renal. Aunque la reducción de la proteinuria puede llevar varios meses, el manejo adecuado y el monitoreo constante pueden mejorar significativamente el pronóstico de los pacientes, especialmente en aquellos que no progresan a insuficiencia renal terminal.
Por último, los pacientes con nefropatía membranosa primaria que progresan a insuficiencia renal terminal tienen excelentes perspectivas de tratamiento mediante trasplante renal. Dado que la nefropatía membranosa primaria es una causa de insuficiencia renal irreversible en algunos casos, el trasplante es una opción valiosa para aquellos pacientes que no responden adecuadamente al tratamiento conservador o inmunosupresor. El trasplante renal ofrece una oportunidad de restaurar la función renal y mejorar significativamente la calidad de vida de los pacientes afectados por esta enfermedad.

Fuente y lecturas recomendadas:
- Peritore L et al. How to choose the right treatment for membranous nephropathy. Medicina. 2023;59:1997. [PMID: 38004046] Ponticelli C. Primary membranous nephropathy: an endless story. J Nephrol. 2023;36:563. [PMID: 36251213]
- Stai S et al. From KDIGO 2012 towards KDIGO 2021 in idiopathic membranous nephropathy guidelines: what has changed over the last 10 years? J Nephrol. 2023;36:551. [PMID: 36450999]
Originally posted on 29 de marzo de 2025 @ 8:55 AM