Sulfonilureas
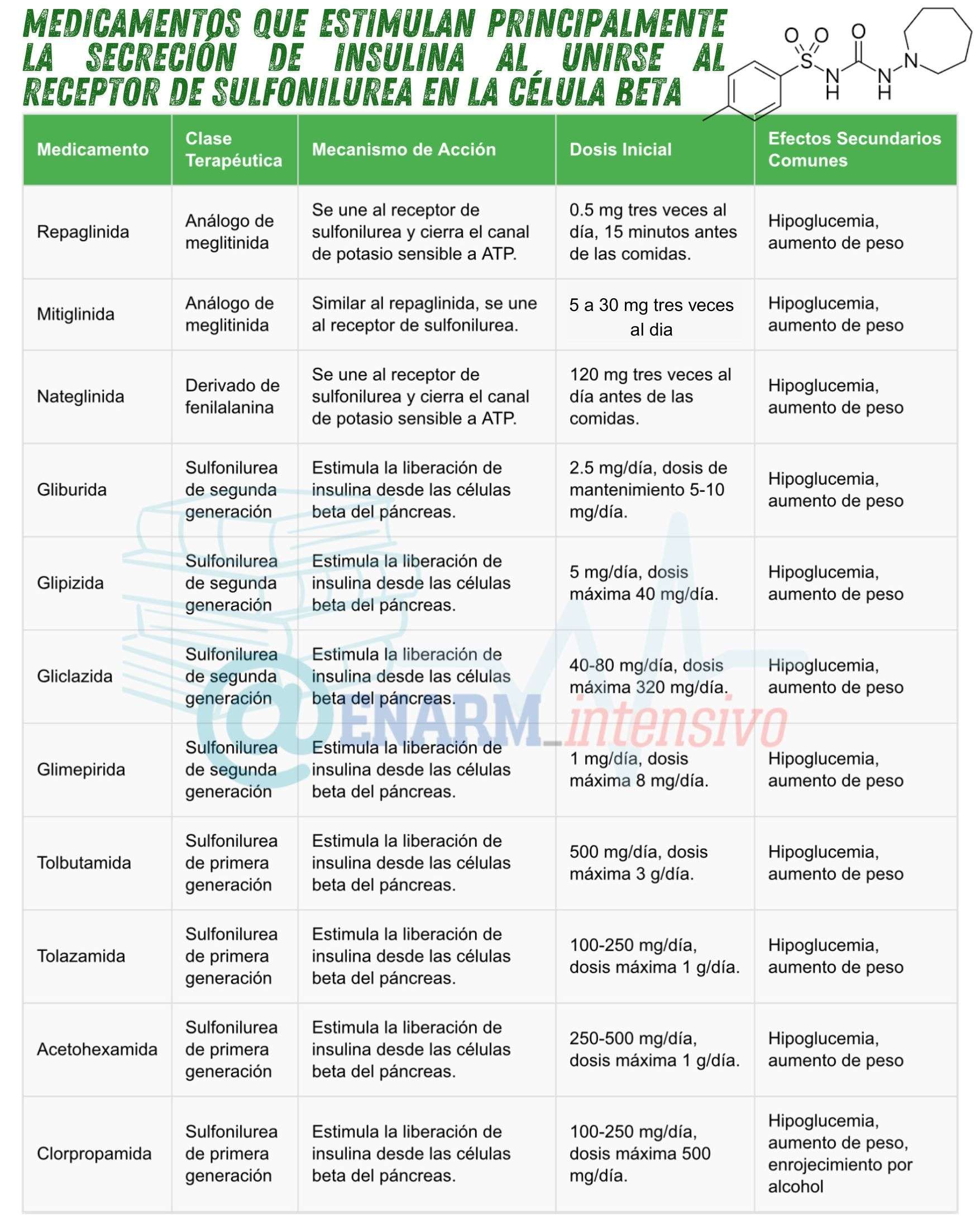
Los medicamentos que estimulan principalmente la secreción de insulina al unirse al receptor de sulfonilurea en las células beta del páncreas, como las sulfonilureas, juegan un papel fundamental en el tratamiento de la diabetes tipo 2. Su mecanismo de acción primario consiste en incrementar la liberación de insulina desde las células beta del páncreas, lo que contribuye a la reducción de los niveles de glucosa en sangre. Las sulfonilureas se metabolizan en el hígado, y, salvo en el caso del acetohexamida, cuyo metabolito es más activo que el compuesto original, los metabolitos de las otras sulfonilureas son débilmente activos o inactivos. Estos metabolitos se excretan a través de los riñones, y en el caso de las sulfonilureas de segunda generación, parte de ellos se excretan también por la bilis.
Uno de los efectos adversos más comunes de las sulfonilureas es la hipoglucemia, que puede ser especialmente pronunciada cuando la medicación se toma en dosis elevadas o en combinación con otros factores como el ejercicio o la ingesta insuficiente de alimentos. Además, el aumento de peso es frecuente, particularmente durante el primer año de uso. Este aumento de peso se puede atribuir a la mejora del control glucémico y a un mayor consumo de alimentos como respuesta a los episodios de hipoglucemia. Las reacciones idiosincráticas son poco comunes, pero pueden incluir erupciones cutáneas o toxicidad hematológica, como leucopenia o trombocitopenia, que se presentan en menos del 0.1% de los usuarios.
1. Sulfonilureas de primera generación
Las sulfonilureas de primera generación, como el tolbutamida, tolazamida, acetohexamida y clorpropamida, han sido en gran medida reemplazadas por agentes de generaciones más recientes. La clorpropamida, en particular, tiene un efecto biológico prolongado, lo que puede llevar a la aparición de hipoglucemia severa, especialmente en personas mayores, debido a la disminución de la depuración renal asociada con el envejecimiento. Además, entre sus efectos secundarios se incluyen el enrojecimiento facial inducido por el alcohol y la hiponatremia, que resulta del aumento de la secreción de vasopresina.
2. Sulfonilureas de segunda generación
Las sulfonilureas de segunda generación, como la gliburida, glipizida, gliclazida y glimepirida, son de 100 a 200 veces más potentes que el tolbutamida. Estos medicamentos deben usarse con precaución en pacientes con enfermedades cardiovasculares o en pacientes mayores, en quienes la hipoglucemia prolongada sería especialmente peligrosa. La gliburida, por ejemplo, suele iniciarse a una dosis oral de 2.5 mg al día, con una dosis de mantenimiento promedio de 5 a 10 mg al día, administrada como una dosis única por la mañana. Las dosis superiores a 20 mg al día no son recomendadas. La gliburida se metaboliza en el hígado, y los productos metabólicos tienen actividad hipoglucemiante. Aunque rara vez se ha informado sobre el enrojecimiento facial tras la ingestión de etanol, este medicamento puede causar hipoglucemia prolongada y no debe usarse en pacientes mayores ni en aquellos con insuficiencia hepática o enfermedad renal crónica.
La glipizida, por otro lado, generalmente comienza con una dosis oral de 5 mg al día, con un máximo de 15 mg al día administrado como una dosis diaria única antes del desayuno. Cuando se requieren dosis diarias más altas, deben dividirse y tomarse antes de las comidas. La dosis máxima recomendada es de 40 mg al día, aunque las dosis superiores a 10-15 mg probablemente no proporcionan beneficios adicionales. Para obtener el máximo efecto en la reducción de la hiperglucemia posprandial, la glipizida debe ingerirse 30 minutos antes de las comidas, ya que la absorción rápida se retrasa cuando se toma con alimentos.
La gliclazida, que no está disponible en los Estados Unidos, tiene una duración de acción intermedia de aproximadamente 12 horas. La dosis inicial recomendada es de 40 a 80 mg al día, con una dosis máxima de 320 mg. Las dosis de 160 mg o más se administran en dosis divididas antes del desayuno y la cena. Este medicamento también se metaboliza en el hígado, pero sus metabolitos no tienen efectos hipoglucemiantes. Existe una formulación de liberación prolongada disponible para este medicamento.
La glimepirida tiene una larga duración de acción con una vida media de 5 horas, lo que permite su dosificación una o dos veces al día. La glimepirida es eficaz en dosis más bajas que cualquier otro compuesto de sulfonilurea, y una dosis diaria de 1 mg ha demostrado ser efectiva. La dosis máxima recomendada es de 8 mg. Al igual que las otras sulfonilureas, la glimepirida se metaboliza completamente en el hígado a productos metabólicos relativamente inactivos.
Análogos de meglitinida
El repaglinida es un medicamento que, estructuralmente, es similar a la gliburida, pero carece del grupo ácido sulfónico-urea. Su mecanismo de acción consiste en unirse al receptor de sulfonilurea en las células beta del páncreas, lo que provoca el cierre del canal de potasio sensible a ATP. Este mecanismo genera una liberación rápida de insulina. El repaglinida es absorbido de manera rápida desde el intestino y, posteriormente, es metabolizado completamente en el hígado, dando lugar a productos inactivos que se excretan por la bilis, lo que le confiere una vida media plasmática de menos de una hora. Esto implica que el medicamento induce un pulso rápido pero breve de insulina tras su administración.
La dosis inicial recomendada de repaglinida es de 0.5 mg tres veces al día, tomada 15 minutos antes de cada comida. La dosis puede ajustarse hasta un máximo de 16 mg diarios. Al igual que las sulfonilureas, el repaglinida puede ser utilizado en combinación con metformina para un control glucémico más eficaz. El principal efecto secundario de este medicamento es la hipoglucemia, un fenómeno común también en otras clases de secretagogos de insulina. Además, el repaglinida puede causar aumento de peso, similar a las sulfonilureas, debido a la mejora en el control glucémico y la respuesta a la hipoglucemia.
El metabolismo de repaglinida ocurre principalmente a través de la isoenzima 3A4 del citocromo P450, por lo que otros fármacos que induzcan o inhiban esta isoenzima pueden alterar el metabolismo del repaglinida, incrementando o disminuyéndolo, respectivamente. Este medicamento puede ser útil en pacientes con insuficiencia renal o en adultos mayores, ya que no depende de la función renal para su eliminación. Además de repaglinida, existe otro medicamento denominado mitiglinida, un derivado del ácido bencilsuccínico que también se une al receptor de sulfonilurea y presenta efectos clínicos similares a los del repaglinida.
Derivado de D-fenilalanina
El nateglinida es otro secretagogo de insulina que actúa de manera similar al repaglinida y a las sulfonilureas. Su mecanismo de acción consiste en unirse al receptor de sulfonilurea en las células beta del páncreas, lo que también induce el cierre del canal de potasio sensible a ATP. Este proceso provoca la liberación de insulina. El nateglinida se absorbe rápidamente en el intestino y alcanza niveles plasmáticos máximos en aproximadamente una hora tras su administración. El fármaco es metabolizado en el hígado y tiene una vida media plasmática de aproximadamente 1.5 horas, lo que lo hace un agente de acción corta.
Al igual que el repaglinida, el nateglinida causa un breve y rápido pulso de insulina, lo que lo hace eficaz para reducir el aumento de glucosa en sangre posterior a las comidas. La dosis inicial y de mantenimiento recomendada para la mayoría de los pacientes es de 120 mg tres veces al día, antes de las comidas. En pacientes con niveles ligeramente elevados de hemoglobina A1c, la dosis puede reducirse a 60 mg. Al igual que otros secretagogos de insulina, los efectos secundarios más comunes de nateglinida son la hipoglucemia y el aumento de peso, debido a la estimulación de la liberación de insulina.

Fuente y lecturas recomendadas:
- Goldman, L., & Schafer, A. I. (Eds.). (2020). Goldman-Cecil Medicine (26th ed.). Elsevier.
- Loscalzo, J., Fauci, A. S., Kasper, D. L., Hauser, S. L., Longo, D. L., & Jameson, J. L. (Eds.). (2022). Harrison. Principios de medicina interna (21.ª ed.). McGraw-Hill Education.
- Papadakis, M. A., McPhee, S. J., Rabow, M. W., & McQuaid, K. R. (Eds.). (2024). Diagnóstico clínico y tratamiento 2025. McGraw Hill.
- Rozman, C., & Cardellach López, F. (Eds.). (2024). Medicina interna (20.ª ed.). Elsevier España.
Originally posted on 7 de mayo de 2025 @ 11:31 PM



