El proceso subyacente en el síndrome coronario sin elevación del segmento ST (SCACEST) se inicia con la rotura o erosión de una placa ateroesclerótica en una arteria coronaria. Esta placa, compuesta por lípidos, células inflamatorias y otros componentes, puede volverse vulnerable debido a varios factores.
La cubierta fibrosa que normalmente protege el núcleo lipídico de la placa se ve comprometida por la inflamación local y sistémica, factores mecánicos y cambios anatómicos. Este deterioro conduce a la transformación de la placa ateroesclerótica estable en una «placa vulnerable». Esta placa vulnerable, al sufrir una rotura o erosión, expone su contenido procoagulante al torrente sanguíneo.
La respuesta del cuerpo a esta rotura desencadena la adherencia, activación y agregación plaquetarias, dando lugar a la formación de un trombo. Este trombo puede obstruir parcial o completamente el flujo sanguíneo en la arteria coronaria, lo que resulta en el SCACEST.
El depósito de lipoproteínas de baja densidad oxidadas en la pared coronaria desencadena una respuesta inflamatoria significativa. Este proceso conlleva la acumulación de macrófagos y linfocitos T en el límite de la placa ateroesclerótica. Estas células inflamatorias desempeñan un papel crucial en la progresión de la enfermedad coronaria al secretar diversas moléculas, entre las cuales se destacan citocinas como el factor de necrosis tumoral, la interleucina 1 y el interferón γ.
La acción de estas citocinas tiene efectos perjudiciales en la placa ateroesclerótica al inhibir la síntesis y el depósito de colágeno, una proteína esencial para la integridad estructural de la placa. Además, las células inflamatorias liberan enzimas como las metaloproteinasas de la matriz y las catepsinas, que promueven la degradación del colágeno y de la elastina. Esto debilita la cubierta fibrosa suprayacente, aumentando así la vulnerabilidad de la placa a la rotura.
Es importante destacar que la inflamación no se limita a la localización de la placa, sino que también puede tener un impacto sistémico. Este hecho se evidencia en la predisposición al síndrome coronario agudo en personas con condiciones inflamatorias crónicas como la gingivitis, la artritis reumatoide, y en casos de infección aguda o crónica. La inflamación sistémica contribuye al proceso de ruptura de la placa ateroesclerótica, acentuando la importancia de abordar tanto los factores locales como los sistémicos en la prevención y tratamiento de las enfermedades coronarias.
En síndrome coronario agudo, los estudios angiográficos y angioscópicos revelan fenómenos como la ulceración y trombosis de placas en múltiples puntos de las arterias coronarias. Esta observación sugiere la presencia de un proceso inflamatorio sistémico y difuso. Este fenómeno indica que no se trata simplemente de eventos localizados, sino que hay factores inflamatorios que afectan a múltiples áreas de las arterias coronarias.
La estabilidad de las placas coronarias parece depender de características mecánicas específicas y su ubicación anatómica. Por ejemplo, las placas con cubiertas fibrosas delgadas tienen una mayor propensión a erosionarse o romperse en comparación con aquellas con cubiertas más gruesas. Esta diferencia estructural influye en la vulnerabilidad de la placa y su capacidad para resistir tensiones mecánicas.
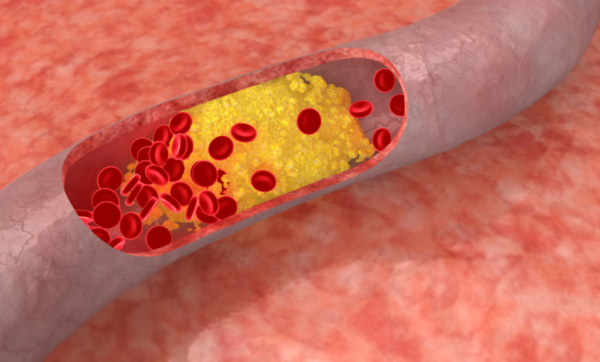
Los puntos con baja tensión de cizallamiento, como las bifurcaciones de los vasos, presentan condiciones adversas. En estos sitios, se reduce la producción de sustancias vasodilatadoras endoteliales, como el óxido nítrico y la prostaciclina. Esto contribuye a la aceleración de la acumulación de lípidos y células inflamatorias en esas áreas. Además, hay un aumento en la degradación de la matriz extracelular y un adelgazamiento de la cubierta fibrosa, factores que colectivamente contribuyen a la inestabilidad de la placa en esos puntos específicos.
El análisis histológico detallado de las placas ateroescleróticas en evolución revela un fenómeno fascinante: la presencia de una rica neovascularización. Este proceso se desencadena como resultado de la liberación de péptidos angiógenos, entre los cuales destacan los factores de crecimiento de los fibroblastos, factores de crecimiento del endotelio vascular, factor de crecimiento placentario, oncostatina M y factor inducible por la hipoxia. Estos péptidos son secretados por diversos actores celulares, incluyendo los miocitos lisos, células inflamatorias y plaquetas.
La neovascularización en las placas ateroescleróticas desempeña un papel crucial en la progresión de la enfermedad. Contribuye al crecimiento del ateroma, que es la acumulación de lípidos y células inflamatorias en la pared arterial. Además, facilita la circulación de leucocitos, células que forman parte del sistema inmunológico, hacia la placa ateroesclerótica. Esta migración de leucocitos puede intensificar la inflamación en la placa, exacerbando la respuesta inmune local.
La neovascularización también se asocia con la posibilidad de hemorragia en la placa, lo que añade otra capa de complejidad al proceso ateroesclerótico. La presencia de sangre en la placa contribuye a su desestabilización, aumentando el riesgo de ruptura. Cuando la placa se torna vulnerable, hay un mayor riesgo de eventos cardiovasculares agudos, como el síndrome coronario agudo.