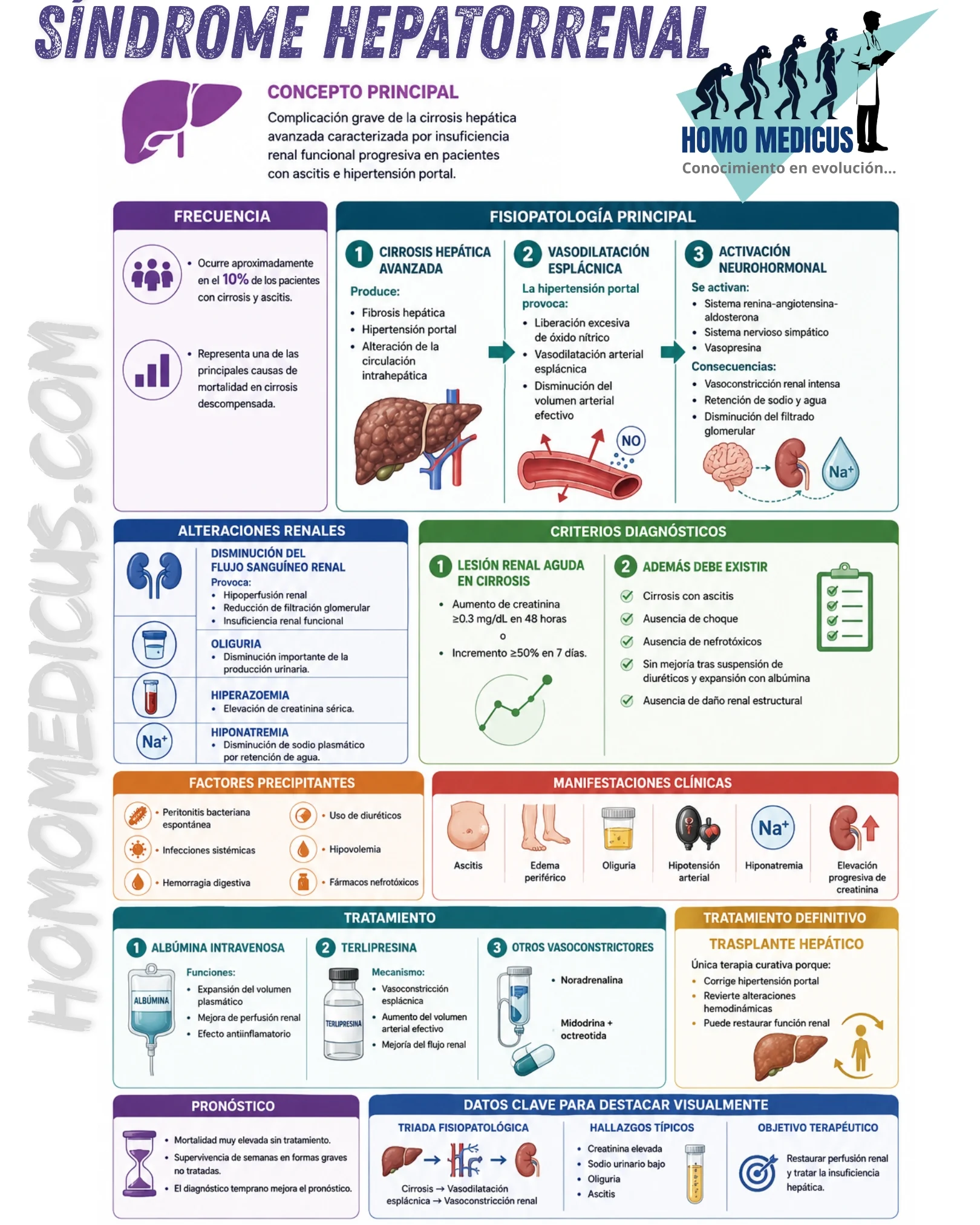
El síndrome hepatorrenal constituye una de las complicaciones más graves y complejas de la cirrosis hepática avanzada. Se trata de una forma de insuficiencia renal funcional que aparece en individuos con enfermedad hepática crónica descompensada, particularmente en presencia de ascitis, hipertensión portal e intensa disfunción circulatoria sistémica. Su relevancia clínica radica en que representa la expresión final de profundas alteraciones hemodinámicas, neurohormonales e inflamatorias inducidas por la progresión de la cirrosis. La mortalidad asociada continúa siendo extremadamente elevada, especialmente cuando no se instaura tratamiento precoz o cuando el paciente no es candidato a trasplante hepático. Diversos estudios clínicos y consensos internacionales han demostrado que aproximadamente el 10% de los pacientes con cirrosis y ascitis desarrollan síndrome hepatorrenal durante la evolución de su enfermedad.
La cirrosis hepática avanzada produce una transformación estructural progresiva del hígado caracterizada por fibrosis difusa, formación de nódulos regenerativos y distorsión de la arquitectura vascular intrahepática. Estos cambios incrementan la resistencia al flujo portal y originan hipertensión portal. El aumento sostenido de la presión portal desencadena vasodilatación arterial esplácnica mediada principalmente por óxido nítrico, monóxido de carbono, prostaciclinas, endocannabinoides y otros mediadores vasodilatadores. Como consecuencia, ocurre un secuestro masivo de volumen sanguíneo en el territorio esplácnico, lo cual reduce el volumen arterial efectivo a pesar de que el volumen plasmático total pueda encontrarse aumentado por retención hidrosalina.
La disminución del volumen arterial efectivo constituye el evento fisiopatológico central que explica el desarrollo del síndrome hepatorrenal. El organismo interpreta esta reducción como un estado de hipovolemia arterial y activa mecanismos compensadores neurohormonales extremadamente potentes. Entre ellos destacan la activación del sistema renina-angiotensina-aldosterona, el incremento de la actividad simpática y la liberación no osmótica de vasopresina. La activación del sistema renina-angiotensina-aldosterona induce intensa vasoconstricción renal y aumenta la reabsorción tubular de sodio y agua. Simultáneamente, la hiperactividad simpática incrementa todavía más la resistencia vascular renal, mientras que la vasopresina favorece retención de agua libre. Todos estos mecanismos intentan preservar la presión arterial y la perfusión cerebral y coronaria, pero generan un deterioro progresivo de la perfusión renal.
La circulación renal en el síndrome hepatorrenal presenta una vasoconstricción intensa y sostenida, predominantemente en la corteza renal. Aunque el riñón conserva inicialmente una estructura histológica relativamente normal, el flujo sanguíneo renal y la filtración glomerular disminuyen de manera crítica. Este fenómeno diferencia al síndrome hepatorrenal de otras formas de lesión renal intrínseca, ya que el daño inicial es funcional más que estructural. Sin embargo, cuando la hipoperfusión se prolonga, puede coexistir lesión tubular aguda verdadera, especialmente en pacientes con sepsis, hipotensión severa o exposición a nefrotóxicos.
En años recientes se ha demostrado que la inflamación sistémica desempeña un papel fundamental en la fisiopatología del síndrome hepatorrenal. La hipertensión portal y el edema intestinal favorecen translocación bacteriana desde el intestino hacia ganglios linfáticos mesentéricos y circulación sistémica. Productos bacterianos como lipopolisacáridos inducen liberación masiva de citocinas proinflamatorias, incluyendo factor de necrosis tumoral alfa e interleucinas inflamatorias. Estas sustancias agravan la vasodilatación esplácnica y empeoran la disfunción circulatoria sistémica. Además, la inflamación contribuye directamente a disfunción endotelial y alteraciones microcirculatorias renales. Este componente inflamatorio explica por qué infecciones bacterianas como la peritonitis bacteriana espontánea precipitan con frecuencia síndrome hepatorrenal.
La hiperazoemia observada en el síndrome hepatorrenal se manifiesta principalmente mediante incremento progresivo de creatinina sérica. El diagnóstico moderno se basa en criterios definidos por el International Club of Ascites. Actualmente se considera lesión renal aguda en cirrosis un aumento de creatinina sérica ≥0.3 mg/dL en menos de 48 horas o un incremento ≥50% respecto al valor basal en los siete días previos. El diagnóstico de síndrome hepatorrenal requiere además la presencia de cirrosis con ascitis, ausencia de choque, ausencia de nefrotóxicos recientes y falta de mejoría de la función renal después de retirar diuréticos y administrar albúmina intravenosa durante al menos 48 horas. También deben excluirse datos de lesión renal estructural, como proteinuria significativa, hematuria microscópica importante o alteraciones ultrasonográficas renales.
La oliguria es consecuencia directa de la intensa vasoconstricción renal y de la reducción de la presión de filtración glomerular. El riñón disminuye la producción urinaria como mecanismo adaptativo para conservar volumen intravascular. Simultáneamente, la reabsorción tubular de sodio alcanza niveles máximos debido a la activación neurohormonal extrema. Por esta razón, la concentración de sodio urinario suele ser muy baja y la fracción excretada de sodio generalmente es inferior a 0.2%. Estas alteraciones reflejan la capacidad conservada del túbulo renal para retener sodio, característica típica del síndrome hepatorrenal funcional.
La hiponatremia dilucional representa otra manifestación frecuente y clínicamente relevante. El aumento de vasopresina produce retención de agua libre desproporcionada respecto al sodio corporal total. Como resultado, la concentración plasmática de sodio disminuye progresivamente. La hiponatremia en cirrosis avanzada se asocia con peor pronóstico, mayor riesgo de encefalopatía hepática y mayor mortalidad perioperatoria en trasplante hepático. Además, refleja un grado avanzado de disfunción circulatoria sistémica.
El síndrome hepatorrenal históricamente se clasificaba en tipo 1 y tipo 2. Actualmente, la nomenclatura ha evolucionado hacia síndrome hepatorrenal asociado a lesión renal aguda, denominado HRS-AKI, y formas no asociadas a lesión renal aguda. El HRS-AKI corresponde al deterioro rápidamente progresivo de la función renal, mientras que las formas crónicas se relacionan con insuficiencia renal más estable pero persistente. Esta actualización diagnóstica permite identificar la enfermedad en etapas más tempranas y mejorar la oportunidad terapéutica.
El tratamiento del síndrome hepatorrenal se fundamenta en revertir las alteraciones hemodinámicas responsables de la hipoperfusión renal. La albúmina intravenosa constituye un componente esencial porque expande el volumen plasmático efectivo, incrementa el retorno venoso y mejora la perfusión arterial. Además de su función oncótica, la albúmina posee propiedades antioxidantes, antiinflamatorias y transportadoras de moléculas tóxicas. La expansión con albúmina también permite diferenciar hipovolemia verdadera de síndrome hepatorrenal auténtico.
La terlipresina es el vasoconstrictor más estudiado y actualmente uno de los tratamientos de elección. Se trata de un análogo sintético de vasopresina con afinidad predominante por receptores V1 vasculares. Su principal efecto consiste en inducir vasoconstricción esplácnica, reduciendo el secuestro sanguíneo en el territorio portal y aumentando el volumen arterial efectivo. Como consecuencia, disminuye la activación neurohormonal y mejora la perfusión renal. Diversos ensayos clínicos aleatorizados demostraron que la combinación de terlipresina y albúmina aumenta significativamente la reversión del síndrome hepatorrenal en comparación con albúmina sola.
El estudio CONFIRM, uno de los ensayos clínicos más importantes en esta enfermedad, evaluó 300 pacientes con síndrome hepatorrenal tipo 1 tratados con terlipresina más albúmina versus placebo más albúmina. La reversión confirmada del síndrome hepatorrenal ocurrió en 32% de los pacientes tratados con terlipresina comparado con 17% en el grupo placebo, demostrando beneficio significativo del tratamiento vasoconstrictor.
Sin embargo, la terlipresina no está exenta de riesgos. Debido a su potente acción vasoconstrictora puede producir isquemia periférica, arritmias, eventos cardiovasculares e insuficiencia respiratoria, particularmente en pacientes con sobrecarga de volumen o enfermedad cardiopulmonar avanzada. Por esta razón, su administración requiere vigilancia estrecha.
Otros vasoconstrictores utilizados incluyen noradrenalina y la combinación de midodrina con octreotida. La noradrenalina puede ser tan eficaz como la terlipresina en algunos contextos, especialmente en unidades de cuidados intensivos, aunque requiere administración intravenosa continua y monitorización hemodinámica.
El trasplante hepático continúa siendo el único tratamiento definitivo para el síndrome hepatorrenal porque corrige la hipertensión portal, la insuficiencia hepatocelular y las alteraciones circulatorias sistémicas subyacentes. Después del trasplante, muchos pacientes recuperan parcial o totalmente la función renal, especialmente cuando la duración de la insuficiencia renal previa ha sido corta. No obstante, en casos avanzados puede persistir daño renal irreversible.
El pronóstico del síndrome hepatorrenal es extremadamente grave. Sin tratamiento, la supervivencia media del HRS-AKI puede ser solamente de semanas. La aparición de insuficiencia renal en cirrosis avanzada indica descompensación sistémica severa y se asocia con elevada mortalidad hospitalaria. Por ello, el reconocimiento temprano, la identificación de factores precipitantes y el inicio rápido de tratamiento representan medidas esenciales para mejorar la supervivencia.

Fuente y lecturas recomendadas:
- Angeli, P., Ginès, P., Wong, F., Bernardi, M., Boyer, T. D., Gerbes, A., Moreau, R., Jalan, R., Sarin, S. K., Piano, S., Moore, K., Lee, S. S., Durand, F., Salerno, F., Caraceni, P., Kim, W. R., Garcia-Tsao, G., Trebicka, J., Gustot, T., … International Club of Ascites. (2015). Diagnosis and management of acute kidney injury in patients with cirrhosis: Revised consensus recommendations of the International Club of Ascites. Journal of Hepatology, 62(4), 968–974. https://doi.org/10.1016/j.jhep.2014.12.029
- Ginès, P., Solà, E., Angeli, P., Wong, F., Nadim, M. K., Kamath, P. S., & Moreau, R. (2018). Hepatorenal syndrome. Nature Reviews Disease Primers, 4, 23. https://doi.org/10.1038/s41572-018-0022-7
- Simonetto, D. A., Gines, P., Kamath, P. S., & Nadim, M. K. (2020). Hepatorenal syndrome: Pathophysiology and management. BMJ, 370, m2687. https://doi.org/10.1136/bmj.m2687
- Wong, F., Pappas, S. C., Curry, M. P., Reddy, K. R., Rubin, R. A., Porayko, M. K., Gonzalez, S. A., Mumtaz, K., Lim, N., Simonetto, D. A., Sharma, P., Sanyal, A. J., Mayo, M. J., Frederick, R. T., Escalante, S., Jamil, K., & CONFIRM Study Investigators. (2021). Terlipressin plus albumin for the treatment of type 1 hepatorenal syndrome. New England Journal of Medicine, 384(9), 818–828. https://doi.org/10.1056/NEJMoa2008290
- Fagundes, C., Barreto, R., Guevara, M., García, E., Solà, E., Rodríguez, E., Graupera, I., Ariza, X., Pereira, G., Alfaro, I., Cárdenas, A., Fernández, J., Poch, E., & Ginès, P. (2013). A modified acute kidney injury classification for diagnosis and risk stratification of impairment of kidney function in cirrhosis. Journal of Hepatology, 59(3), 474–481. https://doi.org/10.1016/j.jhep.2013.04.036
- Bernardi, M., Angeli, P., Claria, J., Moreau, R., Gines, P., Jalan, R., Caraceni, P., Fernández, J., Gerbes, A., O’Brien, A. J., Trebicka, J., Gustot, T., Arroyo, V., & European Foundation for the Study of Chronic Liver Failure Consortium. (2015). Albumin in decompensated cirrhosis: New concepts and perspectives. Gut, 64(7), 1147–1157. https://doi.org/10.1136/gutjnl-2014-308843