La parada circulatoria representa una de las formas más extremas de insuficiencia hemodinámica aguda, caracterizada por la interrupción completa del flujo sanguíneo sistémico. En esta situación cesa de manera inmediata el transporte de oxígeno y sustratos metabólicos hacia todos los tejidos del organismo, al mismo tiempo que se detiene la eliminación de dióxido de carbono, protones y metabolitos tóxicos. Aunque todos los órganos experimentan consecuencias graves, el cerebro constituye la estructura más vulnerable debido a su elevadísima demanda energética, su limitada capacidad de almacenamiento metabólico y su dependencia absoluta de un flujo sanguíneo continuo y estrictamente regulado. La lesión cerebral asociada con parada circulatoria constituye la principal causa de muerte y discapacidad neurológica en pacientes reanimados después de paro cardíaco.
El tejido nervioso consume aproximadamente el 20 % del oxígeno corporal total a pesar de representar solo cerca del 2 % de la masa corporal. Este consumo extraordinariamente elevado se debe a la intensa actividad electroquímica neuronal, especialmente al mantenimiento permanente de gradientes transmembrana de sodio, potasio y calcio mediante bombas iónicas dependientes de trifosfato de adenosina. Las neuronas poseen reservas energéticas mínimas y prácticamente carecen de capacidad significativa para almacenar glucógeno. Por ello, incluso períodos muy breves de interrupción circulatoria producen alteraciones funcionales inmediatas. La pérdida de conciencia ocurre generalmente entre 5 y 10 s después de la detención completa del flujo sanguíneo cerebral, debido al colapso rápido de la actividad eléctrica cortical.
Durante la parada circulatoria desaparece el aporte de oxígeno al encéfalo. La ausencia de oxígeno impide el funcionamiento normal de la cadena respiratoria mitocondrial y bloquea la fosforilación oxidativa, principal mecanismo de generación de trifosfato de adenosina en las neuronas. La caída de las concentraciones intracelulares de trifosfato de adenosina conduce rápidamente al fracaso energético celular. Como consecuencia, las bombas sodio-potasio adenosina trifosfatasa dejan de funcionar adecuadamente, permitiendo acumulación intracelular de sodio y pérdida de potasio hacia el espacio extracelular. El agua ingresa al interior de las neuronas siguiendo gradientes osmóticos, originando edema citotóxico y aumento del volumen celular.
Simultáneamente, se produce entrada masiva de calcio al interior neuronal. El calcio intracelular excesivo constituye uno de los principales mecanismos de destrucción celular porque activa proteasas, fosfolipasas, endonucleasas y otras enzimas degradativas capaces de destruir membranas celulares, proteínas estructurales, receptores y ácido desoxirribonucleico. La acumulación sostenida de calcio también induce apertura de poros de transición mitocondrial, agravando el fracaso energético y acelerando los procesos apoptóticos y necróticos.
Debido a la imposibilidad de obtener energía mediante metabolismo aeróbico, las células nerviosas recurren transitoriamente a la glucólisis anaerobia. Este mecanismo genera cantidades muy limitadas de trifosfato de adenosina y produce ácido láctico como metabolito final. El ácido láctico se acumula rápidamente en el tejido cerebral porque la ausencia de circulación impide su eliminación. Como consecuencia se desarrolla acidosis intracelular y extracelular severa. La acidosis altera la actividad enzimática, modifica la permeabilidad de membranas y favorece la desnaturalización de proteínas celulares.
Otro mecanismo central de lesión cerebral durante la parada circulatoria corresponde a la excitotoxicidad glutamatérgica. La falla energética altera el control de liberación y recaptación de neurotransmisores excitadores, particularmente glutamato. El exceso de glutamato estimula receptores ionotrópicos postsinápticos, especialmente receptores N-metil-D-aspartato, permitiendo ingreso masivo adicional de calcio y sodio al interior neuronal. Este fenómeno amplifica la lesión celular y favorece la muerte neuronal irreversible.
La susceptibilidad cerebral a la isquemia no es uniforme. Determinadas regiones encefálicas poseen vulnerabilidad particularmente elevada, entre ellas el hipocampo, la corteza cerebral, el estriado, el tálamo y las células de Purkinje cerebelosas. El hipocampo es especialmente sensible debido a su intensa actividad metabólica y elevada densidad de receptores glutamatérgicos excitadores. Por esta razón, muchos pacientes que sobreviven a una parada circulatoria prolongada presentan alteraciones prominentes de memoria, aprendizaje y funciones cognitivas superiores.
Históricamente se consideró que la hipoxia cerebral aguda era el único mecanismo responsable del daño neurológico asociado con parada circulatoria. Sin embargo, investigaciones posteriores demostraron que la fisiopatología es considerablemente más compleja y que las alteraciones microcirculatorias desempeñan un papel esencial. Entre estas alteraciones destaca el denominado fenómeno de “no reflujo”, descrito inicialmente en estudios experimentales de isquemia cerebral. Este fenómeno consiste en la incapacidad de reperfundir adecuadamente la microvasculatura cerebral incluso después de restaurar la permeabilidad de los grandes vasos y reiniciar la circulación sistémica.
El fenómeno de “no reflujo” implica que ciertas regiones cerebrales permanecen hipoperfundidas o completamente isquémicas a pesar del restablecimiento del latido cardíaco. Histológicamente aparecen múltiples defectos focales de perfusión capilar distribuidos en áreas cerebrales vulnerables. La magnitud de estos defectos aumenta proporcionalmente con la duración de la isquemia.
Diversos mecanismos contribuyen al desarrollo del fenómeno de “no reflujo”. Uno de los más importantes corresponde a la coagulación intravascular y la formación de microtrombos durante la estasis sanguínea. En condiciones normales, el flujo sanguíneo continuo mantiene dispersos los elementos formes y evita activación excesiva de la coagulación. Cuando la sangre permanece inmóvil dentro de los vasos cerebrales durante la parada circulatoria, desaparecen las fuerzas hemodinámicas que normalmente inhiben agregación plaquetaria y formación de trombos. Simultáneamente, el endotelio vascular sufre hipoxia y pierde sus propiedades anticoagulantes fisiológicas.
La activación de la coagulación conduce a formación de microtrombos de fibrina y agregados plaquetarios que obstruyen capilares y pequeñas arteriolas cerebrales. También participan neutrófilos adheridos al endotelio, agregados eritrocitarios y aumento de viscosidad sanguínea. Estas obstrucciones microvasculares impiden la reperfusión homogénea del tejido nervioso incluso después de recuperar circulación sistémica.
Estudios experimentales clásicos demostraron claramente la importancia de la coagulación intravascular en la lesión cerebral isquémica. En investigaciones realizadas por Crowell se extrajo la sangre de animales al inicio de la parada circulatoria y posteriormente se restituyó al finalizar el período isquémico. Debido a que la sangre no permaneció estancada dentro de los vasos, no se desarrolló coagulación intravascular significativa. Sorprendentemente, el cerebro pudo tolerar hasta aproximadamente 30 min de parada circulatoria sin daño neurológico permanente importante. Estos resultados demostraron que el daño cerebral no dependía exclusivamente de la hipoxia, sino también de la alteración microvascular secundaria a coagulación intravascular. Este hallazgo transformó profundamente la comprensión fisiopatológica de la lesión cerebral postisquémica.
Posteriormente se observó que la administración experimental de heparina o estreptocinasa antes de inducir parada cardíaca aumentaba significativamente la supervivencia cerebral. La heparina inhibe múltiples factores de coagulación y disminuye formación de fibrina, mientras la estreptocinasa favorece degradación fibrinolítica de trombos ya formados. Ambos mecanismos preservan la permeabilidad capilar y facilitan reperfusión más homogénea después del restablecimiento circulatorio.
Además de la coagulación, otros factores contribuyen al fenómeno de “no reflujo”. El edema de células endoteliales reduce el diámetro luminal capilar. Simultáneamente, los pericitos localizados alrededor de capilares cerebrales pueden contraerse intensamente durante la isquemia y permanecer en contracción sostenida tras la reperfusión, comprimiendo mecánicamente la microvasculatura. También intervienen edema intersticial, alteración de la barrera hematoencefálica y reacción inflamatoria postisquémica.
La reperfusión cerebral posterior a la parada circulatoria, aunque indispensable para la supervivencia tisular, también puede desencadenar lesión secundaria importante. El restablecimiento brusco del aporte de oxígeno favorece generación masiva de especies reactivas de oxígeno, incluyendo radical superóxido, radical hidroxilo y peróxido de hidrógeno. Estas moléculas producen peroxidación lipídica, oxidación proteica y daño del ácido desoxirribonucleico. La lesión oxidativa agrava la disfunción mitocondrial y acelera la muerte celular.
Paralelamente, la reperfusión induce intensa respuesta inflamatoria sistémica y cerebral. Los leucocitos activados migran hacia el tejido nervioso y liberan citocinas proinflamatorias, proteasas y radicales libres. El endotelio vascular aumenta su permeabilidad, favoreciendo extravasación de proteínas plasmáticas y formación de edema cerebral. El incremento de presión intracraneal compromete todavía más la perfusión cerebral y perpetúa el daño neuronal.
Actualmente se considera que la lesión cerebral asociada con parada cardíaca ocurre mediante un modelo fisiopatológico de “doble impacto”. El primer impacto corresponde a la interrupción inmediata del flujo sanguíneo y la hipoxia global cerebral. El segundo impacto ocurre durante las horas y días posteriores al restablecimiento circulatorio, cuando predominan mecanismos de lesión secundaria como reperfusión, inflamación, disfunción microvascular, edema cerebral, alteración de autorregulación cerebral y estrés oxidativo.
La duración de la parada circulatoria constituye el principal determinante pronóstico. Generalmente, más de 5 a 8 min de ausencia completa de flujo sanguíneo cerebral producen lesión neurológica permanente en una proporción considerable de pacientes. Períodos de 10 a 15 min suelen ocasionar destrucción extensa de neuronas corticales y profundas, con deterioro irreversible de funciones cognitivas y neurológicas superiores.
La hipotermia terapéutica puede aumentar la tolerancia cerebral a la isquemia porque reduce el metabolismo neuronal, disminuye consumo de oxígeno y atenúa formación de radicales libres y liberación excitotóxica de glutamato. Este principio explica la utilidad clínica del control dirigido de temperatura en pacientes reanimados después de paro cardíaco.
La reanimación cardiopulmonar temprana constituye la medida más importante para prevenir lesión cerebral irreversible. Aunque las compresiones torácicas generan solo una fracción del flujo sanguíneo normal, este flujo parcial puede retrasar el agotamiento energético neuronal y prolongar la viabilidad cerebral hasta lograr desfibrilación o recuperación de circulación espontánea. La desfibrilación precoz resulta especialmente importante en fibrilación ventricular porque permite restaurar actividad cardíaca efectiva antes de que el daño neurológico alcance un punto irreversible.
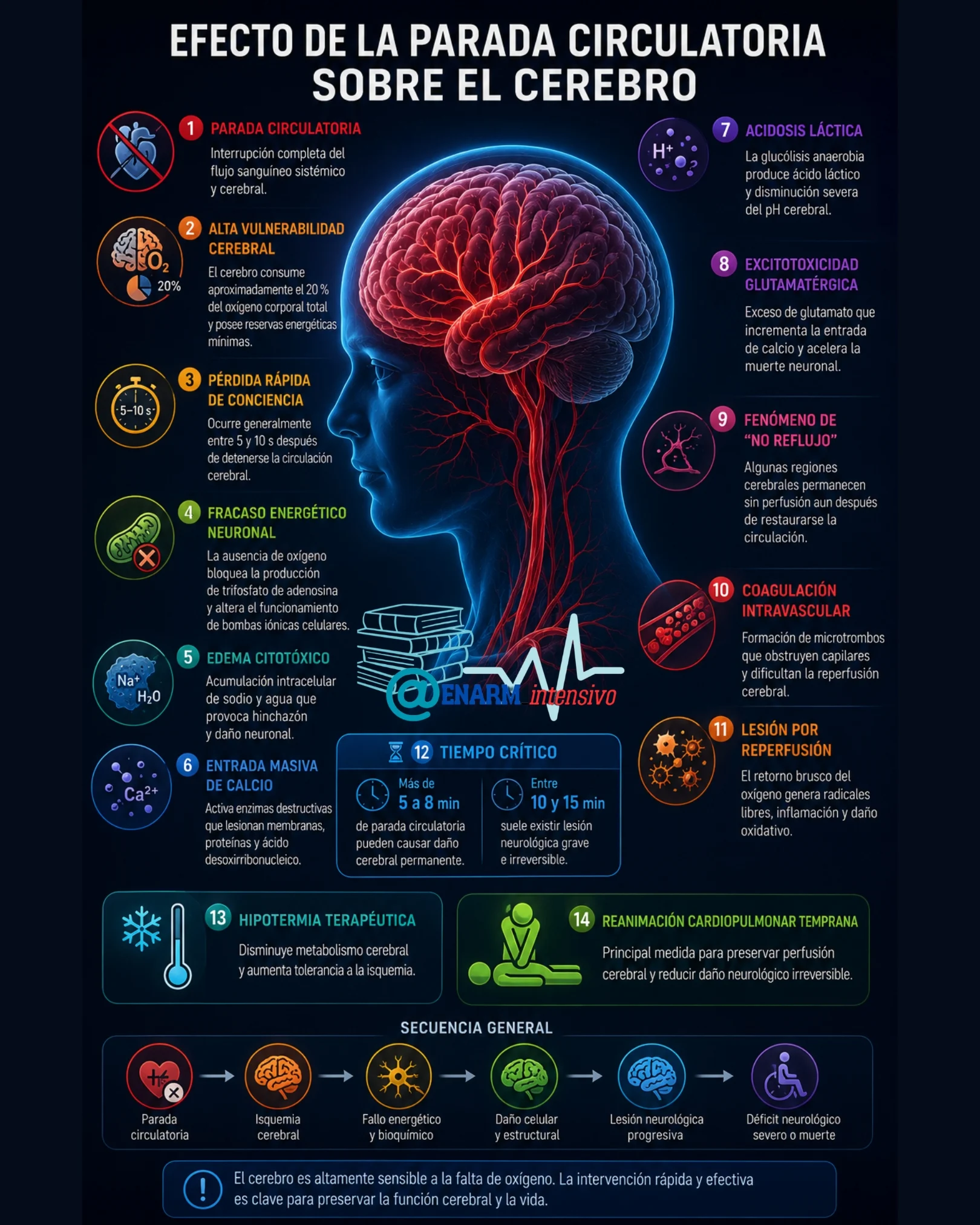
El efecto de la parada circulatoria sobre el cerebro constituye un fenómeno fisiopatológico extraordinariamente complejo en el que participan hipoxia, fracaso energético, alteración iónica, edema citotóxico, acidosis láctica, excitotoxicidad glutamatérgica, coagulación intravascular, fenómeno de “no reflujo”, inflamación y lesión oxidativa por reperfusión. El cerebro posee una tolerancia extremadamente limitada a la interrupción circulatoria debido a sus elevadas demandas metabólicas y a la ausencia de reservas energéticas significativas. Las investigaciones modernas demostraron que el daño cerebral no depende exclusivamente de la privación de oxígeno, sino también de alteraciones microvasculares persistentes que impiden reperfusión adecuada aun después de restablecer la circulación sistémica. Estos conocimientos han fundamentado el desarrollo de estrategias modernas de reanimación, anticoagulación, neuroprotección y control de temperatura orientadas a preservar la función cerebral después de la parada circulatoria.

Fuente y lecturas recomendadas:
- Ames, A., Wright, R. L., Kowada, M., Thurston, J. M., & Majno, G. (1968). Cerebral ischemia. II. The no-reflow phenomenon. The American Journal of Pathology, 52(2), 437–453.
- Bottiger, B. W., Krumnikl, J. J., Gass, P., Schmitz, B., Motsch, J., Martin, E., & Teschendorf, P. (1997). The cerebral no-reflow phenomenon after cardiac arrest in rats: Influence of low-flow reperfusion. Resuscitation, 34(1), 79–87. https://doi.org/10.1016/S0300-9572(96)01029-5
- Kloner, R. A., King, K. S., & Harrington, M. G. (2018). No-reflow phenomenon in the heart and brain. American Journal of Physiology-Heart and Circulatory Physiology, 315(3), H550–H562. https://doi.org/10.1152/ajpheart.00183.2018
- Luo, X., Zhang, S., Wang, L., & Li, J. (2024). Pathological roles of mitochondrial dysfunction in endothelial cells during the cerebral no-reflow phenomenon: A review. Medicine, 103(51), e40951. https://doi.org/10.1097/MD.0000000000040951
- Sandroni, C., Cronberg, T., & Sekhon, M. (2021). Brain injury after cardiac arrest: Pathophysiology, treatment, and prognosis. Intensive Care Medicine, 47(12), 1393–1414. https://doi.org/10.1007/s00134-021-06548-2
- Schaller, B., & Graf, R. (2004). Cerebral ischemia and reperfusion: The pathophysiologic concept as a basis for clinical therapy. Journal of Cerebral Blood Flow & Metabolism, 24(4), 351–371. https://doi.org/10.1097/00004647-200404000-00001
- Sekhon, M. S., Ainslie, P. N., & Griesdale, D. E. (2017). Clinical pathophysiology of hypoxic ischemic brain injury after cardiac arrest: A two-hit model. Critical Care, 21(1), 90. https://doi.org/10.1186/s13054-017-1670-9
- Wada, T. (2017). Coagulofibrinolytic changes in patients with post-cardiac arrest syndrome. Frontiers in Medicine, 4, 156. https://doi.org/10.3389/fmed.2017.00156
- Zhang, Y., Jiang, M., Gao, Y., Zhao, W., Wu, C., Li, C., Li, M., Wu, D., Wang, W., & Ji, X. (2024). No-reflow phenomenon in acute ischemic stroke. Journal of Cerebral Blood Flow & Metabolism, 44(1), 3–20. https://doi.org/10.1177/0271678X231208476