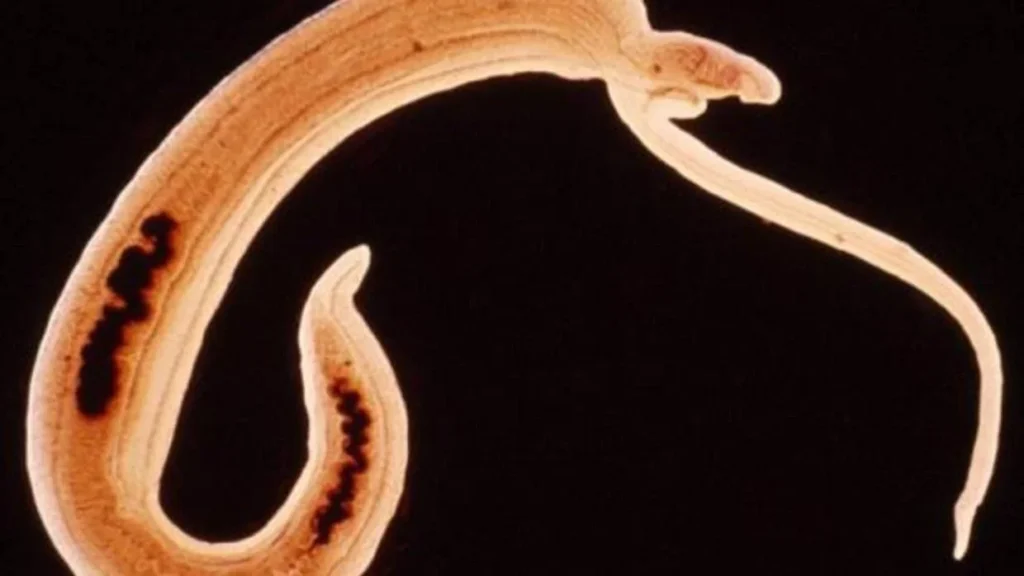
La esquistosomiasis es una enfermedad parasitaria grave que afecta a un considerable número de personas en diversas regiones del mundo, particularmente en áreas rurales y empobrecidas de África, Asia y América Latina. La enfermedad es provocada por seis especies de trematodos del género Schistosoma, conocidas como duelas sanguíneas, que parasitan el sistema circulatorio humano. De estas especies, cinco están implicadas en la esquistosomiasis intestinal, al infectar las vénulas mesentéricas, mientras que la sexta causa la esquistosomiasis urinaria al afectar las vénulas del tracto urinario.
Entre las especies responsables de la esquistosomiasis intestinal se encuentran:
- Schistosoma mansoni, endémico en África, la península arábiga, Sudamérica y el Caribe.
- Schistosoma japonicum, presente en China y en varios países del sudeste asiático.
- Schistosoma mekongi, que se localiza cerca del río Mekong en el sudeste asiático.
- Schistosoma intercalatum y Schistosoma guineensis, que habitan ciertas regiones de África.
Por otro lado, la esquistosomiasis urinaria es causada por Schistosoma haematobium, que afecta predominantemente a las vénulas del tracto urinario y es endémico en África y en algunos países del Medio Oriente.
La prevalencia global de la esquistosomiasis afecta a más de 200 millones de personas, con alrededor de 20 millones que experimentan consecuencias graves, y unas 100,000 muertes anuales relacionadas con la enfermedad. Este impacto es especialmente pronunciado en zonas de alta transmisión, donde las condiciones sanitarias son precarias y el acceso a tratamientos es limitado. Aunque los esfuerzos de control han logrado reducir la transmisión en muchas regiones, en algunas áreas de África subsahariana y otras localizaciones endémicas persiste una alta carga de la enfermedad.
La transmisión de la esquistosomiasis está íntimamente relacionada con el contacto de los seres humanos con agua dulce contaminada por cercarias, que son las formas larvales del parásito. Estos parásitos se liberan por los caracoles infectados, los cuales actúan como hospedadores intermediarios. Al entrar en contacto con el agua contaminada, las cercarias penetran la piel o las membranas mucosas de los individuos, lo que marca el inicio de la infección.
Una vez que las cercarias atraviesan la piel, se convierten en esquistosómulas, que migran rápidamente a través del sistema circulatorio hasta alcanzar la circulación portal, donde maduran y se transforman en gusanos adultos. Tras un periodo de aproximadamente seis semanas, los parásitos adultos se aparean y migran a las vénulas mesentéricas o vesicales, dependiendo de la especie involucrada. Las hembras depositan sus huevos en estas zonas, y algunos de estos huevos alcanzan la luz del intestino o la vejiga, siendo eliminados por las heces o la orina. Sin embargo, otros huevos quedan atrapados en los tejidos, principalmente en la pared intestinal o vesical, y pueden ser transportados a otros órganos, siendo el hígado uno de los destinos más comunes debido a su conexión con la circulación portal.
El daño patológico causado por la esquistosomiasis en las áreas endémicas está vinculado principalmente a la respuesta inmunitaria del huésped ante los huevos depositados en los tejidos. El cuerpo reacciona formando granulomas alrededor de los huevos, lo que provoca inflamación crónica. Con el tiempo, esta inflamación puede llevar a fibrosis, un proceso de cicatrización que afecta tanto a los vasos sanguíneos mesentéricos como al tracto urinario. En el caso de la esquistosomiasis intestinal, la fibrosis de las vénulas mesentéricas puede causar hipertensión portal, mientras que en la esquistosomiasis urinaria, la obstrucción y cicatrización del tracto urinario puede resultar en disfunción renal y otras complicaciones urológicas.
Además de la infección crónica, las personas que no han estado previamente expuestas al parásito, como los viajeros que visitan áreas endémicas y entran en contacto con agua contaminada, pueden experimentar esquistosomiasis aguda. Esta forma de la enfermedad se manifiesta típicamente con un cuadro febril entre dos y ocho semanas después de la infección, y puede ser acompañada de otros síntomas como dolor abdominal, diarrea o urticaria.
En resumen, la esquistosomiasis es una enfermedad parasitaria compleja con implicaciones de salud significativas en regiones endémicas. La interacción entre el parásito y el huésped humano lleva a una serie de respuestas inmunológicas que, a largo plazo, causan daño a órganos vitales. Aunque los esfuerzos de control han reducido la transmisión en algunas regiones, la enfermedad sigue siendo un problema de salud pública en muchas partes del mundo, particularmente en áreas con condiciones socioeconómicas desfavorecidas y acceso limitado a servicios médicos adecuados.
Manifestaciones clínicas
La esquistosomiasis es una enfermedad parasitaria que se manifiesta a través de una variedad de signos y síntomas que varían según la fase de la infección y la especie del Schistosoma involucrada. Los síntomas pueden ir desde reacciones locales leves hasta complicaciones graves y crónicas que afectan diversos órganos. A continuación, se describen las principales manifestaciones clínicas de la enfermedad.
Dermatitis cercarial (prurito del nadador)
Una de las primeras reacciones que puede experimentarse tras la penetración de las cercarias en la piel es la dermatitis cercarial, también conocida como «prurito del nadador». Este síntoma ocurre típicamente poco después del contacto con agua dulce contaminada por cercarias. Las personas afectadas pueden desarrollar un eritema localizado en la zona de penetración, que puede progresar a una erupción maculopapular pruriginosa. Este cuadro clínico generalmente persiste entre varios días y una semana. Aunque este tipo de dermatitis es más comúnmente asociado con esquistosomas humanos, en zonas no tropicales también puede ser provocada por especies de Schistosoma que infectan aves, las cuales no pueden completar su ciclo de vida en humanos. En este caso, la reacción es menos grave, pero igualmente causa un prurito molesto.
Esquistosomiasis aguda (síndrome de Katayama)
La esquistosomiasis aguda, también conocida como síndrome de Katayama, se presenta entre dos y ocho semanas después de la exposición al parásito, particularmente en individuos que no han sido previamente infectados. Esta fase aguda de la enfermedad es más común tras infecciones intensas causadas por Schistosoma mansoni o Schistosoma japonicum. Los síntomas incluyen fiebre de inicio súbito, cefalea, mialgias (dolores musculares), tos persistente, malestar general y urticaria. También pueden observarse diarrea, que en algunos casos es sanguinolenta, así como hepatoesplenomegalia (aumento simultáneo de tamaño del hígado y el bazo), linfadenopatía (agrandamiento de los ganglios linfáticos) e infiltrados pulmonares. En raras ocasiones, la esquistosomiasis aguda puede provocar manifestaciones graves, que incluyen alteraciones en el sistema nervioso central e incluso la muerte. Sin embargo, en la mayoría de los casos, la esquistosomiasis aguda se resuelve espontáneamente en un periodo que va de dos a ocho semanas, sin dejar secuelas a largo plazo.
Esquistosomiasis crónica
En su forma crónica, la esquistosomiasis se presenta como una infección persistente que puede permanecer asintomática durante mucho tiempo. Se estima que entre el 50 % y el 60 % de las personas infectadas no desarrollan síntomas evidentes, mientras que un 5 % a 10 % puede presentar daño orgánico avanzado. Es importante destacar que, aunque muchos individuos infectados no experimentan síntomas inmediatos, los niños que se infectan de manera asintomática pueden sufrir de anemia y retraso en el crecimiento, lo que afecta su desarrollo físico y cognitivo.
Los pacientes con esquistosomiasis intestinal, que es la forma más común en regiones endémicas, suelen presentar síntomas como dolor abdominal crónico, diarrea, fatiga y hepatomegalia (aumento del tamaño del hígado). A medida que la enfermedad progresa, pueden desarrollarse problemas más graves, como anorexia, pérdida de peso, debilidad generalizada, pólipos colónicos e hipertensión portal. La hipertensión portal es una complicación que ocurre cuando la presión en la circulación portal (que transporta la sangre desde los intestinos hacia el hígado) aumenta debido a la fibrosis de los vasos sanguíneos mesentéricos. Esta condición puede llevar a sangrados graves, como hematemesis (vómitos con sangre) debido a las várices esofágicas, insuficiencia hepática y, en casos avanzados, hipertensión pulmonar.
Esquistosomiasis urinaria
La esquistosomiasis urinaria es causada por Schistosoma haematobium, que infecta las vénulas del tracto urinario, y suele manifestarse pocos meses después de la infección primaria. Los síntomas típicos incluyen hematuria (presencia de sangre en la orina) y disuria (dolor o dificultad al orinar), siendo más comunes en niños y adultos jóvenes. Si la infección persiste, los cambios fibróticos en el tracto urinario pueden generar complicaciones más graves, como hidroureter (dilatación de los uréteres), hidronefrosis (dilatación de los riñones debido a la obstrucción de la orina) e infecciones urinarias bacterianas recurrentes. En los casos más avanzados, esta forma de esquistosomiasis puede provocar enfermedad renal crónica y un mayor riesgo de cáncer de vejiga.
Esquistosomiasis genital crónica
En las fases más crónicas de la esquistosomiasis urinaria, las personas pueden desarrollar complicaciones adicionales que afectan el sistema genital. Estas manifestaciones incluyen lesiones locales en los órganos reproductivos y un mayor riesgo de incontinencia urinaria, infertilidad y una mayor susceptibilidad a la infección por el virus de la inmunodeficiencia humana (VIH). Las mujeres, en particular, pueden experimentar cambios en los tejidos genitales que facilitan la transmisión del VIH durante las relaciones sexuales.
Exámenes diagnósticos
El diagnóstico de esquistosomiasis se basa en una serie de métodos que permiten identificar la presencia del parásito o sus productos biológicos en el organismo, confirmando la infección y evaluando su extensión. La identificación de los huevos característicos del Schistosoma en muestras biológicas, como heces u orina, constituye el pilar fundamental del diagnóstico. Además, existen varias pruebas complementarias que incluyen la evaluación de tejidos, pruebas serológicas y, en algunos casos, biopsias, para proporcionar un diagnóstico preciso y una evaluación detallada de la enfermedad.
Examen microscópico de heces o orina
La observación microscópica de heces o orina en busca de huevos es el método diagnóstico estándar en la esquistosomiasis. Los huevos de Schistosoma tienen características morfológicas particulares que permiten su identificación bajo el microscopio. En el caso de la esquistosomiasis intestinal, los huevos de Schistosoma mansoni son los más comunes, y tienen una espícula prominente en un extremo, mientras que los de Schistosoma japonicum son más redondeados y carecen de esta espícula. Los huevos de Schistosoma haematobium, responsables de la esquistosomiasis urinaria, se identifican por su espícula en el extremo opuesto al extremo de la cápsula.
La prueba de heces más utilizada para la detección de estos huevos es la técnica de Kato-Katz, que permite examinar un frotis de heces bajo el microscopio para contar la cantidad de huevos presentes. Esta técnica es relativamente simple y eficiente, aunque su sensibilidad depende de la cantidad de huevos eliminados, lo que puede variar a lo largo del tiempo. El recuento de huevos es un indicador clave para determinar la intensidad de la infección. Se considera que una infección es intensa si se detectan más de 400 huevos por gramo de heces, o si la orina contiene más de 10 mL de muestra con alta concentración de huevos, lo que indica un mayor riesgo de complicaciones y una enfermedad más avanzada.
Evaluación de tejidos y biopsias
En casos más complejos o cuando los huevos no se detectan fácilmente en heces u orina, se puede recurrir a la evaluación de tejidos afectados por la infección. Las biopsias de tejidos como el recto, el colon, el hígado o la vejiga pueden proporcionar información valiosa sobre la presencia del parásito. En algunos casos, las lesiones granulomatosas causadas por la respuesta inmunitaria a los huevos del Schistosoma pueden ser evidentes en los tejidos afectados, lo que también puede ayudar a confirmar el diagnóstico.
Pruebas serológicas
Las pruebas serológicas, que detectan la presencia de anticuerpos contra el parásito, son otra herramienta útil en el diagnóstico de la esquistosomiasis. El ensayo inmunoenzimático (ELISA) es uno de los métodos más utilizados en los Centros para el Control y la Prevención de Enfermedades (CDC) y tiene una especificidad muy alta, superior al 99 % para todas las especies de Schistosoma. Sin embargo, no distingue entre infecciones pasadas y actuales, lo que limita su utilidad en áreas endémicas. La sensibilidad varía según la especie de Schistosoma: es muy alta para Schistosoma mansoni(99 %), moderada para Schistosoma haematobium (95 %) y baja para Schistosoma japonicum (menos del 50 %).
Aunque la serología no es tan útil en regiones endémicas debido a la alta prevalencia de infecciones previas, puede ser particularmente valiosa para diagnosticar esquistosomiasis en viajeros que provienen de áreas no endémicas, donde las infecciones son menos comunes. Las pruebas serológicas pueden volverse positivas antes de que los huevos sean detectados en muestras biológicas, lo que ofrece una ventaja en etapas tempranas de la infección.
Pruebas de antígeno
Las pruebas de antígeno circulante, que detectan proteínas específicas liberadas por los esquistosomas en el suero o la orina, son otra opción de diagnóstico. Estas pruebas tienen una mayor sensibilidad que los frotis de heces, especialmente para Schistosoma mansoni, y se utilizan con frecuencia para detectar infecciones en personas que han sido recientemente infectadas. Sin embargo, la sensibilidad de estas pruebas es más baja para Schistosoma haematobium, lo que las hace menos útiles en el diagnóstico de esquistosomiasis urinaria. Estas pruebas también son útiles para evaluar la carga parasitaria en individuos infectados y para determinar la respuesta al tratamiento, ya que la cantidad de antígenos circulantes puede disminuir con la eliminación del parásito.
Pruebas moleculares
Aunque las pruebas moleculares, como la PCR (reacción en cadena de la polimerasa), han mostrado un gran potencial en la detección de esquistosomiasis al identificar el ADN del parásito, actualmente no se utilizan de manera rutinaria en la práctica clínica. Estas pruebas son altamente sensibles y específicas, pero su costo y la complejidad técnica de su implementación las hacen menos viables para el diagnóstico rutinario en áreas endémicas.
Esquistosomiasis aguda
En la fase aguda de la enfermedad, también conocida como síndrome de Katayama, las pruebas serológicas pueden volverse positivas antes de que los huevos sean detectados en las muestras de heces u orina. Esto se debe a la respuesta inmunitaria que se genera en el cuerpo tras la penetración de las cercarias y la maduración de los esquistosomas. En esta fase, puede haber una leucocitosis (aumento del número de glóbulos blancos) y eosinofilia (aumento de los eosinófilos, un tipo de glóbulo blanco asociado a infecciones parasitarias), lo que también puede contribuir al diagnóstico temprano, aunque no siempre es concluyente.
Identificación de huevos después del tratamiento
Después de que un paciente recibe tratamiento para la esquistosomiasis, los huevos pueden continuar siendo excretados en heces o orina durante varios meses. Este fenómeno debe tenerse en cuenta durante el seguimiento, ya que la presencia de huevos en muestras biológicas no siempre indica una infección activa. En consecuencia, la identificación de huevos en fluidos o tejidos no es suficiente para diferenciar entre enfermedad activa o pasada, lo que requiere de pruebas adicionales, como la medición de antígenos o la evaluación clínica de los síntomas del paciente.
Evaluación de la extensión de la enfermedad
Una vez confirmado el diagnóstico de esquistosomiasis, es crucial evaluar la extensión de la enfermedad, ya que las complicaciones pueden ser graves si no se tratan adecuadamente. Para la esquistosomiasis intestinal, se recomienda realizar pruebas de función hepática y realizar estudios de imagen, como ecografías, para examinar el estado del hígado y evaluar posibles daños como la fibrosis o la hipertensión portal. En casos de esquistosomiasis urinaria, las ecografías y otros estudios de imagen del aparato urinario pueden ser necesarios para detectar alteraciones como hidronefrosis, cáncer de vejiga o insuficiencia renal.
Tratamiento
El tratamiento de la esquistosomiasis es esencial para reducir la carga parasitaria y prevenir las complicaciones graves que pueden surgir a medida que la enfermedad progresa. En regiones donde la reinfección es frecuente, el tratamiento tiene un papel fundamental no solo en la erradicación de los esquistosomas existentes, sino también en la limitación de las secuelas clínicas a largo plazo. Este enfoque terapéutico es crucial para minimizar la morbilidad asociada a la esquistosomiasis, que afecta principalmente a órganos vitales como el hígado, el tracto urinario y, en algunos casos, el sistema nervioso central.
Fármaco de elección: prazicuantel
El fármaco de primera línea para el tratamiento de la esquistosomiasis es el prazicuantel, un agente antilipídico que se administra por vía oral. El prazicuantel tiene un espectro de acción amplio y es eficaz contra las diferentes especies de Schistosoma que causan la esquistosomiasis en humanos. Dependiendo de la especie de esquistosoma, la dosis varía: para Schistosoma mansoni, Schistosoma haematobium, Schistosoma intercalatum y Schistosoma guineensis, se administra una dosis de 40 mg por kilogramo de peso corporal en una o dos tomas. En el caso de Schistosoma japonicum y Schistosoma mekongi, la dosis recomendada es de 60 mg por kilogramo de peso corporal, dividida en dos o tres tomas. Esta dosificación es fundamental para garantizar la máxima eficacia del tratamiento.
Una de las características destacadas del prazicuantel es su alta tasa de curación, que generalmente supera el 80 % tras una sola dosis. Sin embargo, en aquellos casos en los que el tratamiento no logra erradicar completamente la infección, se observa una reducción significativa en la intensidad de la misma. Esto implica que el fármaco, aunque no curativo en algunos casos, sigue siendo eficaz para aliviar los síntomas y minimizar el daño orgánico relacionado con la infección.
Mecanismo de acción del prazicuantel
El prazicuantel actúa de manera eficaz contra las cercarias invasoras, las cuales son las formas larvales que penetran en la piel del huésped y se convierten en esquistosómulas, la etapa inicial de desarrollo de los gusanos adultos. No obstante, el fármaco no es efectivo contra las esquistosómulas en desarrollo ni contra los huevos ya depositados en los tejidos. Por esta razón, si se administra de forma temprana, tras la exposición a cercarias, el prazicuantel puede no prevenir el inicio de la enfermedad, ya que la invasión por los esquistosomas puede ya haber ocurrido antes de que el fármaco sea administrado. En infecciones recientes, se puede recomendar un tratamiento repetido tras unas semanas para asegurar la eliminación de las formas adultas de los parásitos.
Uso en el embarazo y efectos secundarios
El prazicuantel se considera seguro para su uso durante el embarazo, lo que lo convierte en el fármaco de elección en mujeres embarazadas que sufren de esquistosomiasis, especialmente en áreas endémicas donde la infección es prevalente. Sin embargo, como ocurre con la mayoría de los medicamentos, el prazicuantel no está exento de efectos secundarios. Estos incluyen dolor abdominal, diarrea, urticaria, cefalea, náuseas, vómitos y fiebre. Estos efectos pueden ser atribuibles tanto a la acción directa del fármaco sobre los gusanos adultos como a la respuesta inmunológica del organismo ante la muerte de los parásitos. En general, estos efectos son transitorios y suelen desaparecer una vez que el cuerpo se adapta al tratamiento.
Terapias alternativas
Aunque el prazicuantel es el tratamiento estándar, existen terapias alternativas para algunas especies de Schistosoma. La oxamniquina es eficaz para el tratamiento de infecciones por Schistosoma mansoni, mientras que el metrifonato se utiliza para infecciones por Schistosoma haematobium. Sin embargo, estos medicamentos tienen disponibilidad limitada y no se encuentran disponibles en países como los Estados Unidos. Además, la resistencia a estos fármacos es una preocupación creciente, lo que limita su uso en ciertas regiones.
Para Schistosoma japonicum, no existe un tratamiento alternativo ampliamente disponible, lo que complica el manejo de la esquistosomiasis causada por esta especie.
Arteméter y su uso en quimioprofilaxis
El arteméter, un medicamento utilizado principalmente en el tratamiento de la malaria, ha mostrado actividad contra las esquistosómulas y los gusanos adultos, lo que sugiere que podría ser útil en la quimioprofilaxis de la esquistosomiasis, especialmente en áreas donde tanto la malaria como la esquistosomiasis son endémicas. Sin embargo, el arteméter es costoso y su uso prolongado en zonas donde la malaria es endémica puede resultar en la selección de cepas de Plasmodium resistentes, lo que podría empeorar la situación epidemiológica.
Uso de corticosteroides en casos graves
En los casos más graves de esquistosomiasis, cuando la enfermedad ha causado complicaciones significativas como inflamación severa, fibrosis u obstrucción de órganos, se puede considerar el uso de corticosteroides. Estos medicamentos pueden ayudar a reducir la inflamación y las complicaciones asociadas, especialmente cuando se administran junto con prazicuantel. El uso de corticosteroides debe ser cuidadosamente monitoreado debido a los posibles efectos secundarios, como la inmunosupresión.
Seguimiento post-tratamiento
Después de recibir tratamiento, se recomienda que los pacientes sean monitoreados a través de exámenes repetidos de heces o orina para detectar la presencia de huevos. Esto debe hacerse cada tres meses durante al menos un año, ya que los huevos pueden seguir siendo excretados durante varios meses después de que el tratamiento haya tenido lugar. Si los huevos son detectados durante el seguimiento, se debe considerar un nuevo ciclo de tratamiento para garantizar la erradicación completa de la infección.
Prevención
La esquistosomiasis es una enfermedad transmitida por parásitos, cuyo ciclo de vida involucra a los caracoles de agua dulce, que liberan cercarias, las formas larvales del parásito, en cuerpos de agua. Los viajeros que se desplazan a zonas endémicas, donde la esquistosomiasis es prevalente, corren el riesgo de infectarse si tienen contacto con agua dulce contaminada. Por esta razón, es esencial que los viajeros a estas áreas eviten cualquier tipo de contacto con agua dulce, como ríos, lagos o embalses, ya que la exposición a estos ambientes incrementa significativamente el riesgo de adquirir la infección.
Prevención a través del secado energético
Una estrategia recomendada para los viajeros que, por diversas razones, puedan haber tenido contacto con agua dulce en zonas endémicas es secarse enérgicamente con una toalla inmediatamente después de la exposición. El secado rápido de la piel reduce la probabilidad de que las cercarias, que ya se han adherido a la epidermis, puedan penetrar y completar su ciclo de vida dentro del huésped. Aunque esta medida no garantiza la completa protección contra la infección, puede disminuir la posibilidad de que las cercarias atraviesen la barrera de la piel, lo que constituye el primer paso en la infección.
Quimioprofilaxis con arteméter
En cuanto a la quimioprofilaxis, se ha investigado el uso de ciertos medicamentos como el arteméter para prevenir la infección en individuos que viajan a zonas endémicas. El arteméter, un fármaco utilizado principalmente para el tratamiento de la malaria, ha demostrado cierta eficacia contra las esquistosómulas, que son las formas larvales que invaden al huésped después del contacto con las cercarias. Este fármaco podría, en teoría, ayudar a reducir la probabilidad de infección si se administra antes de la exposición o poco después de la misma. Sin embargo, el uso de arteméter como medida preventiva no es una práctica estándar ni ampliamente recomendada, principalmente por su costo elevado y la falta de estudios a largo plazo que respalden su eficacia y seguridad en la prevención de la esquistosomiasis.
Control comunitario de la esquistosomiasis
El control de la esquistosomiasis no solo depende de medidas individuales como evitar el contacto con agua dulce, sino que también requiere de un enfoque comunitario integral que aborde las condiciones ambientales y de infraestructura en las zonas endémicas. Las principales estrategias de control incluyen:
- Mejoras en el saneamiento y el suministro de agua: La esquistosomiasis está estrechamente vinculada a la calidad del agua en las zonas rurales, donde el acceso a agua potable y servicios de saneamiento es limitado. La contaminación del agua por los huevos del Schistosoma, excretados en las heces y la orina de personas infectadas, favorece la proliferación de los caracoles intermediarios que hospician a las cercarias. Mejorar el acceso a agua potable y las condiciones sanitarias, como la instalación de sistemas de alcantarillado y la promoción de prácticas de higiene, reduce significativamente la contaminación del agua y, por ende, disminuye el riesgo de transmisión del parásito.
- Eliminación de hábitats de caracoles: Los caracoles de agua dulce actúan como hospedadores intermedios esenciales para el ciclo de vida del Schistosoma. En zonas endémicas, la eliminación de los hábitats naturales de estos caracoles, como la modificación de cuerpos de agua estancados o la introducción de medidas de control biológico, puede reducir la cantidad de caracoles disponibles para albergar las cercarias. Esto limita la cantidad de parásitos disponibles para infectar a los humanos y, en consecuencia, disminuye la transmisión de la enfermedad.
- Tratamiento preventivo masivo: El tratamiento masivo preventivo, en el que se administran medicamentos antiparasitarios, como el prazicuantel, a toda la población en zonas endémicas, es una estrategia clave para reducir la carga parasitaria y la prevalencia de la esquistosomiasis. Este enfoque tiene como objetivo eliminar la infección en aquellos individuos que aún no presentan síntomas, pero que pueden ser portadores del parásito y actuar como fuente de infección para otros. Aunque esta medida no erradica por completo la enfermedad, reduce significativamente el riesgo de transmisión y mejora la salud pública en general.
El tratamiento preventivo debe ser parte de un programa integral que combine estas intervenciones con la educación comunitaria sobre los riesgos de la esquistosomiasis, el acceso a servicios de salud y el monitoreo regular de la prevalencia de la enfermedad. Estos esfuerzos coordinados no solo disminuyen la carga parasitaria en la población, sino que también contribuyen a un control sostenido de la esquistosomiasis en regiones endémicas.

Fuente y lecturas recomendadas:
- Goldman, L., & Schafer, A. I. (Eds.). (2020). Goldman-Cecil Medicine (26th ed.). Elsevier.
- Loscalzo, J., Fauci, A. S., Kasper, D. L., Hauser, S. L., Longo, D. L., & Jameson, J. L. (Eds.). (2022). Harrison. Principios de medicina interna (21.ª ed.). McGraw-Hill Education.
- Papadakis, M. A., McPhee, S. J., Rabow, M. W., & McQuaid, K. R. (Eds.). (2024). Diagnóstico clínico y tratamiento 2025. McGraw Hill.
- Rozman, C., & Cardellach López, F. (Eds.). (2024). Medicina interna (20.ª ed.). Elsevier España.
- Aula OP et al. Schistosomiasis with a focus on Africa. Trop Med Infect Dis. 2021;6:109. [PMID: 34206495] Carbonell C et al. Clinical spectrum of schistosomiasis: an update. J Clin Med. 2021;10:5521. [PMID: 34884223]