Las mordeduras de arañas y picaduras escorpiones representan un modelo biológico particularmente ilustrativo de cómo los venenos animales han evolucionado como mezclas complejas de moléculas bioactivas capaces de interactuar con sistemas fisiológicos humanos altamente conservados. Desde una perspectiva de la toxicología molecular y la fisiopatología, estos venenos no son simplemente sustancias irritantes, sino combinaciones específicas de proteínas, péptidos y enzimas con blancos celulares bien definidos, lo cual explica la diversidad de manifestaciones clínicas observadas.
En la mayoría de las especies de arañas y escorpiones, el efecto de la “picadura” permanece confinado al sitio de inoculación. Este fenómeno se explica por la baja potencia sistémica del veneno y por su difusión limitada en el tejido. La respuesta local se caracteriza por dolor, eritema e inflamación, procesos que derivan de la activación inmediata del sistema inmunitario innato. Tras la inoculación, componentes del veneno inducen la liberación de mediadores inflamatorios como histamina, prostaglandinas y citocinas proinflamatorias, lo que conduce a vasodilatación y aumento de la permeabilidad capilar. Esta alteración vascular permite la extravasación de plasma y células inmunitarias hacia el tejido afectado, generando edema y enrojecimiento. Paralelamente, la activación de nociceptores periféricos por estas moléculas explica la sensación dolorosa, ya que se incrementa la excitabilidad de las terminaciones nerviosas sensitivas cutáneas. Este mecanismo ha sido ampliamente descrito en estudios experimentales de inflamación inducida por toxinas animales, donde se demuestra que la activación de receptores específicos en fibras nerviosas tipo C y Aδ es responsable del dolor agudo inmediato.
En contraste, ciertas especies han desarrollado venenos con alta capacidad de difusión sistémica y con afinidad por blancos moleculares críticos, como los canales iónicos de membrana en neuronas y células musculares. En el caso de la viuda negra, el veneno contiene una neurotoxina principal conocida como alfa-latrotoxina, una proteína que interactúa con receptores presinápticos como neurexinas y latrofilinas en las terminaciones nerviosas. Esta interacción induce la formación de poros en la membrana neuronal o la activación de vías intracelulares dependientes de calcio, lo que resulta en una liberación masiva e incontrolada de neurotransmisores como acetilcolina, noradrenalina y glutamato. La consecuencia fisiológica de este fenómeno es una hiperestimulación del sistema neuromuscular y autónomo. Clínicamente, esto se traduce en dolor muscular intenso, espasmos generalizados y rigidez, manifestaciones que reflejan la contracción sostenida de fibras musculares debido a la estimulación continua de las placas neuromusculares. La afectación del sistema nervioso autónomo explica síntomas adicionales como diaforesis, hipertensión y taquicardia, evidenciando que el efecto del veneno no se limita al sistema motor, sino que involucra una disrupción global de la neurotransmisión.
Por otro lado, la araña reclusa marrón produce un veneno cuyo mecanismo de acción difiere radicalmente, ya que está dominado por enzimas con actividad citotóxica. Entre estas, la esfingomielinasa D desempeña un papel central. Esta enzima hidroliza componentes de la membrana celular, particularmente esfingomielina, generando productos que alteran la integridad estructural de las células y desencadenan cascadas inflamatorias y de muerte celular. La necrosis observada en el sitio de la picadura es el resultado de la destrucción directa de queratinocitos, células endoteliales y otras estructuras tisulares, combinada con la formación de microtrombos que comprometen la perfusión sanguínea local. Este proceso genera una lesión progresiva que puede extenderse durante días. En algunos casos, el veneno alcanza la circulación sistémica y produce hemólisis intravascular. Este efecto se debe a la acción de las toxinas sobre la membrana de los eritrocitos, lo que conduce a su destrucción y liberación de hemoglobina. La hemólisis puede desencadenar complicaciones como anemia aguda, insuficiencia renal secundaria a hemoglobinuria y alteraciones en la coagulación, lo que demuestra que el impacto del veneno puede trascender el tejido cutáneo y afectar sistemas vitales.
En el caso de los escorpiones, los venenos presentan una alta afinidad por los canales de sodio dependientes de voltaje en las membranas neuronales. Las toxinas escorpiónicas, que suelen ser péptidos de bajo peso molecular, se unen a estos canales y modifican su cinética de apertura y cierre, prolongando el estado activado o impidiendo su inactivación. Este efecto genera una despolarización sostenida de las neuronas, lo que resulta en una descarga repetitiva de impulsos nerviosos. La consecuencia fisiopatológica es una hiperexcitabilidad tanto del sistema nervioso somático como del autónomo. En especies del género Centruroides, esta actividad se traduce en manifestaciones clínicas que incluyen espasmos musculares, movimientos involuntarios y síntomas autonómicos como salivación excesiva, diaforesis y alteraciones cardiovasculares. La liberación masiva de catecolaminas inducida por la estimulación del sistema nervioso autónomo explica la aparición de hipertensión arterial y taquicardia. En casos graves, esta tormenta autonómica puede conducir a disfunción cardiovascular y edema pulmonar, este último resultado de un aumento en la presión hidrostática capilar pulmonar y de la permeabilidad vascular. Asimismo, la afectación del sistema nervioso central puede desencadenar convulsiones, lo que refleja la capacidad del veneno para alterar profundamente la excitabilidad neuronal.
La diferencia fundamental entre los efectos locales y sistémicos de estos venenos radica en su composición molecular, su capacidad de difusión y la especificidad de sus blancos biológicos. Mientras que los venenos con actividad predominantemente inflamatoria inducen respuestas locales limitadas, aquellos con componentes neurotóxicos o citotóxicos altamente especializados pueden desencadenar síndromes clínicos complejos que comprometen múltiples sistemas orgánicos. Este conocimiento no solo permite comprender la fisiopatología de las envenenaciones, sino que también ha sido fundamental para el desarrollo de terapias específicas, como los antivenenos, que actúan neutralizando estas toxinas mediante anticuerpos dirigidos.
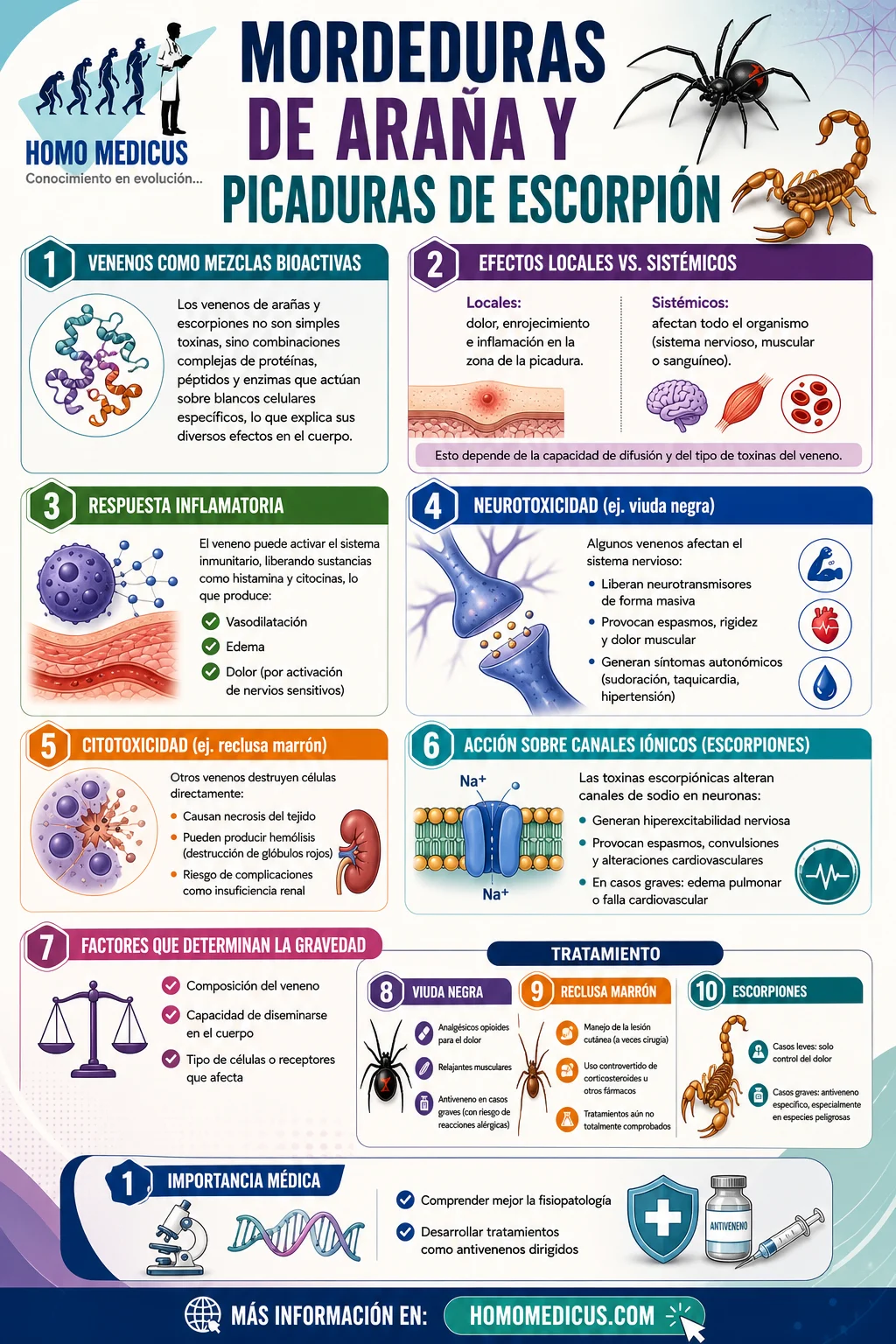
Tratamiento
Tratamiento de las mordeduras de Araña Viuda Negra (Latrodectus mactans)
El tratamiento de las mordeduras de la araña viuda negra se centra principalmente en el alivio de los síntomas, ya que el veneno de esta especie actúa a nivel neuromuscular y puede provocar dolor intenso, espasmos musculares involuntarios y rigidez generalizada. Estos síntomas se deben a una neurotoxina llamada alfa-latrotoxina, que induce la liberación masiva de neurotransmisores como la acetilcolina, la norepinefrina y el ácido gamma-aminobutírico, lo que altera el equilibrio del sistema nervioso autónomo y somático.
Para aliviar el dolor, que puede ser severo y generalizado, se recomienda el uso de analgésicos opioides administrados por vía parenteral. Estos fármacos actúan directamente sobre el sistema nervioso central para bloquear la percepción del dolor, proporcionando un alivio significativo en los casos moderados o graves.
Además del control del dolor, es común el uso de relajantes musculares, como el metocarbamol, en una dosis aproximada de quince miligramos por kilogramo de peso corporal. Este fármaco actúa deprimendo la actividad del sistema nervioso central, lo que reduce los espasmos musculares y la rigidez, mejorando la funcionalidad del paciente y su nivel de confort.
Otra opción terapéutica que se ha explorado es la administración intravenosa de gluconato de calcio al diez por ciento, en una dosis de cero punto uno a cero punto dos mililitros por kilogramo. Este compuesto puede proporcionar un alivio transitorio de la rigidez muscular al estabilizar la excitabilidad de las membranas celulares. No obstante, su eficacia en este contexto sigue siendo cuestionada, ya que la evidencia científica disponible no ha demostrado de manera concluyente beneficios consistentes en comparación con placebo u otras intervenciones.
En los casos más graves o en pacientes que no responden de forma adecuada a las medidas sintomáticas anteriores, puede considerarse el uso de un antiveneno específico contra Latrodectus. Este antiveneno, elaborado a partir de suero equino, tiene la capacidad de neutralizar directamente la toxina circulante, revirtiendo con mayor rapidez los síntomas sistémicos. Sin embargo, su uso no es rutinario, ya que está asociado con un riesgo significativo de reacciones de hipersensibilidad aguda, incluyendo anafilaxia y enfermedad del suero. Por esta razón, su administración se reserva generalmente para grupos de alto riesgo, como los lactantes, los adultos mayores o aquellos pacientes que presentan una evolución clínica desfavorable. En todos los casos, se debe realizar previamente una prueba de sensibilidad al suero equino para minimizar el riesgo de reacciones adversas graves.
Tratamiento de las mordeduras de Araña Reclusa Marrón (Loxosceles reclusa)
La mordedura de la araña reclusa marrón presenta un mecanismo de acción diferente, ya que su veneno tiene propiedades citotóxicas y necrosantes, lo que puede ocasionar destrucción progresiva de los tejidos blandos en la zona de la picadura. Esta necrosis se produce por la acción de enzimas como la esfingomielinasa D, que altera las membranas celulares y desencadena una cascada inflamatoria local severa.
Ante esta posibilidad de evolución a una lesión ulcerativa extensa, algunos especialistas proponen la escisión quirúrgica precoz del tejido afectado. Esta intervención busca eliminar el área necrótica antes de que el proceso inflamatorio se extienda a los tejidos circundantes. Sin embargo, esta práctica es controvertida, ya que el daño tisular inducido por el veneno puede estar en curso en tejidos aparentemente sanos, lo que complica la delimitación precisa del área a resecar.
En un enfoque alternativo, algunos clínicos optan por la administración de corticosteroides por vía oral, con el objetivo de reducir la inflamación y modular la respuesta inmunitaria del organismo ante la lesión. No obstante, la evidencia que respalda esta estrategia es limitada, y los resultados clínicos son variables.
Además, existen informes anecdóticos que mencionan el uso de medicamentos como la dapsona, un agente antiinflamatorio que inhibe la actividad de los neutrófilos, y la colchicina, que interfiere con los procesos inflamatorios intracelulares. Estos tratamientos han mostrado cierta eficacia en casos aislados, pero no cuentan con validación científica suficiente para ser considerados terapias estándar. En consecuencia, todas estas opciones deben considerarse experimentales y utilizadas con cautela, teniendo en cuenta el balance entre riesgos y beneficios.
Tratamiento de las Picaduras de Escorpiones
La mayoría de las especies de escorpiones producen un veneno cuya acción clínica es limitada al sitio de la picadura, generando dolor local, hinchazón y, en algunos casos, sensación de adormecimiento o parestesias. En estos casos, no se requiere un tratamiento específico más allá de medidas de soporte, como el uso de analgésicos convencionales para el control del dolor.
Sin embargo, existen especies de escorpiones cuya toxicidad es considerablemente mayor, especialmente aquellas pertenecientes al género Centruroides. El veneno de estos escorpiones tiene una acción neurotóxica que puede inducir síntomas sistémicos severos, como fasciculaciones musculares, convulsiones, hipertensión arterial y edema pulmonar. En estos casos, la administración de un antiveneno específico constituye la intervención terapéutica más efectiva.
Este antiveneno ha sido diseñado para neutralizar las toxinas del género Centruroides y revertir rápidamente las manifestaciones clínicas potencialmente letales. Su uso está indicado en pacientes que presentan signos de envenenamiento severo o en aquellos con condiciones médicas preexistentes que podrían agravarse con la acción del veneno.

Fuente y lecturas recomendadas:
- Klotz SA et al. Scorpion stings and antivenom use in Arizona. Am J Med. 2021;134:1034. [PMID: 33631163]
- Lopes PH et al. Clinical aspects, diagnosis and management of Loxosceles spider envenomation: literature and case review. Arch Toxicol. 2020;94:1461. [PMID: 32232511]
- Trave I et al. Cutaneous loxoscelism. JAMA Dermatol. 2020;156:203. [PMID: 31721992]
- Warpinski GP et al. North American envenomation syndromes. Emerg Med Clin North Am. 2022;40:313. [PMID: 35461625]




