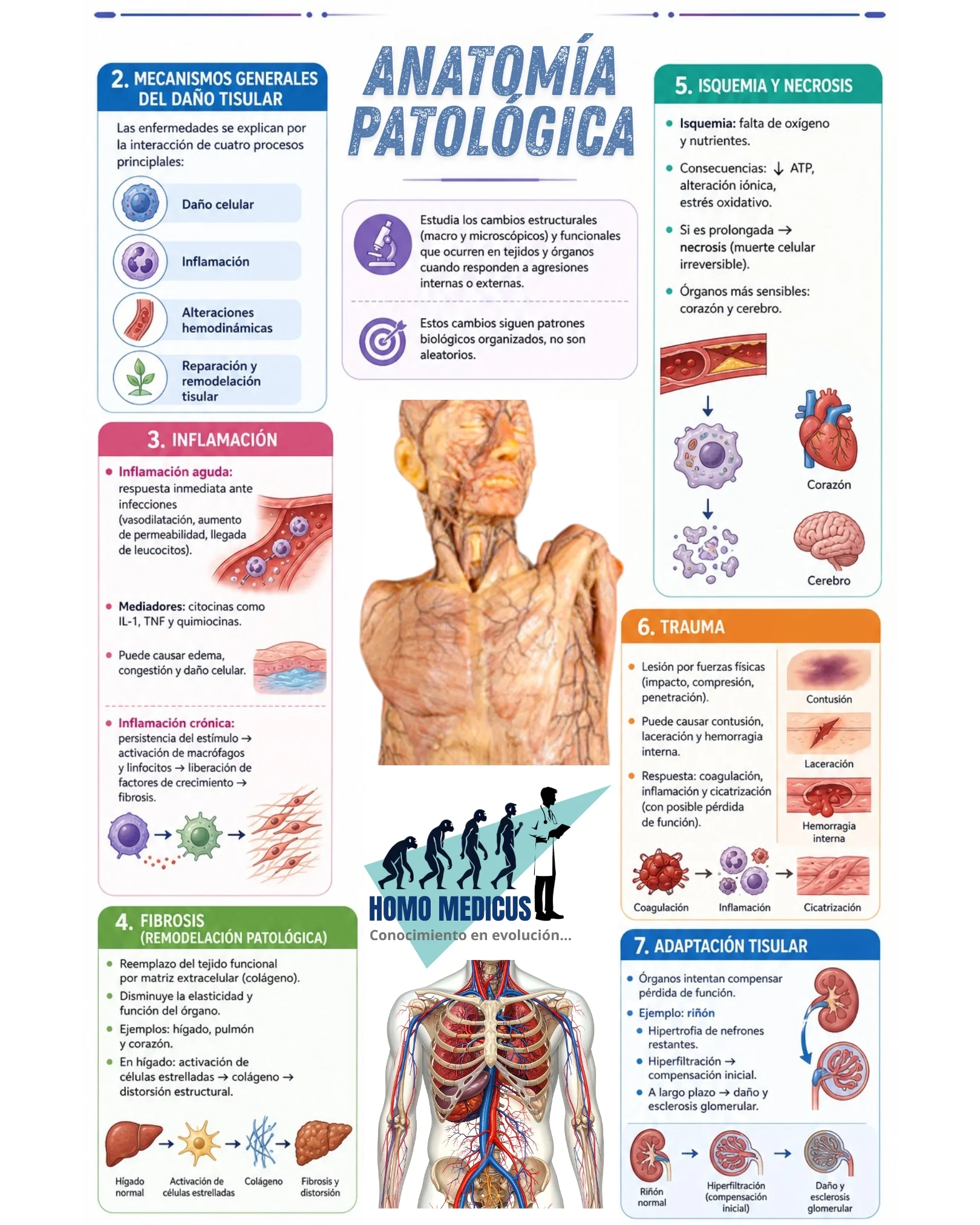
La anatomía y la fisiología patológicas constituyen el campo de estudio que describe de manera sistemática cómo los tejidos y órganos humanos modifican su estructura microscópica, macroscópica y funcional en respuesta a agresiones internas o externas. Estas modificaciones no son aleatorias, sino que siguen patrones biológicos conservados que reflejan la interacción entre mecanismos de daño celular, respuestas inflamatorias, alteraciones hemodinámicas y procesos de reparación tisular, ampliamente documentados en la literatura de patología general y fisiología médica.
En condiciones normales, cada órgano mantiene una arquitectura altamente especializada que sostiene su función mediante la organización precisa de sus células, su matriz extracelular y su microcirculación. Sin embargo, la exposición a agentes infecciosos puede desencadenar una respuesta inflamatoria aguda caracterizada por vasodilatación, aumento de la permeabilidad vascular y reclutamiento de leucocitos. Este proceso, mediado por citocinas como interleucina 1, factor de necrosis tumoral y quimiocinas, tiene como objetivo la eliminación del agente agresor, pero simultáneamente induce cambios estructurales en el tejido afectado, como edema intersticial, congestión vascular y daño celular reversible o irreversible. La persistencia del estímulo infeccioso puede conducir a inflamación crónica, donde la activación sostenida de macrófagos y linfocitos promueve la liberación de factores de crecimiento, especialmente el factor de crecimiento transformante beta, que estimula la deposición de colágeno y la formación de fibrosis, alterando de forma permanente la arquitectura del órgano.
La fibrosis representa un ejemplo fundamental de remodelación patológica. En este proceso, el tejido funcional es progresivamente reemplazado por matriz extracelular densa, lo que disminuye la elasticidad del órgano y compromete su función fisiológica. Este fenómeno ha sido ampliamente descrito en órganos como el hígado, el pulmón y el corazón, donde la reparación inadecuada tras lesión persistente conduce a una pérdida irreversible de unidades funcionales. En el hígado, por ejemplo, la activación de células estrelladas hepáticas tras daño crónico produce colágeno tipo I y III, generando nódulos de regeneración y distorsión de la arquitectura lobulillar.
Las alteraciones del flujo sanguíneo constituyen otro mecanismo esencial de daño orgánico. La reducción del aporte de oxígeno y nutrientes, conocida como isquemia, desencadena una cascada de eventos bioquímicos que incluyen disminución del trifosfato de adenosina, disfunción de bombas iónicas, acumulación intracelular de calcio y generación de especies reactivas de oxígeno. Si la isquemia es transitoria, el daño puede ser reversible; sin embargo, cuando se prolonga, conduce a necrosis, caracterizada por pérdida de integridad de membrana, digestión enzimática del citoplasma y respuesta inflamatoria secundaria. Este tipo de lesión es particularmente relevante en órganos altamente dependientes del metabolismo aeróbico, como el miocardio y el cerebro, donde incluso minutos de hipoxia pueden resultar en daño irreversible.
El traumatismo físico constituye una causa directa de alteración estructural orgánica. Los mecanismos de lesión incluyen fuerzas de impacto, compresión, desaceleración o penetración, que pueden producir desde contusiones hasta laceraciones completas de tejidos. En órganos sólidos como el hígado y el bazo, la alta vascularización y la consistencia parenquimatosa los hacen especialmente vulnerables a rupturas, lo que puede desencadenar hemorragias internas potencialmente letales. La respuesta del organismo ante estas lesiones incluye activación de la coagulación, inflamación aguda y procesos de reparación que pueden culminar en cicatrización con pérdida parcial de función.
En el sistema cardiovascular y respiratorio, muchas enfermedades producen alteraciones predominantemente funcionales antes de generar cambios estructurales evidentes. En la insuficiencia cardíaca, la capacidad del corazón para generar un gasto cardíaco adecuado se ve comprometida debido a disfunción contráctil miocárdica, sobrecarga de presión o volumen, o alteraciones neurohormonales como la activación del sistema renina angiotensina aldosterona. Estas adaptaciones inicialmente compensatorias incluyen hipertrofia miocárdica y remodelado ventricular, pero con el tiempo conducen a dilatación, fibrosis intersticial y deterioro progresivo de la función de bomba.
En la enfermedad pulmonar obstructiva crónica, la inflamación crónica de las vías respiratorias inducida por exposición prolongada a partículas nocivas genera destrucción del parénquima pulmonar, pérdida de elasticidad alveolar y obstrucción del flujo aéreo. Estos cambios funcionales incluyen atrapamiento de aire y alteración del intercambio gaseoso, lo que compromete la oxigenación sistémica incluso antes de que se observen cambios anatómicos macroscópicos extensos.
Los órganos también poseen mecanismos adaptativos frente a la pérdida de tejido o función. En el caso del riñón, la reducción de masa renal funcional desencadena hipertrofia compensatoria de los nefrones remanentes. Este proceso incluye aumento del tamaño celular, incremento de la tasa de filtración glomerular individual y cambios hemodinámicos intraglomerulares mediados por angiotensina II. Aunque esta adaptación permite mantener la homeostasis en etapas iniciales, la hiperfiltración sostenida induce daño progresivo en los glomérulos restantes, favoreciendo la esclerosis glomerular y acelerando la progresión hacia insuficiencia renal crónica.
Estos procesos demuestran que la enfermedad no solo altera la estructura visible de los órganos, sino también sus mecanismos celulares, bioquímicos y hemodinámicos más íntimos. La interacción entre daño, respuesta inflamatoria, reparación y adaptación determina el curso evolutivo de cada patología y explica por qué distintos órganos responden de manera específica a estímulos similares, dependiendo de su arquitectura, su demanda metabólica y su capacidad regenerativa.

Fuente y lecturas recomendadas:
- Kumar, V., Abbas, A. K., & Aster, J. C. (2020). Robbins and Cotran Pathologic Basis of Disease (10th ed.). Elsevier.
- Hall, J. E. (2021). Guyton and Hall Textbook of Medical Physiology (14th ed.). Elsevier.
- Kierszenbaum, A. L., & Tres, L. L. (2019). Histology and Cell Biology: An Introduction to Pathology (5th ed.). Elsevier.
- Fuster, V., & Hurst, J. W. (2011). Hurst’s The Heart (13th ed.). McGraw-Hill Education.
- Barnes, P. J. (2014). Cellular and molecular mechanisms of chronic obstructive pulmonary disease. Clinical Chest Medicine, 35(1), 71–86.
- Duffield, J. S. (2014). Cellular and molecular mechanisms in kidney fibrosis. Journal of Clinical Investigation, 124(6), 2299–2306.
- Sung, H., Ferlay, J., Siegel, R. L., et al. (2021). Global cancer statistics and pathological mechanisms of tissue injury and repair. CA: A Cancer Journal for Clinicians, 71(3), 209–249.




