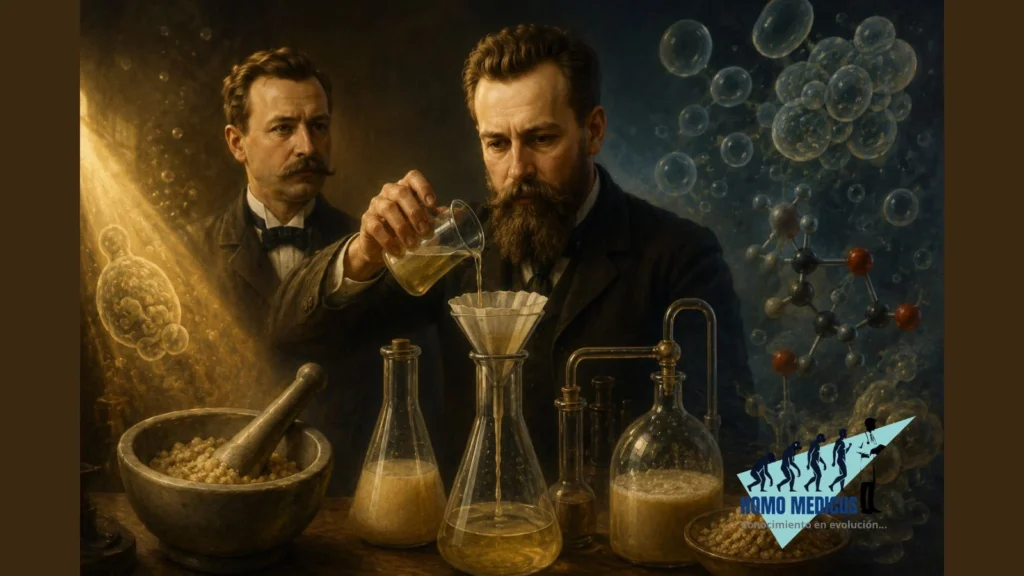Los inicios de la bioquímica moderna estuvieron profundamente ligados al estudio de la fermentación alcohólica y al intento de comprender si los fenómenos vitales dependían exclusivamente de la existencia de células vivas intactas o si, por el contrario, podían explicarse mediante principios químicos universales. Durante siglos, la humanidad había observado que la levadura transformaba los azúcares en alcohol etílico y dióxido de carbono durante la elaboración de pan, cerveza y vino. Sin embargo, hasta finales del siglo XIX persistía la idea de que estos procesos eran manifestaciones inseparables de la “fuerza vital” de los organismos vivos. Esta concepción, conocida como vitalismo, dominó gran parte de la fisiología y la química biológica de la época.
El principal defensor de esta interpretación fue Louis Pasteur, quien sostuvo que la fermentación alcohólica únicamente podía ocurrir en células de levadura vivas e intactas. Sus investigaciones habían demostrado que los microorganismos eran responsables de múltiples transformaciones biológicas y que la fermentación estaba asociada íntimamente con la vida celular. Debido a ello, Pasteur consideraba que la fermentación constituía una expresión inseparable de la actividad fisiológica de la célula viva. Esta interpretación tuvo enorme influencia científica y filosófica porque parecía confirmar que los procesos biológicos no podían reproducirse fuera del organismo.
La ruptura definitiva con esta concepción ocurrió gracias a los experimentos de Eduard Buchner y de su hermano Hans Büchner. En 1897, Eduard Büchner logró obtener extractos de levadura completamente libres de células vivas mediante trituración mecánica y filtración. Posteriormente añadió azúcar al extracto acelular y observó la producción de alcohol etílico y dióxido de carbono. El hallazgo resultó revolucionario porque demostraba que la fermentación podía producirse aun en ausencia de células intactas. Por primera vez en la historia se comprobaba experimentalmente que una reacción biológica compleja podía explicarse mediante agentes químicos presentes en el interior celular y no necesariamente por la “fuerza vital” de un organismo completo.
La importancia de este descubrimiento fue extraordinaria porque transformó por completo la comprensión de la biología. El experimento de Büchner demostró que los fenómenos vitales podían estudiarse mediante métodos químicos y físicos reproducibles. En consecuencia, la vida dejó de considerarse un fenómeno inexplicable y comenzó a entenderse como el resultado de reacciones químicas organizadas. Este cambio conceptual marcó el nacimiento formal de la bioquímica como disciplina científica independiente.
Büchner denominó “zimasa” al conjunto de sustancias responsables de la fermentación observada en sus extractos de levadura. Más adelante se comprendió que la zimasa no era una sola sustancia, sino una compleja mezcla de proteínas catalíticas que posteriormente recibirían el nombre de enzimas. El descubrimiento fue fundamental porque introdujo el concepto moderno de catálisis biológica. Desde ese momento se comprendió que las células contienen moléculas especializadas capaces de acelerar reacciones químicas específicas con enorme eficiencia y precisión.
El impacto científico del descubrimiento fue tan grande que Eduard Büchner recibió el Premio Nobel de Química en 1907 “por sus investigaciones bioquímicas y por su descubrimiento de la fermentación libre de células”. Este reconocimiento reflejaba que la comunidad científica comprendía ya que la bioquímica había inaugurado una nueva era para las ciencias biológicas y médicas.
A partir de este descubrimiento se desencadenó una intensa actividad investigadora dirigida a identificar las sustancias químicas involucradas en la fermentación y en otras rutas metabólicas celulares. Las investigaciones demostraron progresivamente que la degradación de la glucosa ocurre mediante una secuencia ordenada de reacciones químicas catalizadas por enzimas específicas. Este conjunto de reacciones sería posteriormente denominado glucólisis. El análisis detallado de esta vía metabólica permitió identificar metabolitos intermediarios fosforilados y revelar la importancia central del fosfato inorgánico en la transferencia de energía celular.
Durante estas investigaciones se descubrió además la función del adenosín trifosfato o ATP como principal molécula transportadora de energía química en la célula. El ATP actúa como una “moneda energética” universal que almacena energía en enlaces fosfato de alta energía y la transfiere a procesos biosintéticos, transporte activo y contracción muscular. Paralelamente se identificó el adenosín difosfato o ADP como producto de la hidrólisis del ATP y el nicotinamida adenina dinucleótido en sus formas oxidada y reducida, NAD⁺ y NADH, como moléculas esenciales en las reacciones de oxidación y reducción del metabolismo energético. Estas observaciones permitieron comprender que el metabolismo celular depende de sistemas organizados de transferencia de electrones y de energía química.
La elucidación de la glucólisis y de la fermentación alcohólica constituyó uno de los mayores logros científicos de principios del siglo XX porque permitió reconstruir paso a paso cómo una molécula de glucosa puede convertirse en piruvato y posteriormente en etanol y dióxido de carbono. Esto representó la primera demostración completa de una vía metabólica integrada.
En las décadas posteriores, particularmente entre 1930 y 1950, la bioquímica experimentó una expansión extraordinaria. Las investigaciones dirigidas por científicos como Hans Adolf Krebs permitieron identificar los metabolitos intermediarios del ciclo del ácido cítrico, también denominado ciclo de Krebs. Esta vía metabólica demostró cómo los organismos aerobios obtienen energía mediante la oxidación completa de carbohidratos, lípidos y proteínas. El ciclo del ácido cítrico reveló que el metabolismo no consiste en reacciones aisladas, sino en redes químicas integradas y coordinadas.
Simultáneamente se describió el ciclo de la urea, mediante el cual el organismo elimina el exceso de nitrógeno generado durante el catabolismo de aminoácidos. Este descubrimiento tuvo enorme importancia médica porque permitió comprender trastornos metabólicos hereditarios asociados con hiperamonemia y fallas hepáticas.
Otro avance decisivo fue la identificación de coenzimas derivadas de vitaminas. Se descubrió que muchas vitaminas no actúan directamente como nutrientes estructurales, sino como precursores de moléculas indispensables para la actividad enzimática. Entre ellas destacaron el pirofosfato de tiamina derivado de la vitamina B₁, la riboflavina precursora de FAD y FMN, la coenzima A derivada del ácido pantoténico, la coenzima Q implicada en la cadena respiratoria mitocondrial y las cobamidas derivadas de la vitamina B₁₂. Estas observaciones demostraron que numerosas enfermedades carenciales son consecuencia directa de alteraciones bioquímicas específicas.
La década de 1950 marcó además la comprensión detallada del metabolismo de carbohidratos complejos, aminoácidos y ácidos grasos. Los investigadores lograron describir cómo los polisacáridos son degradados hasta azúcares simples y cómo las pentosas participan en la síntesis de nucleótidos y ácidos nucleicos. Paralelamente se esclarecieron las rutas de β-oxidación de ácidos grasos y las vías catabólicas de numerosos aminoácidos. Esto permitió integrar el metabolismo energético en un modelo bioquímico global.
Todos estos descubrimientos fueron posibles gracias al desarrollo de nuevas metodologías experimentales. La ultracentrifugación analítica permitió separar orgánulos celulares y macromoléculas según su densidad. La cromatografía en papel y posteriormente otros tipos de cromatografía hicieron posible identificar metabolitos y purificar enzimas con alta precisión. Después de la Segunda Guerra Mundial, la disponibilidad de radioisótopos como ¹⁴C, ³H y ³²P revolucionó la investigación metabólica porque permitió rastrear átomos individuales dentro de vías bioquímicas complejas. Gracias a estos marcadores radiactivos se pudieron reconstruir rutas biosintéticas completas, incluyendo la biosíntesis del colesterol y numerosos procesos metabólicos celulares.
Otro avance decisivo fue la incorporación de la cristalografía de rayos X al estudio de macromoléculas biológicas. Esta técnica permitió determinar la estructura tridimensional de proteínas, enzimas, polinucleótidos y virus con resolución atómica. El conocimiento estructural reveló cómo las enzimas reconocen específicamente a sus sustratos y cómo pequeñas modificaciones estructurales pueden alterar radicalmente la función biológica.
Finalmente, el descubrimiento de la estructura de doble hélice del ADN por James Watson y Francis Crick transformó definitivamente la bioquímica al integrar genética y biología molecular. A partir de este hallazgo surgieron técnicas revolucionarias como la reacción en cadena de la polimerasa, la ingeniería genética y la producción de animales transgénicos o con genes inactivados. Estas herramientas permitieron analizar funciones génicas específicas y comprender las bases moleculares de múltiples enfermedades humanas.
En conjunto, los inicios de la bioquímica representaron una transformación radical de las ciencias biológicas. El descubrimiento de la fermentación libre de células destruyó el vitalismo y estableció que los fenómenos vitales obedecen leyes químicas universales. A partir de entonces, la bioquímica permitió explicar el metabolismo, la herencia, la producción de energía, la catálisis enzimática y la regulación celular mediante principios moleculares precisos. Esta transición convirtió a la bioquímica en una de las disciplinas fundamentales para el desarrollo de la medicina moderna, la farmacología, la genética molecular y la biotecnología contemporánea.


Fuente y lecturas recomendadas:
- Buchner, E. (1897). Alkoholische Gärung ohne Hefezellen. Berichte der Deutschen Chemischen Gesellschaft, 30(1), 117–124.
- Kohler, R. E. (1971). The background to Eduard Buchner’s discovery of cell-free fermentation. Journal of the History of Biology, 4(1), 35–61.
- Krebs, H. A., & Johnson, W. A. (1937). The role of citric acid in intermediate metabolism in animal tissues. Enzymologia, 4, 148–156.
- Sumner, J. B. (1926). The isolation and crystallization of the enzyme urease. Journal of Biological Chemistry, 69, 435–441.
- Watson, J. D., & Crick, F. H. C. (1953). Molecular structure of nucleic acids: A structure for deoxyribose nucleic acid. Nature, 171(4356), 737–738.
- Barnett, J. A. (2000). Eduard Buchner, zymase and the beginnings of biochemistry. Microbiology, 146(10), 2465–2479.
- Fruton, J. S. (1999). A history of biochemistry at the Rockefeller Institute. New Haven: Yale University Press.
- Lehninger, A. L., Nelson, D. L., & Cox, M. M. (2017). Principles of biochemistry (7th ed.). New York: W. H. Freeman.
- Stryer, L. (2019). Biochemistry (9th ed.). New York: W. H. Freeman.
- Voet, D., Voet, J. G., & Pratt, C. W. (2018). Fundamentals of biochemistry: Life at the molecular level (5th ed.). Hoboken: Wiley.