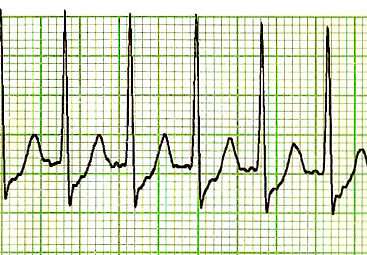
La taquicardia supraventricular paroxística, comúnmente abreviada como TSPV, es un tipo de arritmia que se manifiesta de manera intermitente y se caracteriza por episodios que comienzan y finalizan de forma repentina, acompañados de una respuesta ventricular regular. Estos episodios pueden tener una duración que oscila desde unos pocos segundos hasta varias horas o incluso más, lo que puede generar una considerable incomodidad en los pacientes que los experimentan. La TSPV se presenta con frecuencia en individuos que no presentan enfermedades cardíacas estructurales, lo que la hace aún más intrigante desde el punto de vista clínico.
El mecanismo subyacente más común que da lugar a la TSPV es el fenómeno de reentrada. Este mecanismo se activa cuando un impulso eléctrico se mueve a través de un circuito que permite su regreso a un punto de origen, creando un bucle continuo de activación eléctrica. La reentrada puede ser iniciada o interrumpida por un latido prematuro, que puede ser auricular o ventricular. En la mayoría de los casos, este circuito de reentrada involucra vías duales dentro del nodo auriculoventricular, que consta de una vía de conducción rápida y una vía de conducción lenta. Esta forma particular de la arritmia se denomina taquicardia reentrante nodal auriculoventricular y representa aproximadamente el sesenta por ciento de los casos de TSPV.
Por otro lado, en un menor porcentaje de casos, aproximadamente el treinta por ciento, la reentrada se produce debido a la existencia de una vía accesoria que conecta las aurículas con los ventrículos, lo que se conoce como taquicardia recíproca auriculoventricular. Este tipo de arritmia implica un mecanismo fisiopatológico diferente y requiere un enfoque de manejo que también varía considerablemente. Por lo tanto, es esencial considerar estos dos tipos de TSPV por separado, dado que sus características clínicas, así como las estrategias de tratamiento, pueden diferir de manera significativa.
El entendimiento de la fisiopatología de la TSPV es crucial para el manejo adecuado de esta arritmia. Los episodios pueden ser asintomáticos o pueden presentarse con síntomas que van desde palpitaciones leves hasta signos de insuficiencia cardíaca, lo que resalta la importancia de un diagnóstico preciso. El tratamiento puede incluir maniobras vagales, medicamentos antiarrítmicos o incluso la ablación por radiofrecuencia en casos refractarios. Así, la TSPV, a pesar de ser una arritmia común y a menudo benigna, requiere un enfoque diagnóstico y terapéutico adecuado para garantizar la salud y el bienestar de los pacientes afectados.
Manifestaciones clínicas
Los síntomas de la taquicardia supraventricular paroxística son diversos y pueden manifestarse de manera variable en función de múltiples factores, incluyendo la magnitud de la elevación de la frecuencia cardíaca, la hipotensión que puede resultar de esta condición, así como la presencia de otras comorbilidades en el paciente. Esta variabilidad en la presentación clínica hace que la experiencia de cada individuo sea única y depende de la respuesta fisiológica del organismo ante la arritmia.
Cuando la frecuencia cardíaca se eleva significativamente, el corazón puede no ser capaz de bombear sangre de manera eficiente, lo que puede llevar a una disminución del flujo sanguíneo hacia los órganos vitales. Este fenómeno puede provocar una serie de síntomas, entre los cuales se incluyen las palpitaciones, que son la sensación subjetiva de que el corazón está latiendo de manera rápida o irregular. Este síntoma es común y puede ser angustiante para el paciente.
Además de las palpitaciones, otros síntomas asociados a la TSPV pueden incluir diaforesis, que se refiere a la sudoración excesiva, y disnea, que es la dificultad para respirar. Estos síntomas pueden ser consecuencia de la activación del sistema nervioso simpático en respuesta al aumento de la frecuencia cardíaca, así como de una disminución en la perfusión sanguínea de los tejidos, que puede llevar a una sensación de falta de aire.
La presencia de mareos es otro síntoma que puede presentarse, y se relaciona frecuentemente con la reducción del flujo sanguíneo cerebral. En casos más extremos, puede haber dolor torácico leve, que aunque puede generar preocupación, a menudo no está asociado con cardiopatía isquémica en la mayoría de los pacientes que padecen TSPV. Este dolor puede deberse a la sobrecarga del miocardio o a la tensión emocional provocada por la arritmia.
Es importante señalar que, aunque la síncope, que es la pérdida temporal de la conciencia debido a una disminución del flujo sanguíneo cerebral, puede ocurrir, es un evento raro en el contexto de la TSPV. Esto se debe a que, en general, los episodios de taquicardia supraventricular no suelen provocar una caída tan drástica en la presión arterial como para inducir una pérdida de conocimiento.
La interacción de estos síntomas con las condiciones clínicas subyacentes del paciente, tales como enfermedades pulmonares, cardiacas o metabólicas, puede influir en la intensidad y la naturaleza de la presentación de la TSPV. Por lo tanto, el reconocimiento y la evaluación adecuada de estos síntomas son esenciales para un manejo efectivo de la arritmia y para proporcionar un enfoque terapéutico que se ajuste a las necesidades individuales de cada paciente.
Exámenes complementarios
Obtener un electrocardiograma de doce derivaciones es una práctica esencial en la evaluación de la taquicardia supraventricular paroxística, ya que proporciona información valiosa que ayuda a determinar el mecanismo subyacente de la arritmia. Este estudio electrocardiográfico permite una visualización detallada de la actividad eléctrica del corazón, facilitando así la identificación de patrones que son indicativos de diferentes tipos de taquicardia.
En la mayoría de los casos de taquicardia supraventricular paroxística, la duración del complejo QRS es estrecha, es decir, menor de 120 milisegundos. Esta característica se debe a que la taquicardia supraventricular típicamente origina su impulso eléctrico en las aurículas o en el nodo auriculoventricular, permitiendo que la activación ventricular ocurra de manera normal a través del sistema de conducción. Sin embargo, en situaciones donde existe conducción aberrante, como en el caso de un bloqueo de rama izquierda, un bloqueo de rama derecha, o la presencia de una vía accesoria que participa en la conducción anterógrada, el complejo QRS puede aparecer ancho, lo que puede llevar a confusión en el diagnóstico. Por ello, la interpretación del electrocardiograma es fundamental para diferenciar entre estas condiciones.
La frecuencia cardíaca observada durante un episodio de taquicardia supraventricular paroxística es típicamente regular y se sitúa en un rango que oscila entre 160 y 220 latidos por minuto. No obstante, en casos excepcionales, puede superar los 250 latidos por minuto. Esta frecuencia elevada es un reflejo de la rápida reentrada del impulso eléctrico, y su regularidad sugiere un origen claro en el nodo auriculoventricular o en estructuras asociadas.
Un aspecto distintivo en el electrocardiograma de la taquicardia supraventricular paroxística es la morfología de la onda P. A menudo, esta onda presenta un contorno que difiere del de los latidos sinusales normales, lo que puede indicar que la activación auricular está siendo desencadenada por un mecanismo diferente, como la reentrada. En muchos casos, la onda P puede aparecer simultáneamente con el complejo QRS o justo después de este, lo que indica que la activación auricular y ventricular está ocurriendo en un ciclo rápido y coordinado, a diferencia de lo que se observaría en una taquicardia ventricular o en otras arritmias.
Tratamiento
En la mayoría de los casos de taquicardia supraventricular paroxística, en ausencia de enfermedad cardíaca estructural, los efectos graves son relativamente raros. Esto se debe a que la TSPV, a menudo, es una arritmia benigna que puede resolver espontáneamente sin necesidad de intervención médica. La capacidad del organismo para restaurar un ritmo cardíaco normal es notable, y muchos episodios de TSPV se autolimitan, lo que proporciona un alivio a los pacientes y disminuye la urgencia del tratamiento en estos contextos.
Sin embargo, es crucial tener en cuenta que existen situaciones en las que la taquicardia supraventricular paroxística puede tener implicaciones más serias. Por ejemplo, si se desarrollan síntomas como insuficiencia cardíaca, síncope o dolor anginoso, la situación se vuelve más urgente. La insuficiencia cardíaca puede manifestarse como un deterioro en la función hemodinámica, lo que puede resultar en una disminución del suministro de sangre a los órganos vitales. El síncope, que es la pérdida temporal de la conciencia, puede ser una consecuencia de una perfusión cerebral inadecuada debido a la taquicardia rápida y sostenida. Asimismo, el dolor anginoso podría ser indicativo de isquemia miocárdica, lo cual requiere una atención médica inmediata, especialmente si el paciente tiene antecedentes de enfermedad cardíaca subyacente o, en particular, enfermedad coronaria.
El mecanismo de reentrada es el más común en la taquicardia supraventricular paroxística, y para manejar eficazmente esta arritmia, es esencial interrumpir la conducción en algún punto del circuito de reentrada. Este circuito generalmente implica el nodo auriculoventricular, que actúa como un centro crítico de control en la propagación de impulsos eléctricos entre las aurículas y los ventrículos. La interrupción de la reentrada puede lograrse a través de diversas maniobras y tratamientos. Las maniobras vagales, como la maniobra de Valsalva o la compresión del seno carotídeo, pueden ser efectivas para aumentar el tono vagal y disminuir la conducción a través del nodo auriculoventricular, lo que puede ayudar a restablecer el ritmo normal.
En situaciones en las que las maniobras vagales no son efectivas o cuando se presentan síntomas graves, pueden ser necesarios medicamentos antiarrítmicos o intervenciones más invasivas, como la ablación por radiofrecuencia. Esta última técnica implica la destrucción de un pequeño segmento del tejido cardíaco responsable de la reentrada, proporcionando una solución más permanente a la arritmia.
Medidas Mecánicas
Se han desarrollado y utilizado diversas maniobras físicas con el objetivo de interrumpir los episodios de taquicardia supraventricular paroxística. Estas maniobras son técnicas que los pacientes pueden aprender a realizar por sí mismos, lo que les permite actuar rápidamente en momentos de crisis. La efectividad de estas maniobras radica en su capacidad para inducir un aumento agudo del tono vagal, lo que afecta la conducción eléctrica del corazón y puede ayudar a restablecer un ritmo cardíaco normal.
Una de las maniobras más conocidas es la maniobra de Valsalva, que se realiza con el paciente en una posición semirrecostada a aproximadamente 45 grados. Esta maniobra implica que el paciente genere presión intratorácica al exhalar contra una resistencia, por ejemplo, soplando a través de una jeringa de diez mililitros, de tal manera que se alcance una presión de alrededor de 40 milímetros de mercurio durante al menos quince segundos. Esta presión intratorácica elevada provoca una serie de cambios hemodinámicos que pueden interrumpir el circuito de reentrada responsable de la arritmia. Para aumentar la efectividad de la maniobra, se recomienda mover al paciente a una posición supina inmediatamente después de realizarla y elevar pasivamente sus piernas durante otros quince segundos, lo que puede mejorar el retorno venoso y, en consecuencia, la respuesta del sistema cardiovascular.
Otra técnica que puede ser utilizada es el masaje del seno carotídeo, una maniobra que generalmente es realizada por profesionales de la salud. Esta técnica debe ser empleada con precaución, especialmente en pacientes que presentan un soplo carotídeo, debido al riesgo de complicaciones. Consiste en aplicar una presión firme pero suave en el seno carotídeo derecho durante un periodo de diez a veinte segundos. Si esta maniobra no tiene éxito, se puede intentar sobre el seno carotídeo izquierdo, pero es importante evitar la aplicación de presión en ambos lados simultáneamente, ya que esto podría inducir una bradicardia excesiva o afectar la hemodinámica del paciente de manera adversa.
El contacto facial con agua fría es otra estrategia que puede desencadenar el reflejo de buceo, un fenómeno fisiológico que produce una bradicardia transitoria y puede llevar a la terminación de la taquicardia supraventricular. Esta respuesta refleja es el resultado de la estimulación de los nervios vagales en la cara y puede ser sorprendentemente efectiva para restaurar un ritmo cardíaco normal.
Cuando estas maniobras se realizan de manera adecuada, se ha observado que pueden resultar en la terminación abrupta de la arritmia en un rango que varía entre el veinte y el cincuenta por ciento de los casos. Esto subraya la importancia de la educación del paciente en la identificación de los episodios de taquicardia supraventricular paroxística y la capacitación en la realización de estas maniobras. La capacidad de manejar la arritmia de manera autónoma no solo empodera al paciente, sino que también puede reducir la necesidad de intervenciones médicas urgentes, mejorando la calidad de vida y el manejo general de la condición.
Terapia Médica
Cuando las medidas mecánicas, como las maniobras vagales, no logran interrumpir un episodio de taquicardia supraventricular paroxística, es fundamental considerar la administración de agentes farmacológicos para restaurar un ritmo cardíaco normal. En este contexto, la adenosina intravenosa se recomienda como el agente de primera línea debido a su perfil farmacológico favorable, que incluye una breve duración de acción y una mínima actividad inotrópica negativa, lo que la convierte en una opción segura para el manejo agudo de la arritmia.
La adenosina tiene una vida media extremadamente corta, inferior a diez segundos, lo que permite que su efecto sea casi inmediato. Por lo general, se administra rápidamente en un bolo de seis miligramos, seguido de una inyección de veinte mililitros de solución salina para asegurar la dispersión adecuada del fármaco en el sistema circulatorio. Si esta primera dosis no resulta efectiva en la terminación de la arritmia, se puede considerar una segunda dosis más alta, que típicamente es de doce miligramos. Este enfoque escalonado permite maximizar la posibilidad de éxito en la interrupción de la taquicardia.
El mecanismo de acción de la adenosina se centra en su capacidad para causar un bloqueo de la conducción eléctrica a través del nodo auriculoventricular. Esto interrumpe temporalmente el circuito de reentrada que origina la taquicardia supraventricular, resultando en la terminación de la arritmia en aproximadamente el noventa por ciento de los casos. Este alto porcentaje de efectividad hace que la adenosina sea una herramienta valiosa en situaciones de emergencia.
Sin embargo, aunque los efectos secundarios menores son comunes, como enrojecimiento transitorio, malestar torácico, náuseas y dolor de cabeza, la administración de adenosina debe realizarse con precaución. Existe el riesgo de que la adenosina pueda excitar tanto el tejido auricular como el ventricular, lo que puede provocar fibrilación auricular en hasta el doce por ciento de los pacientes, así como arritmias ventriculares en casos raros. Por esta razón, es esencial que la administración de adenosina se realice bajo un monitoreo cardíaco continuo, con la disponibilidad inmediata de un desfibrilador externo para manejar cualquier complicación que pueda surgir.
Adicionalmente, se debe tener especial cuidado en pacientes que presentan enfermedad de vías respiratorias reactivas, como asma o enfermedad pulmonar obstructiva crónica, ya que la adenosina puede inducir broncoespasmo, lo que podría complicar aún más el estado del paciente. Por lo tanto, la evaluación del perfil clínico del paciente antes de la administración de adenosina es crucial para evitar posibles efectos adversos.
Cuando la adenosina no logra interrumpir un episodio de taquicardia supraventricular paroxística o si existen contraindicaciones para su uso, la administración de bloqueadores de los canales de calcio intravenosos, como el verapamilo y el diltiazem, se presenta como una alternativa efectiva. El verapamilo, en particular, ha demostrado ser altamente eficaz en la terminación de la taquicardia supraventricular paroxística en un entorno agudo, alcanzando una tasa de efectividad cercana al noventa por ciento, comparable a la de la adenosina.
Sin embargo, es importante considerar que los bloqueadores de los canales de calcio deben utilizarse con precaución en pacientes con insuficiencia cardíaca. Esto se debe a que estos medicamentos pueden tener efectos inotrópicos negativos, lo que significa que pueden disminuir la contractilidad del músculo cardíaco. En pacientes con función cardíaca ya comprometida, esto puede agravar la insuficiencia y provocar efectos adversos significativos. Además, la vida media de los bloqueadores de los canales de calcio es más prolongada en comparación con la adenosina, lo que puede dar lugar a una hipotensión persistente, incluso después de haber logrado la restauración del ritmo cardíaco normal. Por lo tanto, el monitoreo constante de la presión arterial y la función hemodinámica es esencial durante su administración.
Un fármaco innovador en este contexto es el etripamil, un bloqueador de los canales de calcio de acción corta que se administra por vía intranasal. En estudios preliminares, se ha demostrado que el etripamil puede inducir una rápida conversión de la taquicardia supraventricular paroxística en aproximadamente dos tercios de los pacientes tratados. Este enfoque presenta la ventaja de evitar la necesidad de una infusión intravenosa, lo que podría ser especialmente beneficioso en situaciones de emergencia. Actualmente, el etripamil está bajo revisión por la Administración de Alimentos y Medicamentos de Estados Unidos, con la esperanza de que su aprobación mejore significativamente el manejo de esta arritmia.
Por otro lado, los beta-bloqueadores intravenosos, que incluyen el esmolol, propranolol y metoprolol, representan otra opción terapéutica. El esmolol es un beta-bloqueador de acción muy corta, lo que lo hace adecuado para situaciones agudas. Aunque los beta-bloqueadores tienden a causar menos depresión miocárdica en comparación con los bloqueadores de los canales de calcio, la evidencia que respalda su efectividad para terminar la taquicardia supraventricular es más limitada. Esto significa que, aunque pueden ser útiles en algunos contextos, no son la primera opción en el tratamiento de la taquicardia supraventricular paroxística.
En cuanto a la amiodarona intravenosa, si bien se considera un fármaco seguro y tiene un amplio espectro de acción, generalmente no es necesario en el tratamiento de la taquicardia supraventricular paroxística. Además, su eficacia para interrumpir esta arritmia no es tan alta como la de otros agentes, lo que limita su uso en situaciones agudas.
Cardioversión
La cardioversión eléctrica sincronizada es un procedimiento crítico en el manejo de arritmias, especialmente en situaciones donde el paciente presenta inestabilidad hemodinámica. Esta inestabilidad puede manifestarse de diversas formas, como hipotensión severa, confusión, signos de insuficiencia cardíaca o dolor torácico significativo. Cuando un paciente se encuentra en esta condición, la restauración rápida de un ritmo cardíaco normal es fundamental para prevenir complicaciones graves, incluyendo el colapso cardiovascular y el daño a órganos vitales.
En tales escenarios, cuando las opciones terapéuticas iniciales, como la adenosina, los beta-bloqueadores y los bloqueadores de los canales de calcio, han demostrado ser ineficaces o están contraindicadas, la cardioversión eléctrica sincronizada se convierte en el tratamiento preferido. Este procedimiento implica la aplicación de una descarga eléctrica controlada al corazón, con el objetivo de restaurar un ritmo sinusal normal. La sincronización es un aspecto esencial de este método, ya que la descarga se aplica en el momento preciso del ciclo cardíaco, específicamente en la fase de repolarización, para minimizar el riesgo de inducir una fibrilación ventricular, que podría agravar aún más la situación del paciente.
La cardioversión se inicia generalmente con una energía de cien julios, aunque este valor puede ajustarse según la respuesta del paciente y la naturaleza de la arritmia. En casos de arritmias más resistentes, como la fibrilación ventricular o la taquicardia ventricular sin pulso, se pueden utilizar dosis más altas de energía, siempre bajo supervisión médica adecuada. La elección de comenzar con cien julios para la cardioversión eléctrica sincronizada se basa en la evidencia de que esta dosis es efectiva para la mayoría de las arritmias supraventriculares y de taquicardia ventricular con pulso.
Además de su efectividad, la cardioversión eléctrica sincronizada se caracteriza por ser un procedimiento relativamente seguro cuando se realiza en un entorno controlado, como en un hospital, donde se dispone de monitoreo continuo y de recursos adecuados para manejar cualquier complicación. Sin embargo, es esencial que se lleve a cabo en un entorno donde se puedan garantizar medidas de resucitación, incluyendo la disponibilidad de un desfibrilador automático, para actuar rápidamente en caso de que se produzcan arritmias más graves durante el procedimiento.
La decisión de realizar una cardioversión eléctrica sincronizada debe estar precedida por una evaluación exhaustiva del estado clínico del paciente, considerando factores como su historial médico, la duración de la arritmia, la presencia de comorbilidades y su respuesta a tratamientos previos. De este modo, la cardioversión eléctrica se presenta como una intervención fundamental en el manejo de situaciones de emergencia en cardiología, ofreciendo una solución rápida y efectiva para restaurar la estabilidad hemodinámica en pacientes con taquicardia supraventricular paroxística u otras arritmias que comprometan la función cardiovascular.
Prevención
La ablación por catéter se ha convertido en un enfoque preferido en el manejo de la taquicardia supraventricular paroxística, especialmente en casos de taquicardia reentrante sintomática recurrente. Este procedimiento, que generalmente utiliza la técnica de ablación por radiofrecuencia, se considera favorable debido a las preocupaciones sobre la seguridad y la tolerancia de los medicamentos antiarrítmicos. La ablación por catéter tiene como objetivo interrumpir de manera permanente el circuito de reentrada que causa la arritmia, ya sea dentro del nodo auriculoventricular o a través de vías accesorias.
La eficacia de la ablación radica en su capacidad para eliminar el tejido responsable de la conducción anormal, lo que a menudo resulta en una resolución definitiva de la arritmia. Este procedimiento se realiza de manera mínimamente invasiva y tiene un perfil de efectividad y seguridad que lo posiciona como una opción de tratamiento especialmente atractiva para pacientes que experimentan síntomas recurrentes y no toleran bien la terapia médica.
En cuanto a la terapia médica, los agentes bloqueadores del nodo auriculoventricular son los medicamentos de elección como tratamiento de primera línea para la taquicardia supraventricular. Estos medicamentos actúan disminuyendo la conducción eléctrica a través del nodo auriculoventricular, lo que puede ayudar a controlar la frecuencia cardíaca y restaurar un ritmo sinusal. Dentro de esta clase de fármacos, los beta-bloqueadores y los bloqueadores de los canales de calcio no dihidropiridínicos, como el diltiazem y el verapamilo, son comúnmente utilizados. Estos agentes son eficaces y generalmente bien tolerados, lo que los convierte en opciones de tratamiento iniciales para muchos pacientes.
Sin embargo, para aquellos que no responden adecuadamente a los agentes que aumentan la refractariedad del nodo auriculoventricular, puede ser necesario recurrir a antiarrítmicos más específicos. En pacientes sin enfermedad cardíaca estructural subyacente, los agentes de clase Ic, como la flecainida y la propafenona, pueden ser utilizados de manera segura. Estos fármacos son eficaces en la supresión de la taquicardia y suelen ser bien tolerados en este grupo de pacientes.
Por otro lado, en pacientes que presentan evidencia de enfermedad cardíaca estructural, se recomienda un enfoque más cauteloso. En estos casos, los agentes de clase III, como el sotalol o la amiodarona, son preferidos debido a su menor incidencia de proarrítmias ventriculares durante la terapia a largo plazo. Estos fármacos tienen un perfil de seguridad más favorable en individuos con un mayor riesgo de complicaciones cardíacas, lo que es crítico para evitar efectos adversos que puedan agravar la condición del paciente.

Fuente y lecturas recomendadas:
- Goldman, L., & Schafer, A. I. (Eds.). (2020). Goldman-Cecil Medicine (26th ed.). Elsevier.
- Loscalzo, J., Fauci, A. S., Kasper, D. L., Hauser, S. L., Longo, D. L., & Jameson, J. L. (Eds.). (2022). Harrison. Principios de medicina interna (21.ª ed.). McGraw-Hill Education.
- Papadakis, M. A., McPhee, S. J., Rabow, M. W., & McQuaid, K. R. (Eds.). (2024). Diagnóstico clínico y tratamiento 2024. McGraw Hill.