La hipoparatiroidismo adquirido es una condición caracterizada por una disminución o ausencia de secreción de hormona paratiroidea (PTH), secundaria a causas no genéticas. La etiología más común de esta alteración endocrina es la cirugía en la región anterior del cuello, particularmente procedimientos que comprometen la glándula tiroides o las glándulas paratiroides. Entre estos, la tiroidectomía total se destaca como la principal intervención quirúrgica asociada a hipoparatiroidismo adquirido, debido a la cercanía anatómica y la vulnerabilidad funcional de las glándulas paratiroides durante la resección tiroidea.
Durante una tiroidectomía total, las glándulas paratiroides pueden ser lesionadas directa o indirectamente. La extirpación inadvertida, la interrupción de su irrigación sanguínea, o incluso una manipulación quirúrgica excesiva pueden inducir isquemia y pérdida de función paratiroidea. En consecuencia, se observa hipoparatiroidismo transitorio en aproximadamente una cuarta parte de los pacientes sometidos a este procedimiento, mientras que el hipoparatiroidismo permanente se manifiesta en cerca del cuatro por ciento. El riesgo de daño irreversible puede mitigarse mediante la técnica de autotrasplante paratiroideo. Esta estrategia consiste en reimplantar en el músculo esternocleidomastoideo las glándulas que han sufrido daño vascular evidente durante la cirugía, lo cual favorece su revascularización y potencial recuperación funcional.
Otra situación quirúrgica asociada a hipoparatiroidismo es la paratiroidectomía, ya sea por adenomas únicos o múltiples, generalmente en el contexto de hiperparatiroidismo primario. En casos donde se reseca un solo adenoma, la supresión crónica del resto del tejido paratiroideo puede generar hipoparatiroidismo transitorio, acentuado por un fenómeno conocido como «síndrome del hueso hambriento», en el cual se produce una intensa remineralización ósea que reduce drásticamente los niveles de calcio sérico. En intervenciones más extensas, como la resección de múltiples adenomas o hiperplasia paratiroidea, el riesgo de hipoparatiroidismo permanente aumenta, y su diagnóstico se confirma si persiste más allá de los doce meses posteriores a la cirugía.
El seguimiento inmediato postoperatorio es crucial. Todos los pacientes sometidos a tiroidectomía o paratiroidectomía deben ser observados estrechamente durante al menos doce a veinticuatro horas, con determinaciones seriadas de calcio sérico y hormona paratiroidea. La hipocalcemia resultante puede ser severa, especialmente en pacientes que presentaban enfermedad ósea por hiperparatiroidismo previo, o que tenían deficiencia concomitante de vitamina D o magnesio.
Fuera del contexto quirúrgico, el hipoparatiroidismo también puede tener una etiología autoinmune. En algunos casos, esta afección ocurre de forma aislada, pero puede coexistir con otras deficiencias endocrinas, en el marco del síndrome poliendocrino autoinmune tipo I (APS-I), también conocido como poliendocrinopatía autoinmune-candidiasis-displasia ectodérmica (APECED). Este síndrome es causado por mutaciones en el gen regulador autoinmune (AIRE) y se asocia frecuentemente a hipoparatiroidismo temprano en la vida. Además, enfermedades autoinmunes como el lupus eritematoso sistémico pueden inducir hipoparatiroidismo mediante la producción de anticuerpos dirigidos contra las glándulas paratiroides.
Existen otras causas menos frecuentes de hipoparatiroidismo adquirido, entre las que se incluyen la toxicidad por metales pesados como el cobre (enfermedad de Wilson) o el hierro (hemocromatosis, hemosiderosis por transfusiones), así como procesos infiltrativos como granulomatosis, tiroiditis de Riedel, tumores, infecciones e irradiación cervical. Además, las alteraciones en los niveles de magnesio desempeñan un papel fisiopatológico relevante. Mientras una hipomagnesemia leve estimula la secreción de PTH, una deficiencia más profunda —por debajo de 1.2 miligramos por decilitro— inhibe la secreción de esta hormona e induce resistencia a su acción en los tejidos diana, como el hueso y los túbulos renales. En estos casos, la corrección de la hipomagnesemia puede revertir rápidamente la disfunción paratiroidea. Por otro lado, la hipermagnesemia también suprime la secreción de PTH, al activar de manera inapropiada el receptor sensible al calcio (CaSR) de las glándulas paratiroides.
El hipoparatiroidismo congénito, aunque no es adquirido, merece ser mencionado por su diagnóstico tardío en algunos casos. Esta forma de la enfermedad suele manifestarse con hipocalcemia desde la infancia, pero puede permanecer sin reconocimiento clínico durante años. Debido a que el hipoparatiroidismo puede ser hereditario, se recomienda el análisis genético del gen AIRE en aquellos pacientes con hipoparatiroidismo idiopático que además presenten signos compatibles con el síndrome APECED.
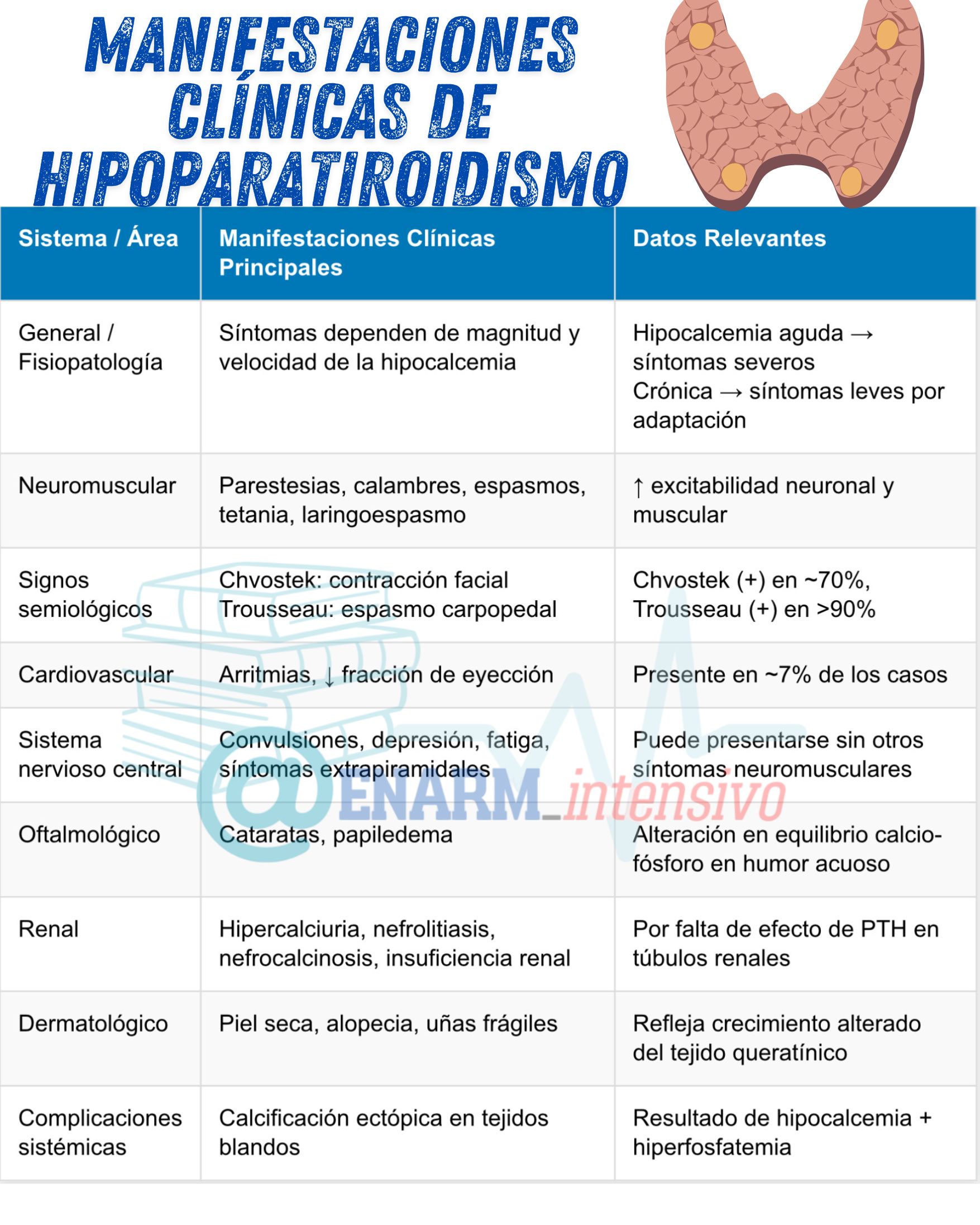
Manifestaciones clínicas
Los síntomas del hipoparatiroidismo dependen de dos factores fundamentales: la magnitud del descenso del calcio sérico y la velocidad con la que ocurre esta disminución. Esta relación dinámica entre la concentración de calcio y la adaptación fisiológica del organismo explica por qué pacientes con hipocalcemia aguda pueden presentar síntomas graves aun cuando los niveles de calcio en sangre se encuentren solo ligeramente reducidos o incluso dentro del rango bajo-normal. En contraste, pacientes con hipocalcemia crónica y severa, desarrollada de forma lenta y progresiva, pueden exhibir escasa sintomatología o manifestaciones clínicas poco evidentes, debido a mecanismos compensatorios que atenúan la respuesta neuromuscular y sistémica a la deficiencia de calcio.
Desde el punto de vista neuromuscular, la hipocalcemia inducida por hipoparatiroidismo se caracteriza por un aumento de la excitabilidad de las membranas neuronales y musculares. Esta hiperexcitabilidad se traduce clínicamente en irritabilidad neuromuscular, que se manifiesta por parestesias, especialmente en la región perioral y en las extremidades distales (manos y pies), mialgias, calambres musculares, espasmos musculares generalizados y, en casos severos, tetania. El reflejo osteotendinoso puede encontrarse exacerbado, y en casos críticos puede producirse laringoespasmo, una contracción súbita de la musculatura laríngea que obstruye parcialmente la vía aérea, causando estridor respiratorio, una condición potencialmente peligrosa si no se reconoce y se trata de forma oportuna.
Existen signos clínicos semiológicos clásicos que orientan al diagnóstico de hipocalcemia, como el signo de Chvostek y el signo de Trousseau. El signo de Chvostek consiste en la contracción involuntaria de los músculos faciales al percutir el nervio facial frente al trago; se encuentra presente en aproximadamente el setenta por ciento de los pacientes con hipocalcemia, pero también puede observarse en un pequeño porcentaje de individuos normocalcémicos. Por otro lado, el signo de Trousseau, mucho más específico, se observa en más del noventa por ciento de los individuos con hipocalcemia y en menos del uno por ciento de los individuos sin alteraciones del calcio. Este signo se desencadena al inflar un manguito de presión arterial por encima de la presión sistólica durante varios minutos, lo que induce una contracción característica de la mano y la muñeca (espasmo carpopedal), producto del aumento de la irritabilidad neuromuscular en condiciones de hipocalcemia.
A nivel cardiovascular, la hipocalcemia aguda puede provocar arritmias, presentes en aproximadamente el siete por ciento de los casos. Estas alteraciones incluyen bradicardia, arritmias ventriculares y disminución de la fracción de eyección, reflejo de una disfunción miocárdica inducida por el desequilibrio iónico. Dado que el calcio es fundamental para la contractilidad cardíaca y la conducción del impulso eléctrico, su deficiencia puede alterar profundamente la función cardiovascular.
Las manifestaciones del sistema nervioso central también son frecuentes y variadas. Entre las más relevantes se encuentran las convulsiones, que ocurren en alrededor del once por ciento de los pacientes, incluso en ausencia de otros signos de irritabilidad neuromuscular. También pueden presentarse alteraciones del estado de ánimo, tales como depresión (observada en el doce por ciento de los casos), irritabilidad, fatiga, alteraciones cognitivas, y síntomas psiquiátricos más complejos. En algunos casos, se han descrito síntomas extrapiramidales, lo que sugiere que la hipocalcemia prolongada puede afectar el metabolismo de regiones cerebrales profundas involucradas en el control motor.
En el ámbito oftalmológico, el hipoparatiroidismo crónico puede dar lugar a la formación de cataratas, presentes en aproximadamente el diecisiete por ciento de los casos. Esta opacificación del cristalino se debe a alteraciones en el equilibrio de calcio y fósforo dentro del humor acuoso. En casos de hipocalcemia severa, también puede desarrollarse papiledema, una inflamación del nervio óptico que refleja un aumento en la presión intracraneal secundaria a cambios en la permeabilidad vascular cerebral.
Las manifestaciones renales del hipoparatiroidismo crónico están estrechamente relacionadas con la hipercalciuria. A pesar de los bajos niveles séricos de calcio, la excreción renal puede estar aumentada debido a la ausencia del efecto regulador de la hormona paratiroidea sobre el túbulo distal renal. Esto conduce a complicaciones como nefrolitiasis (formación de cálculos renales), nefrocalcinosis (depósito de sales de calcio en el parénquima renal), presentes en un quince por ciento de los pacientes, y en algunos casos, insuficiencia renal crónica, observada en el doce por ciento de los casos.
Desde el punto de vista dermatológico, la deficiencia crónica de hormona paratiroidea con hipocalcemia persistente se asocia con signos cutáneos visibles. La piel suele volverse seca y áspera, el cabello presenta sequedad y puede observarse alopecia tanto en el cuero cabelludo como en las cejas. Las uñas pueden volverse quebradizas y desarrollar surcos transversales, lo que refleja un crecimiento alterado del tejido queratínico.
La combinación de hipocalcemia crónica con hiperfosfatemia —otra consecuencia típica del hipoparatiroidismo— favorece la precipitación de fosfato cálcico en tejidos blandos. Esta calcificación ectópica puede afectar articulaciones, piel, vasos sanguíneos y otros órganos, comprometiendo su función y generando complicaciones sistémicas progresivas.
Exámenes complementarios
El hallazgo bioquímico más característico es la disminución del calcio sérico total, resultado directo de la insuficiente secreción de hormona paratiroidea, cuya función principal es mantener la homeostasis del calcio mediante su acción sobre el hueso, el riñón y el intestino.
Sin embargo, dado que una fracción significativa del calcio circulante se encuentra unida a proteínas plasmáticas, principalmente a la albúmina, en situaciones de hipoalbuminemia el valor del calcio sérico total puede subestimar el nivel fisiológicamente activo de calcio iónico. Por esta razón, en pacientes con niveles bajos de albúmina sérica, es imprescindible determinar el calcio iónico directamente, o bien calcular una corrección del calcio total mediante la fórmula: calcio corregido (mg/dL) = calcio sérico (mg/dL) + 0.8 × (4.0 − albúmina [g/dL]). Esta corrección proporciona una estimación más precisa del calcio biológicamente disponible.
En cuanto a los niveles de hormona paratiroidea, se espera que estén bajos en el hipoparatiroidismo primario. No obstante, en algunos pacientes pueden encontrarse dentro de los límites normales del rango de referencia, lo cual no excluye el diagnóstico si la concentración de calcio es baja, ya que una respuesta hormonal apropiada sería un aumento compensatorio de la hormona paratiroidea. Por lo tanto, un nivel de PTH inapropiadamente bajo o normal frente a una hipocalcemia confirmada es sugestivo de hipoparatiroidismo. Para confirmar el diagnóstico, es recomendable repetir las mediciones de calcio y PTH séricos en una segunda muestra tomada con al menos dos semanas de intervalo, lo cual ayuda a descartar causas transitorias de hipocalcemia.
El magnesio sérico también debe evaluarse de forma rutinaria, ya que su deficiencia puede inducir un hipoparatiroidismo funcional al interferir con la secreción y acción de la hormona paratiroidea. La hipomagnesemia profunda puede suprimir la secreción de PTH y, además, causar resistencia a su acción en los tejidos diana, como los túbulos renales y el hueso, exacerbando la hipocalcemia.
Existen otras alteraciones bioquímicas que respaldan el diagnóstico de hipoparatiroidismo. Entre ellas destaca la elevación del fósforo sérico, consecuencia de la pérdida del efecto fosfatúrico de la PTH. Esta hormona, al estimular la excreción renal de fosfato, mantiene su nivel dentro de límites fisiológicos; en ausencia de esta función, el fósforo tiende a acumularse en el suero. Asimismo, la producción renal de 1,25-dihidroxivitamina D (la forma activa de la vitamina D) se encuentra disminuida, ya que esta conversión es estimulada directamente por la PTH. Esta deficiencia contribuye a la reducción de la absorción intestinal de calcio, agravando la hipocalcemia. Por otro lado, se observa un aumento en la fracción de excreción urinaria de calcio, ya que la PTH también actúa sobre el túbulo distal renal para favorecer la reabsorción de calcio; su ausencia conduce a una pérdida inapropiada de este ion en la orina, un hallazgo característico del hipoparatiroidismo.
Desde el punto de vista de la imagenología, se recomienda la tomografía computarizada renal sin contraste para evaluar la presencia de nefrolitiasis o nefrocalcinosis, complicaciones frecuentes en pacientes con hipocalcemia crónica y excreción urinaria elevada de calcio. Adicionalmente, en pacientes con hipocalcemia de larga evolución, la tomografía computarizada cerebral puede revelar calcificaciones intracraneales, especialmente en los ganglios basales, pero también en otras estructuras del sistema nervioso central. Estas calcificaciones están presentes en más del cincuenta por ciento de los casos y reflejan la precipitación de sales cálcicas en tejidos neuronales, facilitada por la hiperfosfatemia crónica.
La evaluación ósea puede mostrar un aumento de la densidad mineral ósea, particularmente en la columna lumbar. Este hallazgo puede parecer paradójico, pero es consistente con la fisiopatología del hipoparatiroidismo, donde la ausencia de PTH disminuye el recambio óseo y la resorción, resultando en una acumulación progresiva de masa ósea, aunque esta puede ser metabólicamente inactiva y de calidad estructural alterada. También pueden observarse calcificaciones en tejidos blandos, incluyendo la piel, los vasos sanguíneos y las articulaciones, como resultado de la prolongada combinación de hipocalcemia con hiperfosfatemia.
Entre otros estudios diagnósticos relevantes se encuentra el examen con lámpara de hendidura, que puede evidenciar la formación precoz de cataratas subcapsulares posteriores, una complicación oftalmológica habitual en pacientes con hipocalcemia crónica. Finalmente, el electrocardiograma puede mostrar alteraciones significativas en la conducción eléctrica del corazón. Estas incluyen bloqueo auriculoventricular, prolongación del intervalo QT corregido y cambios en el segmento ST y la onda T que pueden simular un infarto agudo de miocardio, reflejando la influencia del calcio en la electrofisiología cardíaca.
Complicaciones
El hipoparatiroidismo, especialmente cuando no es diagnosticado o tratado de manera oportuna y adecuada, puede dar lugar a una serie de complicaciones clínicas de diversa gravedad que reflejan las alteraciones sistémicas inducidas por la hipocalcemia crónica y por las consecuencias del tratamiento prolongado.
Una de las complicaciones más graves es la tetania aguda, una manifestación de hiperexcitabilidad neuromuscular severa, que puede progresar rápidamente a espasmos musculares generalizados, incluyendo contracciones sostenidas de la musculatura laríngea. Este fenómeno puede generar estridor, una señal clínica de obstrucción parcial de la vía aérea superior. La situación se torna particularmente crítica cuando la tetania se acompaña de parálisis de las cuerdas vocales, condición que puede comprometer aún más el paso del aire y precipitar una obstrucción respiratoria aguda. En estos casos, la intervención inmediata puede requerir medidas avanzadas de manejo de la vía aérea, como una traqueostomía de urgencia, a fin de evitar la asfixia y garantizar una oxigenación adecuada.
Las convulsiones constituyen otra complicación común en pacientes con hipocalcemia no tratada o inadecuadamente controlada. El calcio es esencial para la estabilidad de las membranas neuronales y su deficiencia facilita la despolarización espontánea y anómala de las neuronas, aumentando la propensión a crisis epilépticas. Estas convulsiones pueden ser focales o generalizadas, y en ocasiones representar la primera manifestación del hipoparatiroidismo no diagnosticado.
Desde el punto de vista cardiovascular, la hipocalcemia puede inducir alteraciones importantes en la función y el ritmo cardíaco. La insuficiencia cardíaca se puede desarrollar como consecuencia de la reducción de la contractilidad miocárdica dependiente del calcio intracelular. Además, la hipocalcemia interfiere con la conducción eléctrica del corazón, predisponiendo al desarrollo de disritmias, que incluyen bradicardia, taquiarritmias ventriculares y prolongación del intervalo QT, esta última asociada con riesgo de arritmias malignas como la torsade de pointes. Estas complicaciones pueden ser fatales si no se corrige el desequilibrio electrolítico de forma oportuna.
Otra complicación menos frecuente pero clínicamente relevante es la osificación de los ligamentos paravertebrales, un fenómeno que puede resultar de la prolongada alteración en el metabolismo del calcio y el fósforo. La mineralización ectópica de los tejidos conectivos alrededor de la columna vertebral puede conducir a compresión de raíces nerviosas, lo cual se manifiesta como dolor radicular, debilidad muscular o disfunción sensitiva. En casos avanzados, esta compresión puede requerir tratamiento quirúrgico mediante descompresión espinal.
Es importante señalar que el tratamiento del hipoparatiroidismo con vitamina D activa (calcitriol) y suplementos de calcio, si bien es fundamental para prevenir las consecuencias inmediatas de la hipocalcemia, puede inducir complicaciones a largo plazo si no se administra con un control riguroso. El exceso de calcio, en combinación con un aumento en su absorción intestinal, puede producir hipercalciuria y, eventualmente, nefrocalcinosis. Esta condición implica la deposición de sales cálcicas en el parénquima renal, lo que con el tiempo puede llevar a una progresiva pérdida de la función renal. La vigilancia estrecha de los niveles de calcio sérico y urinario es esencial para evitar esta complicación iatrogénica.
Adicionalmente, el hipoparatiroidismo puede coexistir con otras enfermedades autoinmunes, especialmente cuando forma parte de un síndrome poliglandular autoinmune. Estas asociaciones reflejan una disfunción inmunológica subyacente común y pueden incluir enfermedades como la enfermedad celíaca, caracterizada por una respuesta inmune contra el gluten que daña el epitelio intestinal; la anemia perniciosa, en la cual se produce una destrucción autoinmune de las células parietales gástricas o de los factores intrínsecos, con consiguiente déficit de vitamina B12; y la enfermedad de Addison, que se manifiesta como una insuficiencia suprarrenal primaria causada por destrucción autoinmune de la corteza adrenal. La coexistencia de estas entidades clínicas exige un enfoque multidisciplinario y una evaluación continua del estado inmunológico del paciente.
Diagnóstico diferencial
El diagnóstico diferencial del hipoparatiroidismo requiere una evaluación cuidadosa de las causas potenciales de hipocalcemia, así como de condiciones clínicas que pueden simular los síntomas neuromusculares típicos de la deficiencia de calcio, incluso en presencia de niveles séricos normales. El reconocimiento preciso de estas entidades es esencial para evitar tratamientos inadecuados y para establecer el enfoque terapéutico correcto según la etiología subyacente.
Uno de los principales retos diagnósticos es la diferenciación entre hipocalcemia real y los síntomas inducidos por alcalosis respiratoria, una condición en la cual los niveles de calcio iónico disminuyen transitoriamente sin que exista una verdadera hipocalcemia total. Durante la hiperventilación, el aumento del pH plasmático incrementa la unión del calcio a proteínas como la albúmina, lo que reduce la fracción libre o ionizada de calcio —la forma fisiológicamente activa— a pesar de que los niveles de calcio total permanecen normales. Esta situación puede desencadenar parestesias, calambres musculares o incluso tetania, mimetizando los signos de hipoparatiroidismo. De hecho, en pacientes con hipocalcemia preexistente, la hiperventilación puede exacerbar de manera significativa sus síntomas neuromusculares.
Existen múltiples fármacos capaces de inducir hipocalcemia, lo que debe ser considerado cuidadosamente en la anamnesis. Los diuréticos de asa, como la furosemida, aumentan la excreción renal de calcio, lo cual puede llevar a hipocalcemia, especialmente en pacientes con reservas minerales limitadas. Agentes antineoplásicos como el plicamicina (mithramicina) y medicamentos anticonvulsivantes como la fenitoína también interfieren con el metabolismo del calcio o la vitamina D. Otros agentes, como el foscarnet, un antiviral, o los inhibidores de la resorción ósea como el denosumab y los bisfosfonatos, pueden inducir hipocalcemia al alterar el equilibrio entre la reabsorción ósea y el depósito mineral.
La malabsorción intestinal constituye otra causa relevante de hipocalcemia. Condiciones como la enfermedad celíaca, la enfermedad inflamatoria intestinal, o síndromes de malabsorción posquirúrgicos pueden reducir significativamente la absorción de calcio, magnesio o vitamina D, todos ellos fundamentales para el mantenimiento de la homeostasis del calcio. La deficiencia concomitante de magnesio puede ser particularmente crítica, ya que este mineral no solo es necesario para la secreción de la hormona paratiroidea, sino también para su acción en los tejidos blanco. Por tanto, una hipomagnesemia prolongada puede inducir un hipoparatiroidismo funcional con hipocalcemia secundaria.
En el contexto oncológico, se espera frecuentemente una hipercalcemia como manifestación paraneoplásica, especialmente en carcinomas con metástasis osteolíticas. Sin embargo, ciertos tumores con actividad osteoblástica predominante, como los carcinomas de mama o de próstata, pueden producir hipocalcemia al estimular una intensa incorporación de calcio en el hueso, superando la capacidad de compensación homeostática del organismo.
Una forma particular de hipocalcemia con hiperfosfatemia que simula clínicamente al hipoparatiroidismo puede observarse en pacientes con insuficiencia renal avanzada, o azotemia. En este contexto, la disminución de la excreción renal de fósforo y la alteración en la conversión de vitamina D a su forma activa contribuyen a la hipocalcemia. También puede inducirse artificialmente mediante la administración excesiva de preparaciones de fosfato por vía oral, intravenosa o rectal, o como efecto colateral del tratamiento quimioterápico de linfomas o leucemias sensibles, en los cuales se produce una rápida lisis celular con liberación de fosfato intracelular.
Un diagnóstico diferencial importante es el de la hipocalcemia con hipercalciuria causada por una mutación autosómica dominante en el gen que codifica el receptor sensor de calcio (CaSR). Esta condición, conocida como hipocalcemia autosómica dominante hipercalciúrica, implica una ganancia de función del receptor, lo que genera una supresión inadecuada de la secreción de PTH incluso cuando los niveles de calcio están bajos. A diferencia del hipoparatiroidismo clásico, en estos pacientes los niveles de PTH suelen encontrarse dentro del rango normal o apenas suprimidos, pero inapropiadamente bajos para el grado de hipocalcemia. La administración de calcio y vitamina D, si no se controla cuidadosamente, puede precipitar nefrocalcinosis por el aumento en la carga urinaria de calcio.
Se deben considerar los síndromes de pseudohipoparatiroidismo, un grupo de trastornos congénitos caracterizados por resistencia periférica a la acción de la hormona paratiroidea. En estos casos, aunque la PTH está presente en concentraciones normales o elevadas, sus efectos fisiológicos no se manifiestan debido a mutaciones en componentes clave de la vía de señalización, incluyendo el receptor renal de PTH, la proteína G asociada al receptor, o la adenilil ciclasa. Esta resistencia hormonal resulta en un perfil bioquímico que imita al hipoparatiroidismo (hipocalcemia con hiperfosfatemia), pero se distingue por los niveles séricos elevados de PTH. Algunos subtipos también pueden presentar fenotipos específicos, como el síndrome de Albright, caracterizado por talla baja, obesidad y anormalidades esqueléticas.
Tratamiento
El tratamiento del hipoparatiroidismo, en particular cuando se presenta en el contexto postoperatorio inmediato, requiere una estrategia terapéutica tanto preventiva como correctiva, que se adapte a la gravedad de la hipocalcemia y a la condición clínica del paciente. El objetivo principal es restaurar la normocalcemia de forma segura y sostenida, prevenir complicaciones neuromusculares y cardiovasculares, y corregir alteraciones electrolíticas asociadas, como la hipomagnesemia. El abordaje terapéutico puede dividirse en dos grandes ámbitos: la profilaxis en pacientes de alto riesgo tras cirugía tiroidea o paratiroidea, y el tratamiento de emergencia de la hipocalcemia aguda, particularmente en el contexto de tetania hipoparatiroidea.
A. Profilaxis frente a la hipocalcemia postoperatoria severa
La hipocalcemia es una complicación frecuente después de la tiroidectomía total o la paratiroidectomía, particularmente si ocurre lesión directa o disfunción de las glándulas paratiroides durante la cirugía. Para prevenir el desarrollo de hipocalcemia clínica en el periodo postoperatorio, es fundamental una monitorización temprana y estrecha de los niveles séricos de hormona paratiroidea y calcio. La medición de la hormona paratiroidea a las pocas horas de la intervención permite predecir con alta sensibilidad el riesgo de hipocalcemia. Si el nivel de calcio sérico desciende por debajo de 8.0 miligramos por decilitro (equivalente a 2.0 milimoles por litro) en presencia de una concentración de hormona paratiroidea menor a 10–15 picogramos por mililitro, el paciente se considera en alto riesgo de desarrollar hipocalcemia sintomática y debe iniciarse tratamiento profiláctico.
La profilaxis oral estándar incluye la administración de calcitriol —la forma activa de la vitamina D— en dosis de 0.25 a 1 microgramo dos veces al día. Este fármaco facilita la absorción intestinal de calcio y tiene un inicio de acción rápido, lo cual es crucial en la prevención de la hipocalcemia aguda. Además, se debe administrar calcio por vía oral, generalmente como carbonato de calcio, en dosis de 500 a 1000 miligramos dos veces al día, preferiblemente junto con las comidas para optimizar su absorción. Esta estrategia ayuda a mantener niveles adecuados de calcio plasmático durante el periodo en que las glándulas paratiroides puedan estar transitoriamente inactivas o lesionadas.
B. Tratamiento de emergencia de la hipocalcemia aguda (tetania hipoparatiroidea)
En casos de hipocalcemia aguda con síntomas neuromusculares severos, como tetania, espasmos musculares, laringoespasmo o convulsiones, el tratamiento debe ser inmediato y multidisciplinario.
-
Vía aérea: La primera prioridad es asegurar una vía aérea permeable. La tetania laringea o la parálisis de cuerdas vocales puede comprometer la ventilación, por lo que deben implementarse medidas para garantizar una oxigenación adecuada, incluyendo intubación endotraqueal o traqueostomía en casos extremos.
-
Administración intravenosa de gluconato de calcio: Para el alivio inmediato de los síntomas, se administra gluconato de calcio al 10% por vía intravenosa lenta, en volúmenes de 10 a 20 mililitros, hasta que se resuelva la tetania. En situaciones más prolongadas o si los síntomas persisten, se puede diluir una cantidad mayor (hasta 50 mililitros de gluconato de calcio al 10%) en un litro de solución glucosada al 5% o solución salina al 0.9%, administrado mediante infusión continua. La velocidad de infusión debe ajustarse para mantener el calcio sérico entre 8.0 y 9.0 miligramos por decilitro, lo que representa un rango terapéutico seguro para evitar tanto la hipocalcemia persistente como la hipercalcemia iatrogénica.
-
Calcio oral: Tan pronto como el paciente pueda tolerar la vía oral, se deben administrar sales de calcio por esta vía, con el objetivo de aportar entre uno y dos gramos diarios de calcio elemental. El carbonato de calcio líquido, que contiene un 40% de calcio elemental (500 miligramos por cada 5 mililitros), es especialmente útil en esta etapa y debe administrarse con las comidas para mejorar su biodisponibilidad.
-
Preparaciones de vitamina D: El tratamiento con vitamina D activa debe iniciarse de manera concomitante con el calcio oral. El calcitriol, o 1,25-dihidroxicolecalciferol, es la opción preferida por su rápida acción, aunque su vida media corta implica que puede requerirse ajuste frecuente de la dosis. Se recomienda iniciar con 0.25 microgramos diarios por vía oral, generalmente por la mañana, e ir aumentando progresivamente la dosis hasta alcanzar niveles de calcio cercanos a lo normal. En algunos pacientes, pueden requerirse dosis de hasta 4 microgramos por día para mantener la normocalcemia.
-
Corrección de la hipomagnesemia: La deficiencia de magnesio debe identificarse y corregirse de manera simultánea, ya que impide tanto la secreción como la acción de la hormona paratiroidea. Si el magnesio sérico se encuentra por debajo de 1.8 miligramos por decilitro (0.8 milimoles por litro), debe iniciarse la reposición. En casos críticos (niveles menores a 1.0 miligramos por decilitro o 0.45 milimoles por litro), se administra sulfato de magnesio al 50% (5 gramos por 10 mililitros), diluido en 250 mililitros de solución salina al 0.9% o glucosa al 5%, infundido en un lapso de tres horas. La reposición continua debe guiarse por los niveles séricos y puede mantenerse a largo plazo mediante la administración oral de óxido de magnesio, en tabletas de 500 miligramos (con un 60% de magnesio elemental), una a tres veces al día según necesidad.
C.Tratamiento de mantenimiento
El tratamiento de mantenimiento del hipoparatiroidismo se centra en asegurar que los niveles de calcio en suero se mantengan dentro de un rango adecuado para evitar tanto los síntomas de hipocalcemia como las complicaciones asociadas con el exceso de calcio. Este tratamiento es individualizado según la gravedad del hipoparatiroidismo y los niveles de calcio en el suero de cada paciente. A continuación, se detallan los principios y opciones terapéuticas para el manejo a largo plazo del hipoparatiroidismo, incluyendo la terapia con calcio, vitamina D, magnesio y otras estrategias de manejo.
Tratamiento en pacientes con hipoparatiroidismo leve
Los pacientes con hipoparatiroidismo leve, que no presentan síntomas significativos de hipocalcemia, pueden no requerir tratamiento inmediato. Sin embargo, deben ser monitorizados estrechamente para detectar signos tempranos de hipocalcemia, dado que los niveles de calcio pueden fluctuar con el tiempo, especialmente si la función de las glándulas paratiroides sigue comprometida. Los pacientes en esta categoría pueden requerir ajustes en su tratamiento conforme cambian sus necesidades metabólicas.
Tratamiento en pacientes con hipocalcemia sintomática o niveles de calcio sérico bajos
La terapia farmacológica se indica en pacientes con hipocalcemia manifiesta o niveles de calcio en suero por debajo de 8.0 mg/dL (2 mmol/L). El tratamiento estándar consiste en la administración de calcio y vitamina D, y en algunos casos, magnesio, para mantener niveles adecuados de calcio en sangre y evitar la aparición de síntomas graves o complicaciones.
-
Suplementos de calcio: El calcio se administra generalmente en forma de suplementos orales, siendo el carbonato de calcio una de las opciones más comunes, dado que contiene un 40% de calcio elemental y se absorbe mejor en un entorno ácido del estómago, lo que favorece su absorción durante las comidas. El citrato de calcio, que contiene un 21% de calcio elemental, es una opción preferida en pacientes que reciben inhibidores de la bomba de protones (IBP) o bloqueadores H2, ya que no depende de un pH gástrico bajo para su absorción y causa menos intolerancia gastrointestinal. Los suplementos de calcio se administran en dosis divididas de 0.8 a 4 gramos diarios de calcio elemental, y deben tomarse durante las comidas para mejorar su absorción.
-
Terapia con vitamina D: En pacientes con hipoparatiroidismo crónico, el uso de análogos de la vitamina D es esencial, ya que estos pacientes presentan una deficiencia en la 1-hidroxilación renal de la vitamina D. Los análogos de la vitamina D activados, como el calcitriol y el alfacalcidol, son los más comúnmente utilizados, ya que no requieren conversión adicional en el riñón. Estos fármacos aumentan la absorción intestinal de calcio y ayudan a mantener niveles séricos adecuados de calcio. Se inicia generalmente con 0.25 microgramos de calcitriol al día, con ajustes progresivos para mantener los niveles de calcio en el rango terapéutico.
-
Magnesio: Debido a que la hipomagnesemia puede empeorar la hipocalcemia al interferir con la secreción de hormona paratiroidea y con la acción del calcio, se debe monitorear y mantener el magnesio sérico dentro de los límites normales. En caso de hipomagnesemia, se deben administrar suplementos orales de magnesio, y en casos graves, se puede requerir administración intravenosa de magnesio.
-
Monitoreo de calcio y otros electrolitos: Es crucial monitorear regularmente los niveles de calcio sérico, fosfato sérico y el producto calcio × fosfato para evitar la calcificación ectópica. El producto calcio × fosfato debe mantenerse por debajo de 55 mg²/dL² (4.4 mmol²/L²) para prevenir la calcificación de los tejidos blandos, como en los riñones y las arterias. La monitorización de los niveles de vitamina D3 (25-(OH) vitamina D) también es importante, con mediciones cada 3 a 4 meses para ajustar la dosis de los suplementos de vitamina D.
Uso de la hormona paratiroidea recombinante (rhPTH)
En algunos casos de hipoparatiroidismo crónico severo, que no responden adecuadamente al tratamiento con calcio y vitamina D, se puede utilizar la hormona paratiroidea recombinante (rhPTH) como tratamiento adjunto. Esta terapia ayuda a controlar la hipocalcemia sintomática al mejorar la reabsorción renal de calcio y aumentar los niveles de calcio sérico. La rhPTH se administra por inyección subcutánea cada 1-2 días. Aunque la rhPTH es eficaz, su uso está limitado por su costo y la posibilidad de efectos secundarios como náuseas, vómitos, diarrea, dolor articular y parestesias. También se ha observado que dosis muy altas de rhPTH pueden inducir osteosarcoma en modelos animales, lo que plantea preocupaciones sobre su seguridad a largo plazo.
Transplante de tejido paratiroideo criopreservado
En casos seleccionados, se puede considerar el trasplante de tejido paratiroideo criopreservado, obtenido durante una cirugía anterior. Este procedimiento tiene la capacidad de restaurar la normocalcemia en aproximadamente el 23% de los casos, aunque no es una opción disponible para todos los pacientes debido a su complejidad y los riesgos asociados.
Manejo del hipoparatiroidismo en el embarazo
El hipoparatiroidismo durante el embarazo plantea desafíos únicos. La hipocalcemia materna puede afectar negativamente el desarrollo esquelético del feto y desencadenar hiperparatiroidismo compensatorio en el recién nacido. Por lo tanto, es importante mantener los niveles de calcio materno en la mitad inferior del rango normal, ya que la hipercalcemia materna puede suprimir el desarrollo de las glándulas paratiroides fetales, lo que puede dar lugar a hipocalcemia neonatal. Se recomienda que los niveles de calcio se determinen cada 4 semanas durante el embarazo y la lactancia, y más frecuentemente en los 3 meses previos y posteriores al parto. Los análogos de la hormona paratiroidea y los diuréticos tiazídicos generalmente se evitan durante el embarazo debido a sus posibles efectos adversos sobre el feto.
Pronóstico
En pacientes con hipoparatiroidismo leve, el pronóstico es generalmente favorable debido a que el trastorno puede mantenerse controlado mediante tratamiento sustitutivo adecuado y un seguimiento clínico riguroso. Esta forma leve de la enfermedad suele permitir una regulación relativamente estable del metabolismo del calcio, siempre que se realicen controles periódicos de los niveles séricos de este mineral. Tales controles son fundamentales porque cualquier alteración, ya sea hipocalcemia o hipercalcemia, puede requerir un ajuste inmediato en el régimen terapéutico. La necesidad de este monitoreo constante radica en la naturaleza dinámica del equilibrio calcio-fosfato en el organismo, el cual depende en gran medida de la actividad de la hormona paratiroidea, ausente o deficiente en estos pacientes.
Una complicación importante que puede surgir incluso en pacientes previamente considerados estables es la hipercalcemia inexplicada. Esta puede ser un signo temprano y revelador de una patología concomitante, como la enfermedad de Addison. Esta relación se debe al hecho de que tanto el hipoparatiroidismo como la insuficiencia suprarrenal forman parte del espectro de los síndromes de autoinmunidad poliglandular, en los cuales múltiples glándulas endocrinas pueden verse afectadas por procesos autoinmunes de forma simultánea o secuencial.
En contraste, los pacientes con hipoparatiroidismo de moderado a severo enfrentan una evolución clínica más compleja y, a menudo, un deterioro significativo en su calidad de vida. Aunque reciban una terapia convencional adecuada —basada en calcio oral y vitamina D activa—, estos individuos presentan un riesgo elevado de desarrollar complicaciones crónicas. Entre estas se encuentran las calcificaciones ectópicas, particularmente en los riñones y los ganglios basales del encéfalo, como consecuencia de un control subóptimo del calcio y el fósforo. Estas calcificaciones pueden dar lugar a nefrocalcinosis, cálculos renales, y disfunción renal progresiva. Asimismo, las alteraciones en los ganglios basales están asociadas con manifestaciones neurológicas como crisis epilépticas, trastornos del ánimo y del comportamiento, e incluso síndromes psiquiátricos complejos, lo que contribuye a una reducción generalizada en la percepción del bienestar personal.
La terapia con hormona paratiroidea recombinante humana (rhPTH) ha emergido como una opción terapéutica prometedora, especialmente en los casos moderados y graves. Este tratamiento busca restaurar, al menos parcialmente, la fisiología endocrina normal del metabolismo del calcio, reduciendo la dependencia de suplementos orales y, potencialmente, previniendo o atenuando muchas de las complicaciones a largo plazo asociadas con la enfermedad. De este modo, la administración de rhPTH no solo contribuye a una mejor regulación bioquímica, sino que también puede mejorar de manera sustancial los síntomas neurológicos, psicológicos y renales, elevando así la calidad de vida global de estos pacientes.

Fuente y lecturas recomendadas:
- Bilezikian JP. Hypoparathyroidism. J Clin Endocrinol Metab. 2020;105:1722. [PMID: 32322899]
- Hamny I et al. New directions in the treatment of hypoparathyroidism. Ann Endocrinol (Paris). 2023;84:460. [PMID: 37080533]
- Khan AA et al. Evaluation and management of hypoparathyroidism. Summary statement and guidelines from the second international workshop. J Bone Miner Res. 2022;37:2568. [PMID: 36054621]
Originally posted on 1 de mayo de 2025 @ 9:03 PM