La enfermedad por aglutininas frías (Cold Agglutinin Disease, CAD) es una anemia hemolítica adquirida que se caracteriza por la presencia de anticuerpos autoimmunes, generalmente de tipo IgM, que se dirigen contra los antígenos I/i en los glóbulos rojos (eritrocitos). Estos anticuerpos son conocidos como aglutininas frías debido a que su capacidad de unirse a los glóbulos rojos depende de la temperatura: reaccionan débilmente a 37°C, la temperatura normal del cuerpo humano, pero reaccionan de manera más vigorosa a temperaturas más bajas, generalmente entre 0 y 4°C. Este comportamiento térmico es clave para entender tanto la fisiopatología como los efectos clínicos de la enfermedad.
En condiciones normales, el sistema inmunológico produce anticuerpos en respuesta a la presencia de patógenos o sustancias extrañas en el organismo. Sin embargo, en la enfermedad por aglutininas frías, los anticuerpos IgM se desarrollan de forma patológica y se unen a los glóbulos rojos en partes del cuerpo que experimentan temperaturas relativamente más frías, como las extremidades (dedos de las manos, pies, nariz y orejas). A estas temperaturas frías, el anticuerpo se une al antígeno I/i de la superficie de los eritrocitos, lo que desencadena una serie de reacciones inmunológicas.
Aunque los anticuerpos IgM rara vez provocan directamente la lisis (destrucción) de los glóbulos rojos, el proceso subyacente comienza con la activación del complemento, una parte del sistema inmunológico que puede amplificar la respuesta inflamatoria y mediada por anticuerpos. A temperaturas frías, la IgM se une a los glóbulos rojos y fija varias proteínas del sistema del complemento, especialmente el C3b. Posteriormente, cuando la sangre regresa a las zonas del cuerpo con temperaturas más cálidas (alrededor de 37°C), la IgM se disocia de los glóbulos rojos, pero el C3b permanece adherido a su superficie. Este fragmento de complemento es reconocido por los células de Kupffer en el hígado, que tienen receptores específicos para C3b. Como resultado, los glóbulos rojos son secuestrados y destruidos en el hígado, lo que provoca una hemólisis extravascular.
Sin embargo, en algunos casos raros, el complejo de ataque de membrana del complemento (MAC) puede formarse en la superficie de los glóbulos rojos, lo que da lugar a hemólisis intravascular, un proceso en el cual los glóbulos rojos son destruidos directamente en los vasos sanguíneos.
La mayoría de los casos de la enfermedad por aglutininas frías son idiopáticos, es decir, su origen es desconocido y no se asocian con ninguna enfermedad subyacente. No obstante, existen algunas condiciones que pueden predisponer al desarrollo de esta enfermedad, como el mieloma macroglobulinémico de Waldenström, ciertos tipos de linfoma y leucemia linfocítica crónica (CLL), que se caracterizan por la producción de una paraproteína monoclonal IgM. En estos casos, la enfermedad por aglutininas frías está vinculada a la producción anómala de anticuerpos IgM que pueden inducir la hemólisis a temperaturas bajas.
Además, la enfermedad por aglutininas frías también puede desarrollarse agudamente después de infecciones virales o bacterianas. Un ejemplo de esto es la neumonía por Mycoplasma pneumoniae, en la cual los anticuerpos IgMproducidos en respuesta a la infección pueden cruzar reacciones con los antígenos de los glóbulos rojos, especialmente el antígeno i, lo que da lugar a una forma postinfecciosa de la enfermedad. También se han descrito formas agudas asociadas con infecciones por mononucleosis infecciosa, sarampión, paperas y citomegalovirus.
En cuanto a los síntomas clínicos, los pacientes con enfermedad por aglutininas frías suelen presentar signos de hemólisis, como ictericia, anemia y, en casos más graves, puede haber signos de daño a los órganos debido a la destrucción masiva de glóbulos rojos. Dado que la hemólisis tiende a ocurrir principalmente en las extremidades frías, los pacientes pueden experimentar síntomas como mialgia (dolor muscular) y acrocyanosis (coloración azulada de los dedos de manos y pies) al exponerse al frío.
El tratamiento de la enfermedad por aglutininas frías se centra en evitar la exposición al frío y en el manejo de la hemólisis. En algunos casos, pueden emplearse inmunosupresores o agentes que inhiben el complemento. En situaciones más graves, puede ser necesario realizar tratamientos de plasmaféresis o emplear fármacos como rituximabpara reducir la producción de anticuerpos IgM anómalos.
Manifestaciones clínicas
En la enfermedad crónica por aglutininas frías, los síntomas clínicos están estrechamente relacionados con la aglutinación de los glóbulos rojos debido a la acción de los anticuerpos IgM dirigidos contra los antígenos I/i en los eritrocitos. Esta aglutinación es más pronunciada cuando los pacientes se exponen a temperaturas frías, ya que los anticuerpos IgM, que tienen la capacidad de unirse a los glóbulos rojos a temperaturas más bajas (por debajo de los 30°C), causan la formación de agregados o “aglutinados” en los vasos sanguíneos. Este fenómeno desencadena una serie de reacciones patológicas que producen los síntomas característicos de la enfermedad.
Cuando los pacientes con enfermedad por aglutininas frías se exponen a ambientes fríos, particularmente en las extremidades, como los dedos de las manos, los pies, las orejas y la nariz, se pueden observar cianosis acrocianótica. Esta es una coloración azulada de las áreas afectadas debido a la reducción del flujo sanguíneo y la aglutinación de los glóbulos rojos, que dificulta la circulación adecuada de la sangre oxigenada. Además, los pacientes pueden experimentar entumecimiento o hormigueo en los dedos o los pies, a medida que la circulación periférica se ve comprometida por los agregados de glóbulos rojos.
El proceso de aglutinación de los glóbulos rojos en condiciones frías también puede desencadenar dolor en las extremidades, lo que se conoce como dolor episódico en la parte baja de la espalda o en las extremidades, debido a la obstrucción parcial de los vasos sanguíneos más pequeños. Este dolor puede estar asociado con la hipoxia local (falta de oxígeno) causada por la alteración del flujo sanguíneo. La exposición continua al frío también puede contribuir al daño tisular en las extremidades afectadas.
Uno de los síntomas más característicos de la hemólisis inducida por aglutininas frías es la orina oscura. Esto se debe a la liberación de hemoglobina libre en el torrente sanguíneo como resultado de la destrucción de los glóbulos rojos, particularmente en las zonas más frías del cuerpo. La hemoglobina libre en la circulación puede filtrarse a través de los riñones y ser excretada en la orina, lo que da lugar a una coloración oscura, que es un signo clínico de hemólisis. En algunos pacientes, esto puede ser episódico y ocurrir solo durante exposiciones al frío.
Aunque la anemia hemolítica en la enfermedad crónica por aglutininas frías puede ser grave en algunos casos, no siempre presenta un cuadro clínico dramático. La severidad de la anemia varía según el grado de hemólisis y la cantidad de glóbulos rojos destruidos, lo que a su vez depende de la intensidad y frecuencia de las exposiciones al frío. En general, la anemia suele ser moderada o leve, pero en algunas situaciones puede agravarse si las exposiciones al frío son prolongadas o recurrentes.
Por otro lado, en las síndromes postinfecciosos agudos relacionados con la enfermedad por aglutininas frías, como aquellos que ocurren después de una infección viral (por ejemplo, mononucleosis infecciosa, sarampión, paperas o citomegalovirus) o bacteriana (como la neumonía por Mycoplasma pneumoniae), la hemólisis tiende a ser menos grave y generalmente es transitoria. Aunque en algunos pacientes la producción de anticuerpos IgM durante una infección puede inducir una respuesta inmune que cause aglutinación de glóbulos rojos, este fenómeno no suele ser lo suficientemente intenso como para producir una anemia hemolítica severa. En estos casos, los síntomas son más leves y se resuelven una vez que la infección se trata o se resuelve por sí sola.
Exámenes complementarios
En la enfermedad por aglutininas frías, la anemia leve es uno de los hallazgos más comunes en los pacientes, aunque la severidad puede variar. Esta anemia es generalmente el resultado de la hemólisis extravascular, un proceso en el que los glóbulos rojos se destruyen en órganos como el hígado y el bazo, en lugar de ser destruidos dentro de los vasos sanguíneos. Durante la hemólisis, el cuerpo responde produciendo una cantidad aumentada de reticulocitos, que son glóbulos rojos inmaduros liberados desde la médula ósea para intentar compensar la pérdida de glóbulos rojos. Este fenómeno de reticulocitosis es indicativo de una respuesta regenerativa a la anemia, aunque el grado de reticulocitosis puede ser moderado o bajo, dependiendo de la intensidad de la hemólisis.
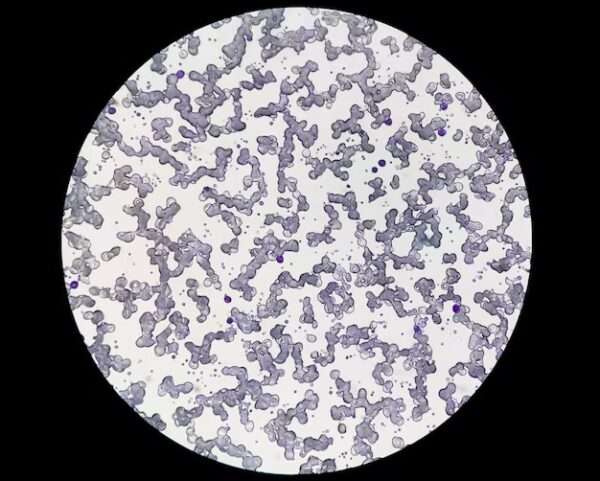
En cuanto a la morfología de los glóbulos rojos, los esferocitos (glóbulos rojos esféricos que carecen de la forma bicóncava típica) rara vez se observan en los frotis de sangre de los pacientes con enfermedad por aglutininas frías, a diferencia de otras formas de anemia hemolítica, como la esferocitosis hereditaria o la anemia autoinmune. En cambio, la característica más distintiva en el frotis sanguíneo es la presencia de aglutinación de glóbulos rojos, que se puede observar solo a temperaturas más bajas, típicamente cuando la muestra de sangre se examina a temperatura ambiente, es decir, entre 18 y 22°C. En cambio, cuando el frotis se prepara y observa a la temperatura del cuerpo (aproximadamente 37°C), no se observa aglutinación, ya que la aglutinina fría (anticuerpo IgM) pierde su capacidad de unirse a los glóbulos rojos a temperaturas normales.
El test directo de antiglobulina (también conocido como prueba de Coombs directa) es una herramienta diagnóstica clave en la evaluación de la enfermedad por aglutininas frías. En este caso, el resultado será positivo solo para complemento, ya que el anticuerpo IgM que se une a los glóbulos rojos activa el sistema del complemento, pero no se fija a la IgG, lo que es típico en otras formas de anemia hemolítica autoinmune. Esto es importante porque diferencia la enfermedad por aglutininas frías de otras formas de hemólisis inmunitaria mediada por anticuerpos IgG.
Además, se puede medir la titulación de las aglutininas frías en suero para cuantificar el nivel de los anticuerpos IgM presentes en el plasma del paciente. Este análisis proporciona una estimación semicuantitativa de la cantidad de autoanticuerpo IgM, lo que ayuda a confirmar el diagnóstico y evaluar la gravedad de la respuesta inmune.
Otro hallazgo relevante es la electroforesis de proteínas séricas, en la cual a menudo se detecta una proteína monoclonal IgM, especialmente en los casos de la enfermedad asociada con trastornos como el mieloma macroglobulinémico de Waldenström o ciertos linfomas. La confirmación de la presencia de esta paraproteína monoclonal se realiza mediante inmunoelectroforesis sérica, que puede identificar la IgM monoclonal y establecer la relación entre esta proteína y los síntomas del paciente.
Durante los episodios de hemólisis, se observan alteraciones en varios parámetros bioquímicos. La hiperbilirrubinemia indirecta (aumento de la bilirrubina no conjugada) es común debido a la liberación de hemoglobina desde los glóbulos rojos destruidos, que posteriormente se metaboliza en bilirrubina. Esta condición es indicativa de una sobrecarga de bilirrubina no conjugada en el cuerpo, derivada de la descomposición de la hemoglobina.
Además, en los períodos de hemólisis activa, los niveles de haptoglobina suelen estar bajos, ya que esta proteína se une a la hemoglobina libre circulante liberada de los glóbulos rojos destruidos, formando complejos que luego son eliminados del cuerpo, particularmente por el hígado. La disminución de haptoglobina es un marcador útil para identificar la hemólisis intravascular o extravascular.
En los casos donde la hemólisis es más intensa, como ocurre ocasionalmente en situaciones de hemólisis intravascular, los niveles de hemoglobina libre en suero se elevan significativamente. La hemoglobina libre circulante, que proviene de los glóbulos rojos destruidos, puede filtrarse a través de los riñones y aparecer en la orina del paciente, lo que se conoce como hemoglobinuria. Este hallazgo es característico de la hemólisis intravascular y se manifiesta como orina de color oscuro, similar a la observada en otras condiciones de hemólisis intravascular, como en el caso de las crisis hemolíticas agudas o en enfermedades como la malaria o el síndrome urémico hemolítico.
Tratamiento
El tratamiento de la enfermedad por aglutininas frías es principalmente sintomático y se enfoca en minimizar los efectos de la hemólisis y prevenir las complicaciones asociadas con la exposición al frío. Dado que la enfermedad se caracteriza por la aglutinación de glóbulos rojos a temperaturas bajas, el enfoque inicial en el manejo de los pacientes se centra en evitar la exposición a ambientes fríos, especialmente en las extremidades, para prevenir la activación de los anticuerpos IgM y la consiguiente aglutinación de los glóbulos rojos. Esto puede implicar el uso de ropa abrigada y precauciones para mantener el cuerpo a una temperatura adecuada, evitando la exposición directa a ambientes fríos.
En cuanto a los tratamientos farmacológicos, se ha encontrado que la esplenectomía y el uso de prednisonageneralmente no son efectivos para el tratamiento de la enfermedad por aglutininas frías, excepto en aquellos casos en los que la enfermedad está asociada con trastornos linfoproliferativos, como el mieloma macroglobulinémico de Waldenström o ciertos tipos de linfoma. Esto se debe a que la hemólisis en la enfermedad por aglutininas frías ocurre principalmente en el hígado y en el torrente sanguíneo, y no en el bazo, por lo que la eliminación del bazo no tiene un impacto significativo en la destrucción de los glóbulos rojos en estos pacientes. La prednisona, un corticosteroide inmunosupresor, no tiene un efecto notable sobre la patogénesis de la enfermedad en la mayoría de los casos, debido a la naturaleza del anticuerpo IgM, que no está mediado por la misma respuesta inmunitaria que en otras formas de anemia autoinmune mediada por IgG.
El tratamiento de elección en la enfermedad por aglutininas frías es el uso de rituximab, un anticuerpo monoclonal dirigido contra el antígeno CD20 de los linfocitos B, que juega un papel crucial en la producción de anticuerpos anómalos. El rituximab tiene la capacidad de reducir la cantidad de linfocitos B que producen los anticuerpos IgM, lo que disminuye la respuesta autoinmune y, por ende, la hemólisis. Sin embargo, su uso debe ser cuidadosamente monitorizado en pacientes con antecedentes de infección por el virus de la hepatitis B, ya que el tratamiento con rituximab puede reactivar la infección por hepatitis B en estos individuos. Por esta razón, en pacientes con historia de infección por hepatitis B, se recomienda administrar profilaxis contra la hepatitis B antes y durante el tratamiento con rituximab para prevenir la reactivación del virus.
La dosificación estándar de rituximab para la enfermedad por aglutininas frías es de 375 mg por metro cuadrado de superficie corporal administrados por vía intravenosa una vez a la semana durante un total de cuatro semanas. Aunque los pacientes pueden experimentar remisiones parciales o completas después de este tratamiento, algunos pueden presentar recaídas, lo que hace necesario un tratamiento adicional con rituximab en esos casos. La reaparición de los síntomas puede responder favorablemente a nuevas rondas de tratamiento, lo que hace que el rituximab sea una opción terapéutica efectiva a largo plazo.
En casos más graves de la enfermedad, especialmente cuando la hemólisis es severa o resistente al tratamiento con rituximab, se puede considerar el uso de inmunoglobulina intravenosa en altas dosis (2 gramos por kilogramo de peso corporal), que puede ser temporalmente eficaz para reducir la hemólisis y mejorar los síntomas. Sin embargo, este tratamiento rara vez se utiliza debido a su alto costo y a la corta duración del beneficio, lo que limita su aplicación en la práctica clínica habitual.
Para los pacientes con formas más graves de la enfermedad, especialmente aquellos con hemólisis persistente o cuando la respuesta a los tratamientos anteriores es insuficiente, se pueden emplear agentes citotóxicos. Medicamentos como el bendamustine (en combinación con rituximab), ciclofosfamida, fludarabina o bortezomib pueden ser utilizados en casos seleccionados, especialmente cuando la enfermedad está asociada con trastornos linfoproliferativos o cuando se sospecha de un componente maligno subyacente. Estos agentes pueden reducir la carga de linfocitos B o T responsables de la producción de los anticuerpos IgM patológicos. Además, también se pueden considerar agentes inmunosupresores, como la ciclosporina, para suprimir la respuesta inmune y controlar la producción de anticuerpos anómalos.
Más recientemente, el bloqueo del complemento se ha convertido en una estrategia terapéutica prometedora para el tratamiento de la enfermedad por aglutininas frías. El sutimlimab, un anticuerpo monoclonal que inhibe la proteína C1sdel sistema del complemento, ha sido aprobado por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) para el tratamiento de la hemólisis asociada a aglutininas frías. El bloqueo del complemento previene la activación del sistema del complemento, lo que reduce la hemólisis mediada por la fijación de complemento a los glóbulos rojos y mejora los resultados clínicos en los pacientes afectados.
En cuanto a las transfusiones de sangre, los pacientes con enfermedad por aglutininas frías pueden enfrentar dificultades para encontrar sangre compatible, debido a la presencia de los anticuerpos IgM que pueden interferir con las pruebas de compatibilidad sanguínea. En estos casos, las transfusiones de glóbulos rojos deben realizarse utilizando un calentador de sangre en línea, que previene la aglutinación de los glóbulos rojos a temperaturas más bajas durante la transfusión.

Fuente y lecturas recomendadas:
- Berentsen, S. How I treat cold agglutinin disease. Blood. 2021;137:1295. [PMID: 33512410]
- Berentsen, S., et al. Autoimmune hemolytic anemias. New England Journal of Medicine. 2021;385:1407. [PMID: 34614331]
- Jäger, U., et al. Diagnosis and treatment of autoimmune hemolytic anemia in adults: recommendations from the First International Consensus Meeting. Blood Reviews. 2020;41:100648. [PMID: 31839434]
- Röth, A., et al. Sutimlimab in cold agglutinin disease. New England Journal of Medicine. 2021;384:1323. [PMID: 33826820]