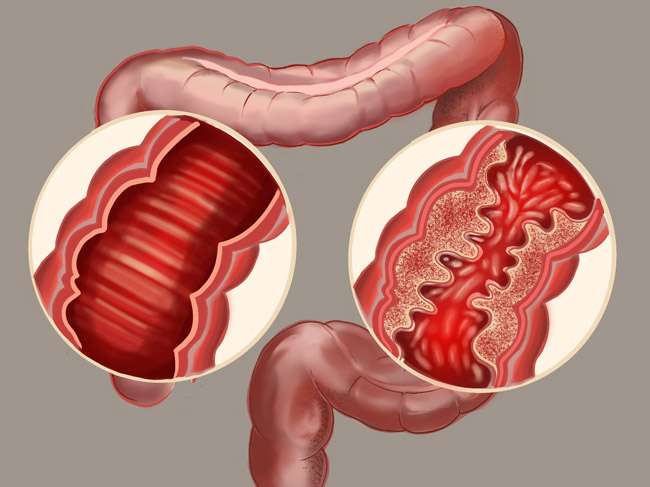
La enfermedad de Crohn es una patología inflamatoria crónica del tracto gastrointestinal que afecta a personas de todas las edades y se caracteriza por la presencia de exacerbaciones y remisiones a lo largo de la vida del paciente. Se trata de una enfermedad autoinmune, en la que el sistema inmunológico del cuerpo ataca por error el tracto digestivo, causando inflamación, úlceras y, en casos más graves, complicaciones estructurales como fístulas, abscesos y estenosis. Esta enfermedad tiene un curso impredecible, donde los pacientes alternan entre periodos de exacerbación de los síntomas y fases de remisión en las cuales la actividad inflamatoria disminuye.
Una de las principales características de la enfermedad de Crohn es que no existe una cura definitiva, por lo que se considera una enfermedad crónica de por vida. No obstante, la evolución de la enfermedad varía considerablemente entre los pacientes. Mientras que algunos pueden experimentar formas leves o intermitentes de la enfermedad, que no presentan una progresión significativa, otros desarrollan una afección más agresiva que requiere tratamiento intensivo y vigilancia a largo plazo. Aunque no hay una terapia específica que cure la enfermedad, la intervención temprana es fundamental para reducir la carga clínica y evitar complicaciones graves.
En este sentido, se ha demostrado que un tratamiento precoz que logre la remisión endoscópica e histológica (es decir, la reducción de la inflamación visible a través de endoscopia y la normalización de los marcadores histológicos de inflamación) se asocia con un menor riesgo de complicaciones. Estas complicaciones incluyen fístulas (canales anormales que se desarrollan entre diferentes partes del intestino o entre el intestino y otros órganos), abscesos (acumulaciones de pus debidas a infecciones locales) y la necesidad de intervenciones quirúrgicas para corregir lesiones o perforaciones. Así, la estratificación del riesgo, es decir, la identificación de los factores que indican un mayor riesgo de un curso agresivo de la enfermedad, se convierte en una herramienta esencial para guiar la selección del tratamiento adecuado, permitiendo a los médicos ofrecer terapias personalizadas que mejoren los resultados a largo plazo de los pacientes.
Entre los factores de riesgo para un curso más agresivo de la enfermedad, se destacan varios elementos clínicos y demográficos. En primer lugar, la edad joven al inicio de los síntomas está asociada con un peor pronóstico, ya que los pacientes que desarrollan la enfermedad en etapas tempranas de la vida tienen una mayor probabilidad de presentar complicaciones a lo largo de su vida. Además, aquellos que requieren corticosteroides de manera temprana para controlar la inflamación también se encuentran en un riesgo más alto, ya que el uso prolongado de estos fármacos puede reflejar una enfermedad más agresiva y resistente a otras terapias.
Otro factor importante es la presencia de enfermedad perianal, fístulas o estenosis (estrechamientos del intestino), que indican un tipo de Crohn más complejo y difícil de manejar. La afectación del tracto gastrointestinal superior, que implica la participación de órganos como el esófago o el estómago, también está asociada con un mayor riesgo de complicaciones graves. Además, los marcadores de laboratorio de inflamación severa, tales como niveles bajos de albúmina (una proteína producida por el hígado que puede disminuir en respuesta a la inflamación crónica), hemoglobina baja (indicativa de anemia, a menudo relacionada con sangrados en el tracto digestivo), y marcadores inflamatorios como la proteína C reactiva (CRP) o la calprotectina fecal (una proteína asociada con la inflamación intestinal), son señales de que la enfermedad está avanzando o es más activa, lo que puede justificar un tratamiento más intensivo. Además, los hallazgos endoscópicos, como la presencia de úceras profundas en el tracto digestivo, también son indicativos de un curso más severo de la enfermedad y sugieren la necesidad de un enfoque terapéutico más agresivo para prevenir daños adicionales.
En términos de prevalencia, aproximadamente entre el 20 y el 30% de los pacientes con enfermedad de Crohn experimentan un curso leve e intermitente de la enfermedad. Esto significa que la inflamación no progresa de manera significativa, y los pacientes pueden pasar largos periodos sin síntomas graves. Sin embargo, la mayoría de los pacientes tienen una enfermedad de moderada a severa, la cual requiere una gestión activa. Para estos pacientes, el uso temprano de terapias biológicas (medicamentos que modifican la respuesta inmune y reducen la inflamación) ha demostrado ser efectivo en el control de la enfermedad y en la prevención de su progresión. Estas terapias pueden frenar la inflamación, prevenir el daño intestinal y reducir la necesidad de intervenciones quirúrgicas. De este modo, la intervención temprana y la elección de tratamientos adecuados, basados en la estratificación del riesgo, son fundamentales para mejorar la calidad de vida de los pacientes y reducir las complicaciones a largo plazo.
Enfermedad de riesgo leve/bajo
La enfermedad de Crohn es un trastorno inflamatorio crónico del tracto gastrointestinal, caracterizado por la inflamación que puede afectar cualquier parte del tracto digestivo, desde la boca hasta el ano. Sin embargo, cuando se describe a los pacientes como aquellos con enfermedad leve y bajo riesgo de progresión, se hace referencia a una forma menos agresiva de la enfermedad, en la que la inflamación es limitada, los síntomas son poco severos y no hay evidencia de complicaciones graves.
Características de la Enfermedad Leve y de Bajo Riesgo
Los pacientes con enfermedad de Crohn leve y bajo riesgo de progresión se distinguen por varios factores clínicos que indican un curso menos agresivo de la enfermedad. Uno de los aspectos más importantes es la presencia de síntomas leves. Estos pacientes suelen experimentar dolor abdominal y diarrea, pero estos síntomas no son debilitantes y no interfieren gravemente con las actividades diarias. Además, la pérdida de peso significativa es poco común, lo que sugiere que el estado nutricional del paciente se mantiene adecuado.
Los marcadores inflamatorios son otro criterio fundamental. En estos pacientes, los niveles de proteína C-reactiva (PCR), calprotectina fecal y albúmina sérica son normales o solo ligeramente elevados. Estos biomarcadores son indicadores clave de la inflamación en el cuerpo, y su normalidad sugiere que la respuesta inflamatoria es mínima.
La ausencia de complicaciones intestinales graves es otro factor distintivo. Los pacientes con enfermedad leve no presentan estenosis (estrechamiento del intestino), abscesos (acumulaciones de pus) ni fístulas (conexiones anormales entre órganos o tejidos). Tampoco se observan problemas perianales, como fisuras o abscesos. A nivel histológico, el compromiso intestinal está limitado a úlceras mucosas superficiales, sin penetración profunda o daño a las capas más profundas del intestino. Estas características sugieren que la enfermedad está controlada y no está progresando de manera significativa hacia formas más complicadas.
Enfoque Nutricional
El manejo nutricional es un pilar fundamental en la atención de los pacientes con enfermedad de Crohn, particularmente aquellos con una forma leve. Se recomienda una dieta equilibrada que contenga todos los grupos alimenticios esenciales para mantener el estado nutricional y evitar deficiencias. Las restricciones dietéticas deben ser mínimas, ya que un enfoque demasiado restrictivo puede llevar a una mala adherencia y a la desnutrición. En algunos casos, puede ser útil adoptar el enfoque de comer porciones más pequeñas pero más frecuentes, lo cual facilita la digestión y reduce la carga sobre el sistema digestivo.
Los pacientes con diarrea deben ser animados a consumir líquidos adecuados para prevenir la deshidratación, un riesgo común en la enfermedad de Crohn. En cuanto a los alimentos, algunos pacientes experimentan un empeoramiento de los síntomas tras consumir alimentos fritos o grasos, por lo que se recomienda evitarlos en la dieta. Dado que la intolerancia a la lactosa es frecuente en estos pacientes, se sugiere eliminar los productos lácteos si los síntomas, como la flatulencia o la diarrea, son prominentes. En cuanto a los probióticos, aunque algunos pacientes pueden buscarlos como una opción de tratamiento, no hay evidencia robusta que demuestre que estos suplementos sean beneficiosos en el tratamiento de la enfermedad de Crohn.
Terapia Sintomática
En cuanto al manejo de los síntomas, se puede utilizar la loperamida para controlar la diarrea. La dosis recomendada es de 2 a 4 mg según sea necesario, con un máximo de cuatro dosis al día. Este medicamento ayuda a disminuir la motilidad intestinal y, por ende, mejora la frecuencia de las deposiciones en los pacientes con diarrea. Sin embargo, el uso de loperamida debe ser vigilado, ya que el tratamiento excesivo de la diarrea podría llevar a otros problemas gastrointestinales.
Terapia Farmacológica
El tratamiento farmacológico es un aspecto fundamental para controlar la enfermedad de Crohn y prevenir su progresión. En los pacientes con enfermedad leve de bajo riesgo, se inicia generalmente con medicamentos de menor potencia pero con menos riesgo de efectos adversos. El tratamiento se adapta en función de la localización y extensión de la enfermedad.
a. Enfermedad en el Íleon Terminal o Colon Ascendente
En los pacientes con enfermedad leve que afecta el íleon terminal o el colon ascendente, se recomienda la utilización de budesonida de liberación prolongada (Entocort), un corticosteroide de acción local que actúa principalmente en el tracto gastrointestinal. Este medicamento se administra en dosis de 9 mg al día durante 8 semanas, con el objetivo de inducir la remisión en un 50-70% de los pacientes. Si se consigue la remisión, la dosis de budesonida debe reducirse gradualmente para evitar efectos adversos, y el paciente debe ser vigilado.
En algunos casos, agentes 5-ASA (ácido 5-aminosalicílico) pueden ser utilizados, aunque la evidencia clínica de su efectividad es limitada. Estas formulaciones liberan mesalamina en el intestino delgado distal, como en el caso de Asacolo Pentasa. Aunque los datos clínicos no son concluyentes, siguen siendo una opción común para el tratamiento de la enfermedad ileocolónica leve.
b. Colitis Izquierda o Difusa
Para los pacientes con colitis leve, ya sea difusa o limitada al lado izquierdo del colon, se recomienda el uso de corticosteroides orales como prednisona o prednisolona. La dosis inicial es de 40 mg al día durante 1–2 semanas, y, si hay respuesta, se realiza una reducción gradual de la dosis. También se puede utilizar sulfasalazina (1.5–3 g dos veces al día), especialmente en pacientes con enfermedad que afecta el colon, pero este medicamento tiene el potencial de generar efectos secundarios graves en una proporción significativa de pacientes. Si los pacientes responden bien, la dosis puede reducirse a 2–4 g al día como tratamiento de mantenimiento.
Si la sulfasalazina no es tolerada o presenta efectos adversos, otros agentes 5-ASA, como mesalamina de liberación retardada o balsalazida, son alternativas para el manejo de la colitis leve.
Seguimiento a Largo Plazo
El seguimiento de los pacientes con enfermedad leve de Crohn es esencial para detectar cualquier signo de recurrencia o progresión. En aquellos que responden favorablemente al tratamiento inicial con budesonida o prednisona, se debe suspender gradualmente la medicación y realizar un monitoreo periódico a través de pruebas de laboratorio (como la PCR y la calprotectina fecal) o endoscopia cada 1–2 años. Si el paciente responde al tratamiento con sulfasalazina o agentes 5-ASA, se continúa con la terapia de mantenimiento a largo plazo.
Los pacientes que no responden al tratamiento inicial o que experimentan recaídas frecuentes deben ser reevaluados y clasificados como de riesgo moderado o alto para la progresión de la enfermedad. Estos pacientes requieren un cambio en el tratamiento hacia terapias más potentes, como corticosteroides orales, inmunomoduladores o agentes biológicos.
Enfermedad de Crohn de moderado a grave/alto riesgo
En su forma moderada a grave, la enfermedad se caracteriza por síntomas gastrointestinales prominentes y complicaciones relacionadas con una inflamación significativa y disfunción intestinal. Los pacientes con esta forma de la enfermedad suelen experimentar diarrea frecuente, que es uno de los síntomas más comunes debido a la alteración de la motilidad intestinal y la inflamación crónica del tracto digestivo. La diarrea puede ir acompañada de una pérdida de peso significativa, ya que la absorción de nutrientes se ve comprometida debido a la inflamación y al daño de las vellosidades intestinales. Además, el dolor abdominal diario y la sensibilidad en el abdomen son frecuentes, dado que la inflamación constante irrita los nervios sensitivos en la pared intestinal, lo que genera un malestar persistente.
Otro signo clínico característico de la enfermedad de Crohn moderada a grave es la presencia de manifestaciones perianales. Estas pueden incluir fisuras, fístulas y abscesos que se desarrollan debido a la inflamación crónica y penetrante de las áreas cercanas al ano. Esta afectación perianal es un indicador de la severidad de la enfermedad, ya que implica un compromiso significativo de los tejidos más profundos de la pared intestinal.
En cuanto a los hallazgos bioquímicos e inflamatorios, los pacientes con enfermedad moderada a grave de Crohn suelen presentar elevaciones de la proteína C reactiva (PCR), que es un marcador sensible de inflamación aguda. La elevación de este marcador refleja la intensidad de la respuesta inflamatoria en el organismo, que en el caso de la enfermedad de Crohn es típicamente activa y difusa. La anemia también es común en estos pacientes, y generalmente se debe a una combinación de pérdida crónica de sangre (a menudo microscópica), deficiencia de nutrientes como el hierro debido a la mala absorción y la inflamación sistémica que afecta la producción de glóbulos rojos. La disminución de los niveles de albúmina sérica es otro indicador clave de la inflamación, ya que la albúmina, una proteína producida por el hígado, se pierde a través del intestino inflamado y su síntesis disminuye en respuesta a la inflamación crónica. La calprotectina fecal, otro biomarcador de inflamación intestinal, suele estar elevada en estos casos, ya que se libera por los neutrófilos en el sitio de la inflamación intestinal.
Desde el punto de vista diagnóstico, las técnicas de endoscopia y las imágenes radiológicas son fundamentales para evaluar la gravedad de la enfermedad. En los casos más graves, las endoscopias pueden revelar úlceras profundas, estenosis (estrechamientos) o signos de enfermedad penetrante, donde la inflamación afecta no solo a la mucosa, sino que se extiende a capas más profundas de la pared intestinal e incluso a estructuras adyacentes. Estas alteraciones son indicativas de una forma de enfermedad de Crohn que puede ser potencialmente discapacitante y que requiere intervención terapéutica inmediata.
El tratamiento de la enfermedad de Crohn moderada a grave se centra en el control de la inflamación y la mejora de la calidad de vida del paciente. El objetivo principal es lograr una remisión clínica sostenida y una curación de la mucosa intestinal, lo que se traduce en la «remisión endoscópica», en la que los hallazgos de la endoscopia muestran una mucosa completamente cicatrizada y sin signos de inflamación activa. Para lograr este objetivo, se recurre a terapias biológicas, que son tratamientos dirigidos específicamente a las moléculas que promueven la inflamación, como los inhibidores de TNF (factor de necrosis tumoral) o las terapias que bloquean las integrinas o interleucinas. Estos agentes biológicos suelen administrarse en combinación con inmunomoduladores en algunos pacientes, con el fin de optimizar la respuesta terapéutica y reducir el riesgo de recaídas.
La elección de las terapias depende de varios factores, como la edad del paciente, las comorbilidades asociadas, las preferencias individuales del paciente, la presencia de manifestaciones extraintestinales (como artritis, uveítis o enfermedad hepática) y las consideraciones de los aseguradores. Es fundamental personalizar el tratamiento para cada paciente, ya que la enfermedad de Crohn puede manifestarse de manera diferente en cada individuo, y lo que funciona para un paciente puede no ser adecuado para otro.
A pesar de los avances terapéuticos, alcanzar una remisión clínica sostenida con curación de la mucosa intestinal no siempre es posible en todos los pacientes. Algunos pacientes pueden experimentar recaídas frecuentes o una resistencia a los tratamientos, lo que dificulta la consecución de los objetivos terapéuticos. Sin embargo, el tratamiento temprano y agresivo con agentes biológicos ha demostrado mejorar significativamente el pronóstico de la enfermedad, permitiendo que muchos pacientes lleven una vida más saludable y libre de complicaciones graves.
Nutrición
Los pacientes con síntomas obstructivos en el tracto gastrointestinal, como los que se presentan en diversas formas de Enfermedad Inflamatoria Intestinal, deben seguir una dieta específica que minimice la irritación y la obstrucción intestinal, con el objetivo de reducir los síntomas y mejorar la calidad de vida. Una de las recomendaciones fundamentales es seguir una dieta baja en fibra. La fibra dietética, especialmente la que se encuentra en frutas y verduras crudas, así como en alimentos como las palomitas de maíz y los frutos secos, puede ser difícil de digerir y, en muchos casos, puede contribuir a la formación de partículas que obstruyen el intestino, empeorando los síntomas obstructivos. Esta restricción ayuda a evitar el riesgo de que los fragmentos fibrosos se acumulen en áreas donde la motilidad intestinal está alterada o donde existe una estenosis (estrechamiento) en el intestino. Los alimentos de alto contenido de fibra, al no ser completamente digeridos, pueden aumentar la presión intraabdominal y dificultar el paso normal de los alimentos, exacerbando la distensión y el dolor abdominal, síntomas comunes en los pacientes con obstrucción intestinal.
Además, la reducción de la ingesta de alimentos procesados se recomienda para los pacientes con Enfermedad Inflamatoria Intestinal, debido a que estos productos suelen contener aditivos, conservantes, grasas trans y azúcares refinados, componentes que pueden desencadenar o agravar la inflamación intestinal. Se ha demostrado que los alimentos procesados, especialmente los de baja calidad nutricional, tienen un impacto negativo sobre la microbiota intestinal, promoviendo un ambiente inflamatorio en el tracto gastrointestinal. De hecho, el consumo frecuente de estos alimentos ha sido asociado con un mayor riesgo de desarrollar o empeorar la Enfermedad Inflamatoria Intestinal, ya que los ingredientes artificiales y las grasas de baja calidad pueden alterar la integridad de la barrera intestinal y aumentar la permeabilidad intestinal, lo que facilita la entrada de patógenos y moléculas proinflamatorias en el organismo.
En pacientes con Enfermedad Inflamatoria Intestinal activa y pérdida de peso progresiva, el tratamiento nutricional adecuado es esencial para el manejo general de la enfermedad. En algunos casos, cuando el paciente no puede tolerar la alimentación enteral (es decir, la nutrición administrada a través del tracto gastrointestinal) debido a complicaciones como obstrucciones de alto grado, fístulas de alto flujo, diarrea grave o dolor abdominal intenso, se recurre a la nutrición parenteral. La nutrición parenteral implica la administración de nutrientes por vía intravenosa, lo que permite proporcionar una fuente de energía, proteínas, lípidos, vitaminas y minerales sin pasar por el tracto digestivo. Este enfoque es utilizado a corto plazo en pacientes que presentan desnutrición y que no son capaces de consumir alimentos por vía oral o enteral debido a las complicaciones mencionadas. Además, la nutrición parenteral es frecuentemente indicada en aquellos pacientes que esperan cirugía, ya que la desnutrición puede complicar la intervención quirúrgica y la recuperación postoperatoria.
En relación con la nutrición parenteral y los tratamientos adicionales, es común que los pacientes con resección del íleon (especialmente si involucra el íleon terminal) o con enfermedad extensa en esta zona del intestino necesiten suplementos vitamínicos específicos. La resección ileal, que implica la extirpación de una porción del intestino delgado, compromete la absorción de varios nutrientes esenciales, entre ellos la vitamina B12. Este déficit es particularmente importante porque la vitamina B12 es crucial para la función nerviosa y la producción de glóbulos rojos. Dado que el íleon es el sitio principal de absorción de esta vitamina, los pacientes con resección ileal requieren un aporte adicional de vitamina B12 para prevenir deficiencias, que pueden llevar a anemia megaloblástica, neuropatías y otros trastornos relacionados. La administración subcutánea de vitamina B12 (generalmente 1000 microgramos al mes) es una estrategia común para asegurar niveles adecuados en estos pacientes.
Por otro lado, la vitamina D también es frecuentemente insuficiente en pacientes con Enfermedad Inflamatoria Intestinal, particularmente en aquellos con resección ileal, debido a la alteración en la absorción de grasa y, en consecuencia, de vitaminas liposolubles como la vitamina D. La deficiencia de vitamina D puede aumentar el riesgo de osteoporosis, fracturas óseas y debilidad muscular, lo que refuerza la necesidad de suplementos orales de vitamina D en este grupo de pacientes. Estos suplementos no solo ayudan a mantener la salud ósea, sino que también tienen un papel en la modulación de la respuesta inmunitaria, lo que puede ser beneficioso en el contexto de una enfermedad inflamatoria crónica como la Enfermedad Inflamatoria Intestinal.
Terapia sintomática
La enfermedad de Crohn es un trastorno inflamatorio crónico que afecta a cualquier parte del tracto gastrointestinal, pero cuando involucra el íleon terminal, puede inducir una serie de complicaciones metabólicas y digestivas que alteran la absorción normal de nutrientes. El íleon terminal es una zona crucial para la absorción de ciertos nutrientes, especialmente las sales biliares, que son esenciales para la digestión y absorción de las grasas. La afectación del íleon terminal en la enfermedad de Crohn o una resección ileal previa puede comprometer la capacidad del intestino para absorber estas sales biliares de manera eficiente. Las sales biliares son liberadas por el hígado en la bilis y se almacenan en la vesícula biliar para ser liberadas en el intestino delgado, donde facilitan la emulsificación y absorción de las grasas y las vitaminas liposolubles. Cuando el íleon terminal está dañado o ha sido parcialmente extirpado, las sales biliares no se reabsorben adecuadamente y pasan al colon. Esta mala absorción de sales biliares puede inducir una forma de diarrea conocida como diarrea secretoria.
La diarrea secretoria resulta de la presencia de sales biliares no absorbidas en el colon, donde tienen un efecto laxante. Estas sales biliares actúan como irritantes, aumentando la secreción de líquidos y electrolitos en el colon, lo que resulta en una evacuación más frecuente y acuosa. En este contexto, los agentes que se unen a las sales biliares mal absorbidas son fundamentales para reducir los síntomas de diarrea. Medicamentos como la colestiramina y el colestipol se utilizan para unir las sales biliares y prevenir su acción irritante en el colon. La colestiramina se administra generalmente en dosis de 2 a 4 gramos, y el colestipol en dosis de 1 a 2 gramos, una a tres veces al día con las comidas, para maximizar la absorción de las grasas y minimizar la diarrea. Alternativamente, el colesevelam, un medicamento similar, puede ser utilizado en dosis de 625 miligramos, de una a tres tabletas, dos veces al día. Estos agentes ayudan a controlar la diarrea secretoria al limitar la cantidad de sales biliares no absorbidas que llegan al colon.
Sin embargo, en pacientes con enfermedad ileal extensa, en la que se ha reseccionado más de 100 centímetros del íleon, la malabsorción de sales biliares es más grave. Esta deficiencia severa de sales biliares impide la correcta emulsificación de las grasas en el intestino, lo que lleva a una disminución en la absorción de grasas y otros nutrientes. Esto resulta en una condición conocida como esteatorrea, caracterizada por heces grasas, voluminosas y malolientes debido a la presencia de grasas no digeridas. En estos casos, la administración de agentes que se unen a las sales biliares no es eficaz y, de hecho, puede empeorar la diarrea, ya que el exceso de sales biliares no absorbidas en el colon ya está contribuyendo a la diarrea secretoria. En lugar de estos agentes, los pacientes con malabsorción grave de sales biliares pueden beneficiarse de una dieta baja en grasas, ya que reduce la carga sobre el sistema digestivo y limita la cantidad de grasas no absorbidas que llegan al colon.
Otro factor relevante en los pacientes con enfermedad de Crohn, especialmente aquellos con resección ileal o fístulas enterales, es el riesgo de sobrecrecimiento bacteriano del intestino delgado (SIBO, por sus siglas en inglés). Este síndrome se desarrolla cuando las bacterias que normalmente residen en el colon se trasladan al intestino delgado, donde su proliferación excesiva interfiere con la digestión y absorción de nutrientes. En los pacientes con enfermedad de Crohn, la presencia de fístulas enterales, la resección ileal o la alteración en la motilidad intestinal pueden crear un ambiente propenso para este sobrecrecimiento bacteriano. El SIBO puede contribuir a la diarrea y a otros síntomas digestivos, como distensión abdominal, flatulencia y malabsorción de nutrientes. En tales casos, el tratamiento con antibióticos de amplio espectro, como la rifaximina, puede ser útil para controlar la proliferación bacteriana y mejorar los síntomas. El tratamiento antibiótico no solo ayuda a reducir la carga bacteriana, sino que también puede aliviar la inflamación y mejorar la absorción de nutrientes.
Además de la diarrea secretoria y el sobrecrecimiento bacteriano, otras causas de diarrea en pacientes con enfermedad de Crohn incluyen la deficiencia de lactasa y el síndrome de intestino corto. La deficiencia de lactasa es una condición en la que el cuerpo no produce suficiente lactasa, la enzima que descompone la lactosa, el azúcar presente en la leche. Los pacientes con enfermedad de Crohn, especialmente aquellos con resección intestinal, pueden experimentar una intolerancia a la lactosa secundaria a la alteración en la función digestiva, lo que puede causar diarrea, distensión abdominal y malestar después del consumo de productos lácteos. Por otro lado, el síndrome de intestino corto, que ocurre cuando se ha reseccionado una porción significativa del intestino delgado, puede dar lugar a malabsorción generalizada y diarrea crónica debido a la incapacidad del intestino restante para absorber adecuadamente los nutrientes.
En algunos pacientes con enfermedad de Crohn, el uso de agentes antidiarreicos orales puede ser beneficioso para controlar los episodios de diarrea, especialmente cuando estos son limitados a cuadros más leves o cuando la diarrea no responde a las medidas dietéticas o terapéuticas más específicas. Los agentes antidiarreicos, como la loperamida, actúan al reducir la motilidad intestinal y la secreción de líquidos, proporcionando alivio sintomático temporal. Sin embargo, estos agentes deben ser utilizados con precaución, ya que en algunos casos pueden empeorar las complicaciones de la enfermedad, como la obstrucción intestinal.
Terapia farmacológica
El tratamiento farmacológico de la enfermedad de Crohn moderada a grave tiene como objetivo principal inducir y mantener la remisión clínica de la enfermedad, lo cual incluye, siempre que sea posible, la curación de la mucosa intestinal. La enfermedad de Crohn es un trastorno inflamatorio crónico del tracto gastrointestinal que puede tener un curso impredecible y a menudo debilitante, lo que hace que la intervención terapéutica sea crucial para controlar los síntomas y prevenir complicaciones a largo plazo.
Corticosteroides: Los corticosteroides son medicamentos potentes que suprimen de manera rápida y eficaz la inflamación, lo que permite controlar los síntomas agudos y los signos clínicos de la enfermedad de Crohn en la mayoría de los pacientes. La rápida acción de estos fármacos hace que sean una opción terapéutica común para los pacientes con enfermedad moderada a grave. Los corticosteroides actúan inhibiendo la liberación de mediadores inflamatorios, lo que ayuda a reducir la inflamación en el tracto gastrointestinal y proporciona una mejoría sintomática rápida. En estos pacientes, los corticosteroides permiten una mejora clínica temprana, lo cual es particularmente importante cuando los síntomas de la enfermedad son graves, tales como diarrea intensa, dolor abdominal, fiebre y pérdida de peso significativa.
Sin embargo, aunque los corticosteroides pueden mejorar significativamente los síntomas agudos, no alteran la historia natural de la enfermedad subyacente ni modifican el curso crónico de la enfermedad de Crohn. Es decir, los corticosteroides no curan la enfermedad, sino que solo alivian temporalmente la inflamación. Por esta razón, los corticosteroides se utilizan típicamente en combinación con otros agentes modificadores de la enfermedad, que tienen un inicio de acción más lento pero que pueden ayudar a controlar la enfermedad a largo plazo. En muchos casos, los pacientes que responden positivamente a los corticosteroides se beneficiarán de la introducción de terapias biológicas u otros inmunosupresores mientras se reduce gradualmente la dosis de corticosteroides.
La administración de corticosteroides en pacientes con enfermedad de Crohn moderada a grave puede realizarse de manera ambulatoria o en un entorno hospitalario, dependiendo de la gravedad de los síntomas. En los casos graves, especialmente aquellos con fiebre alta, vómitos persistentes, evidencia de obstrucción intestinal, o signos de absceso, puede ser necesaria la hospitalización para un manejo más intensivo. En estos pacientes, antes de iniciar el tratamiento con corticosteroides, se debe realizar una evaluación cuidadosa para descartar complicaciones graves, como un absceso abdominal, mediante pruebas de imagen como la tomografía computarizada. Si no se identifica un absceso, se puede administrar metilprednisolona parenteral en dosis de 40 a 60 miligramos diarios para suprimir la inflamación. Para los pacientes ambulatorios, la prednisona oral o la metilprednisolona se administran generalmente en dosis de 40 miligramos al día durante 1-2 semanas, seguidas de una reducción gradual para evitar efectos secundarios a largo plazo.
El uso de corticosteroides a largo plazo se debe evitar siempre que sea posible debido a los efectos secundarios asociados, como la osteoporosis, la hipertensión, el aumento de peso, la diabetes y las infecciones. En los casos en que se considere necesario mantener a un paciente en tratamiento a largo plazo, se recomienda la adición de un inmunomodulador, como azatioprina, mercaptopurina o metotrexato, para reducir la dependencia de los corticosteroides y evitar las complicaciones derivadas del uso prolongado de estos fármacos. Sin embargo, se estima que alrededor del 20% de los pacientes no pueden suspender completamente los corticosteroides sin experimentar un brote sintomático, lo que subraya la necesidad de un enfoque terapéutico integral que incluya agentes de acción más lenta para el manejo a largo plazo de la enfermedad.
Terapias biológicas: Las terapias biológicas han revolucionado el tratamiento de la enfermedad de Crohn, especialmente en pacientes con formas moderadas a graves. Estas terapias están diseñadas para dirigirse a moléculas específicas que participan en la inflamación, como el factor de necrosis tumoral (TNF), las integrinas y las interleucinas, lo que permite controlar la inflamación de manera más precisa y eficaz que los tratamientos convencionales. Los agentes biológicos son especialmente útiles en pacientes que no responden adecuadamente a los corticosteroides o que experimentan efectos secundarios intolerables con estos fármacos.
La terapia de inducción con un agente biológico se recomienda para casi todos los pacientes con enfermedad de Crohn moderada a grave. Los agentes biológicos disponibles incluyen anticuerpos monoclonales anti-TNF, como infliximab, adalimumab y certolizumab, anticuerpos monoclonales anti-integrinas, como vedolizumab, y anticuerpos monoclonales anti-interleucinas, como ustekinumab y risankizumab. Estos fármacos tienen como objetivo bloquear la acción de las moléculas que promueven la inflamación, como el TNF y las integrinas, que están involucradas en el proceso inflamatorio que caracteriza la enfermedad de Crohn.
La elección del agente biológico adecuado depende de diversos factores, como la gravedad de la enfermedad, la edad del paciente, las comorbilidades, las preferencias del paciente y el costo de los medicamentos. En la práctica clínica, los agentes anti-TNF han sido la terapia de primera línea preferida en la mayoría de los pacientes debido a su eficacia comprobada, el perfil de seguridad conocido, la experiencia clínica acumulada y los costos relativamente más bajos en muchos casos. Además, los meta-análisis en red sugieren que los agentes anti-TNF son superiores a otros agentes biológicos en términos de eficacia para inducir la remisión en pacientes con enfermedad de Crohn moderada a grave.
No obstante, la aparición de nuevos agentes biológicos con excelente eficacia y perfiles de seguridad, como el vedolizumab y el ustekinumab, está comenzando a cambiar la toma de decisiones de los médicos y los pacientes. Estos nuevos agentes ofrecen ventajas importantes, como un menor riesgo de inmunogenicidad (lo que significa que el sistema inmune tiene menos probabilidades de generar anticuerpos contra el fármaco) y la posibilidad de administrar el tratamiento sin la necesidad de co-terapia con inmunomoduladores, lo que podría hacerlos más atractivos para algunos pacientes.

Fuente y lecturas recomendadas:
- Barberio B et al. Efficacy of biological therapies and small molecules in induction and maintenance of remission in luminal Crohn’s disease: systematic review and network meta-analysis. Gut. 2023;72:264. [PMID: 35907636]
- D’Haens G et al. Risankizumab as induction therapy for Crohn’s disease: results from the phase 3 ADVANCE and MOTIVATE induction trials. Lancet. 2022;399:2015. [PMID: 35644154]
- Ferrante M et al. Risankizumab as maintenance therapy for moderately to severely active Crohn’s disease: results from the multicentre, randomised, double-blind, placebo-controlled, withdrawal phase 3 FORTIFY maintenance trial. Lancet. 2022;399:2031. [PMID: 35644155]
- Loftus EV et al. Upadacitinib induction and maintenance therapy for Crohn’s disease. N Engl J Med. 2023;388:1966. [PMID: 37224198]
- Parian A et al. Management of perianal Crohn’s disease. Am J Gastroenterol. 2023;118:1323. [PMID: 37207318]
Originally posted on 8 de enero de 2025 @ 9:19 AM